Clear Sky Science · fr
Le signal calcique pyrimidinergique relie le métabolisme tubulaire à la fibrose dans les maladies rénales
Pourquoi la cicatrisation rénale compte
La maladie rénale chronique touche silencieusement des centaines de millions de personnes dans le monde et se termine souvent par des reins cicatrisés et rigides. Une fois cette cicatrisation — appelée fibrose — installée, la récupération de la fonction rénale est difficile. Pourtant, les médecins disposent encore de peu de médicaments ciblant spécifiquement la fibrose. Cette étude pose une question simple mais cruciale : comment des lésions à court terme des tubules filtrants du rein se transforment-elles progressivement en tissu cicatriciel durable, et interrompre cette chaîne d’événements pourrait-il ralentir ou prévenir l’insuffisance rénale ?
Des tubules rénaux actifs et leur chimie cachée
Les tubules proximaux du rein sont des petits ouvriers microscopiques qui reprennent la majeure partie de l’eau et des nutriments filtrés du sang. Pour accomplir ce travail, leur chimie est remarquablement active. En analysant des données d’expression génique cellule par cellule provenant de reins de souris, les chercheurs ont constaté que ces cellules tubulaires sont particulièrement riches en gènes impliqués dans le métabolisme des pyrimidines, une famille de petites molécules qui participent normalement à la synthèse et à la réparation de l’ADN et de l’ARN. Dans les tubules lésés, une enzyme d’une voie de « recyclage », la cytidine désaminase, était fortement augmentée, ce qui suggère que les cellules endommagées réorganisent l’utilisation des pyrimidines pour maintenir certains éléments riches en énergie, dont un composé appelé UDP.
Signaux qui s’échappent des cellules endommagées
Lorsque l’équipe a endommagé en culture des cellules humaines de type tubulaire avec des toxines imitant la chimiothérapie ou un surdosage en acide folique, ces cellules ont libéré de l’UDP dans le milieu environnant. Dans des reins de souris réellement exposés à une lésion, des colorations de coupes tissulaires ont montré à la fois de forts niveaux de l’enzyme de gestion des pyrimidines dans les tubules et des signes que les cellules de soutien voisines, appelées fibroblastes, s’activaient et changeaient de forme. Les fibroblastes restent normalement silencieux entre les tubules, mais une fois activés ils se multiplient et contribuent à déposer du collagène et d’autres fibres qui épaississent et rigidifient le tissu rénal. Ces observations suggèrent une idée simple : les tubules endommagés pourraient « déverser » des signaux chimiques de détresse que les fibroblastes voisins détectent.
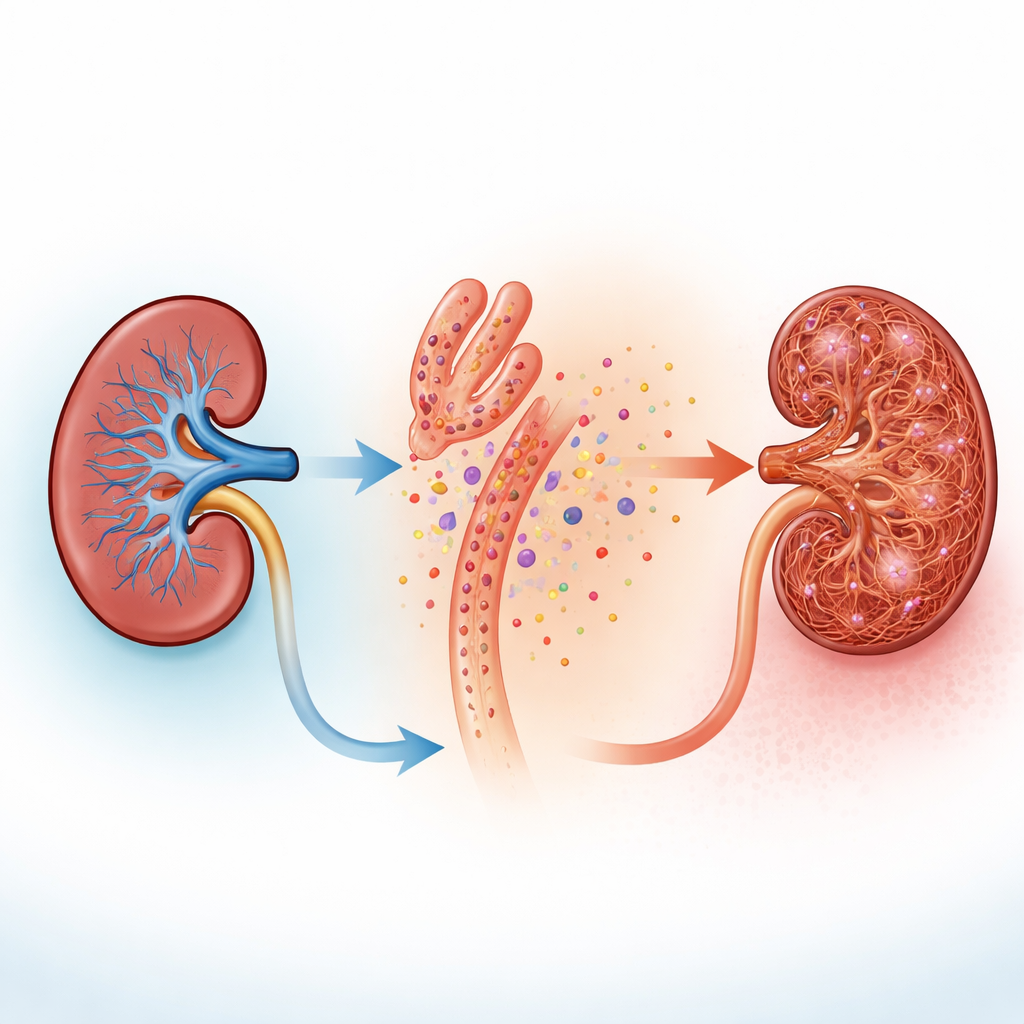
Comment les fibroblastes écoutent avec des éclairs de calcium
Les « oreilles » suspectées des fibroblastes sont les récepteurs P2Y6, des protéines de surface qui répondent à l’UDP. En explorant plusieurs jeux de données unicellulaires, les auteurs ont observé que P2Y6 apparaissait sur les cellules stromales et augmentait encore dans des modèles murins de maladie rénale chronique. Des mesures à l’échelle du rein entier ont confirmé de fortes augmentations des niveaux de P2Y6 dans deux modèles de fibrose différents. Dans des tranches rénales fraîches et dans des fibroblastes rénaux en culture modifiés pour s’illuminer lorsque le calcium intracellulaire augmente, l’ajout d’UDP ou d’un médicament activant P2Y6 a produit des sursauts rapides de calcium. Ces éclairs débutaient dans les longs et fins prolongements qui entourent les tubules puis se propageaient vers le corps cellulaire, et ils disparaissaient lorsque P2Y6 était bloqué ou que le calcium était chimiquement piégé. Chez la souris vivante, la microscopie intravitale à haute résolution a montré que les fibroblastes autour des tubules présentent une activité calcique fréquente et irrégulière qui s’intensifie fortement lorsque les tubules sont lésés, tandis que les cellules tubulaires elles-mêmes s’éteignent.
De signaux brefs à des cicatrices durables
Les explosions de calcium à l’intérieur d’une cellule ne sont pas que des feux d’artifice ; elles peuvent reprogrammer le comportement cellulaire. Lorsque des fibroblastes en culture ont été exposés à un composé activant P2Y6, ils se sont multipliés plus rapidement, ont migré plus facilement, et ont activé des gènes associés à un état plus agressif de « myofibroblaste ». Ces gènes codent des protéines telles que la fibronectine, la vimentine et le collagène qui contribuent directement à la formation de cicatrices. Bloquer P2Y6 ou empêcher les montées de calcium effaçait ces changements, et l’inactivation du gène du récepteur atténuait la réponse. Chez la souris, deux formes distinctes de lésion rénale — l’obstruction de l’uretère et la néphropathie induite par l’acide folique — montraient le même schéma : des reins lésés présentaient davantage de fibroblastes en prolifération, plus de marqueurs de myofibroblastes, plus de collagène et des zones de fibrose plus étendues.
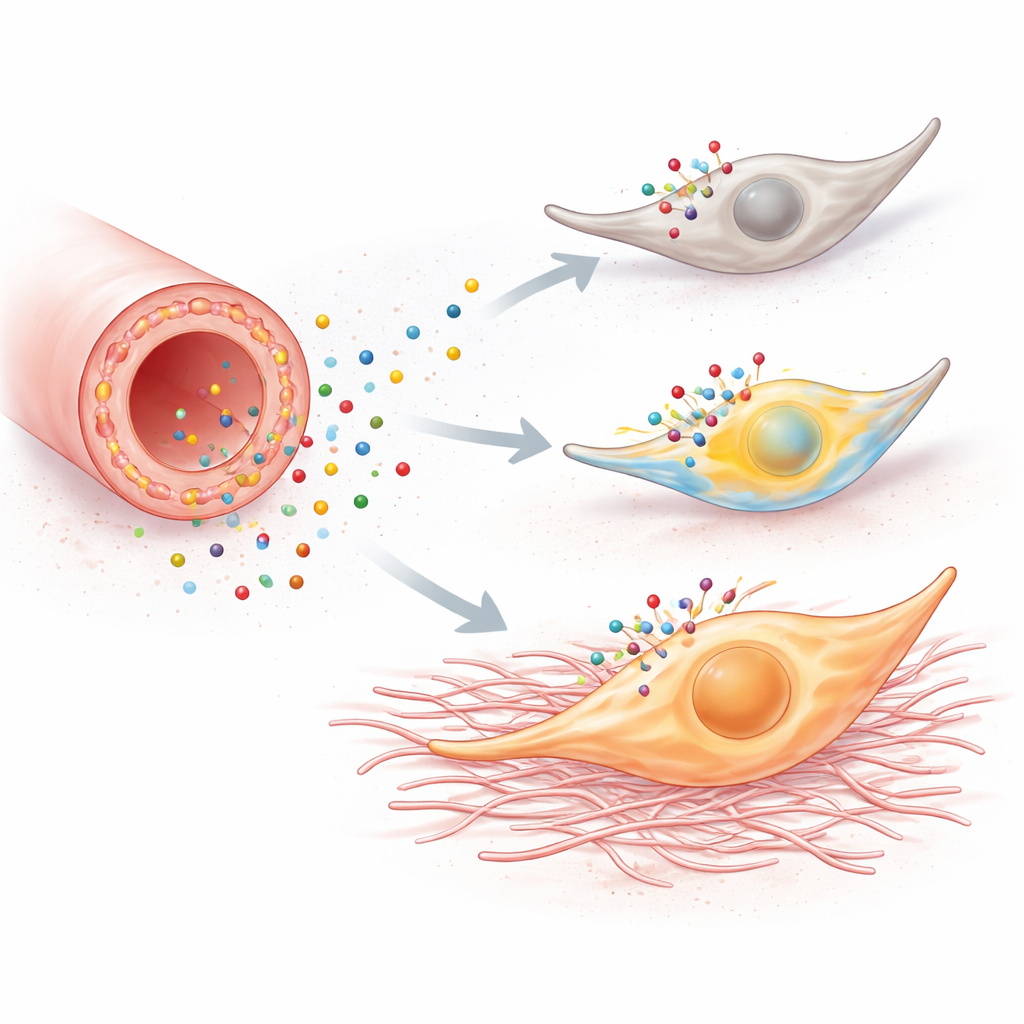
Réduire le volume des signaux nocifs
Pour tester si cette voie est non seulement présente mais réellement dommageable, les chercheurs ont soit supprimé P2Y6 génétiquement, soit l’ont bloqué par un médicament. Les souris dépourvues de ce récepteur ont développé moins de fibrose rénale après l’obstruction urétérale ou la lésion par acide folique : leurs fibroblastes se sont moins multipliés, ont déposé moins de matrice fibreuse et ont recruté moins de cellules inflammatoires. Les analyses sanguines ont montré que ces animaux knock-out conservaient également une meilleure fonction de filtration rénale. Traiter des souris normales avec un composé bloquant P2Y6 a produit une protection comparable, incluant une activité calcique atténuée dans les fibroblastes et une réduction de la cicatrisation, bien que les améliorations des marqueurs sanguins aient été plus variables.
Ce que cela signifie pour les traitements futurs
Dans l’ensemble, ce travail révèle une chaîne d’événements simple mais puissante. Lorsque les cellules tubulaires rénales sont blessées, elles modifient leur chimie interne et libèrent de l’UDP dans le tissu environnant. Les fibroblastes voisins détectent cette molécule via leurs récepteurs P2Y6, répondent par des explosions de calcium intracellulaire, puis basculent en mode cicatrisant — se multipliant, migrant et déposant du collagène. Interrompre cette signalisation calcique basée sur les pyrimidines, en particulier au niveau de P2Y6, atténue fortement la fibrose dans plusieurs modèles murins. Pour les patients, cela suggère une nouvelle cible médicamenteuse : des composés qui bloquent sélectivement P2Y6 dans le rein pourraient aider à rompre le lien entre les lésions rénales fréquentes et la fibrose lente et irréversible qui conduit à la maladie rénale chronique.
Citation: Figurek, A., Jankovic, N., Kollar, S. et al. Pyrimidinergic calcium signaling links tubular metabolism to fibrosis in kidney disease. Nat Commun 17, 3004 (2026). https://doi.org/10.1038/s41467-026-69602-x
Mots-clés: maladie rénale chronique, fibrose rénale, signalisation des fibroblastes, métabolisme des pyrimidines, récepteur P2Y6