Clear Sky Science · fr
Recrutement double de deux molécules CCM2 sur KRIT1 supprime l’expression de KLF4
Pourquoi les vaisseaux sanguins du cerveau exigent un contrôle précis
Les vaisseaux sanguins du cerveau doivent faire preuve d’un grand équilibre : ils doivent être suffisamment robustes pour éviter les fuites, tout en restant assez flexibles pour répondre aux besoins de l’organisme. Quand cet équilibre se rompt, des malformations caverneuses cérébrales peuvent apparaître — des amas de vaisseaux fragiles en forme de bulle qui peuvent saigner et provoquer des crises d’épilepsie ou des AVC. Cette étude révèle une interaction moléculaire jusqu’ici inconnue entre trois protéines qui contribue à la stabilité des vaisseaux cérébraux, et montre comment la rupture de cette interaction peut entraîner la maladie.
Les gardiens de la santé vasculaire
Les cellules qui tapissent les vaisseaux s’appuient sur un ensemble d’interrupteurs maîtres, nommés KLF2 et KLF4, pour contrôler les gènes qui maintiennent la solidité et l’identité vasculaires. Si ces interrupteurs sont trop activés, les vaisseaux deviennent anormaux et vulnérables aux dommages. Deux autres protéines, KRIT1 et CCM2, sont connues pour réguler ce système. Les personnes qui héritent de versions défectueuses de l’une ou l’autre de ces protéines présentent un risque élevé de malformations caverneuses cérébrales. Jusqu’à présent, cependant, les mécanismes précis par lesquels KRIT1 et CCM2 coopèrent pour limiter KLF4 restaient inconnus.
Une équipe surprenante de trois
Les chercheurs ont utilisé des cellules d’aspect endothélial humain cultivées en laboratoire et ont réduit sélectivement la quantité de CCM2 ou de KRIT1 à l’aide d’outils génétiques. Lorsque l’une ou l’autre protéine était diminuée, les niveaux de KLF4 montaient en flèche, reproduisant ce qui est observé chez l’animal et chez les patients. La restauration de niveaux normaux de CCM2 ou de KRIT1 ramenait KLF4 à la normale — mais seulement si les protéines restaurées pouvaient encore interagir entre elles. En introduisant des modifications précises dans les régions où CCM2 et KRIT1 s’interfacent, l’équipe a montré que ce contact physique est essentiel pour empêcher l’augmentation de KLF4. Ces expériences placent sans équivoque le partenariat KRIT1–CCM2 au cœur du système de régulation de ce facteur de transcription puissant.
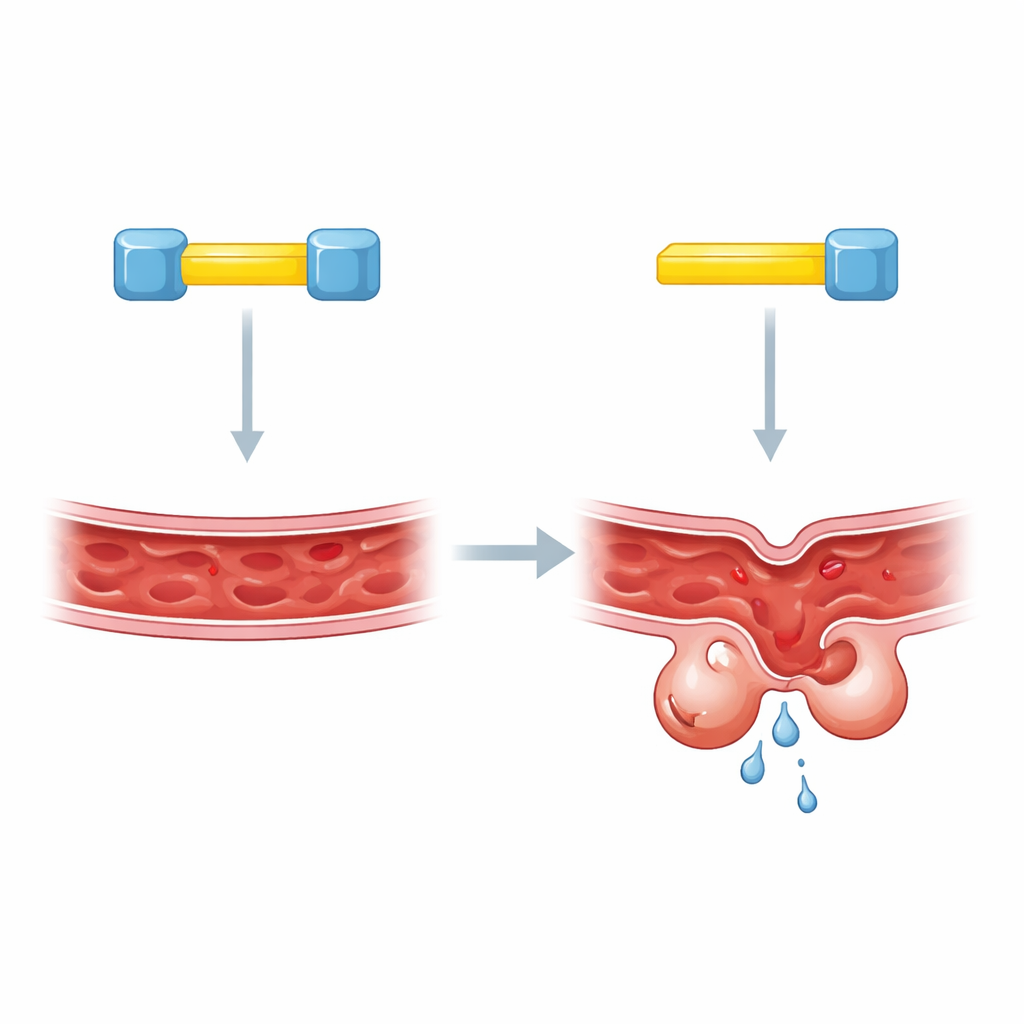
Deux serrures pour une clé
Pour aller plus loin, les auteurs se sont concentrés sur de courts segments au sein de KRIT1 qui servent de sites d’amarrage moléculaires. Des travaux antérieurs suggéraient que CCM2 se lie à KRIT1 à l’un de ces sites, mais des méthodes différentes avaient donné des réponses contradictoires quant à l’emplacement exact. La nouvelle étude montre que la confusion venait du fait que la réalité est plus complexe : KRIT1 porte deux segments d’amarrage voisins, et les deux sont nécessaires. Lorsque l’un ou l’autre segment était perturbé, les niveaux de KLF4 restaient anormalement élevés, comme si KRIT1 manquait complètement. Des tests biochimiques dans des cellules modifiées ont montré qu’une seule protéine KRIT1 peut relier deux molécules distinctes de CCM2 simultanément, suggérant un assemblage inattendu à trois partenaires.
Voir la pince moléculaire en détail
L’équipe a ensuite purifié les fragments pertinents de CCM2 et de KRIT1 et a examiné comment ils s’associent en solution et en cristaux. Les mesures de la masse du complexe ont indiqué que deux copies d’une région clé de CCM2 se lient à une seule bande de KRIT1 portant la paire de sites d’amarrage. Des clichés structuraux à haute résolution ont confirmé cet arrangement 2:1 : un peptide allongé de KRIT1 s’insère entre deux domaines de CCM2, chaque site d’amarrage s’emboîtant dans une poche similaire d’une molécule différente de CCM2. Un court segment hélicoïdal entre les sites d’amarrage aide à positionner les deux domaines de CCM2 côte à côte, créant une structure serrée en forme de pince. Ce type d’engagement double — deux domaines de liaison qui s’attachent à des sites en tandem sur un partenaire — n’avait pas été observé auparavant pour cette famille de modules protéiques.
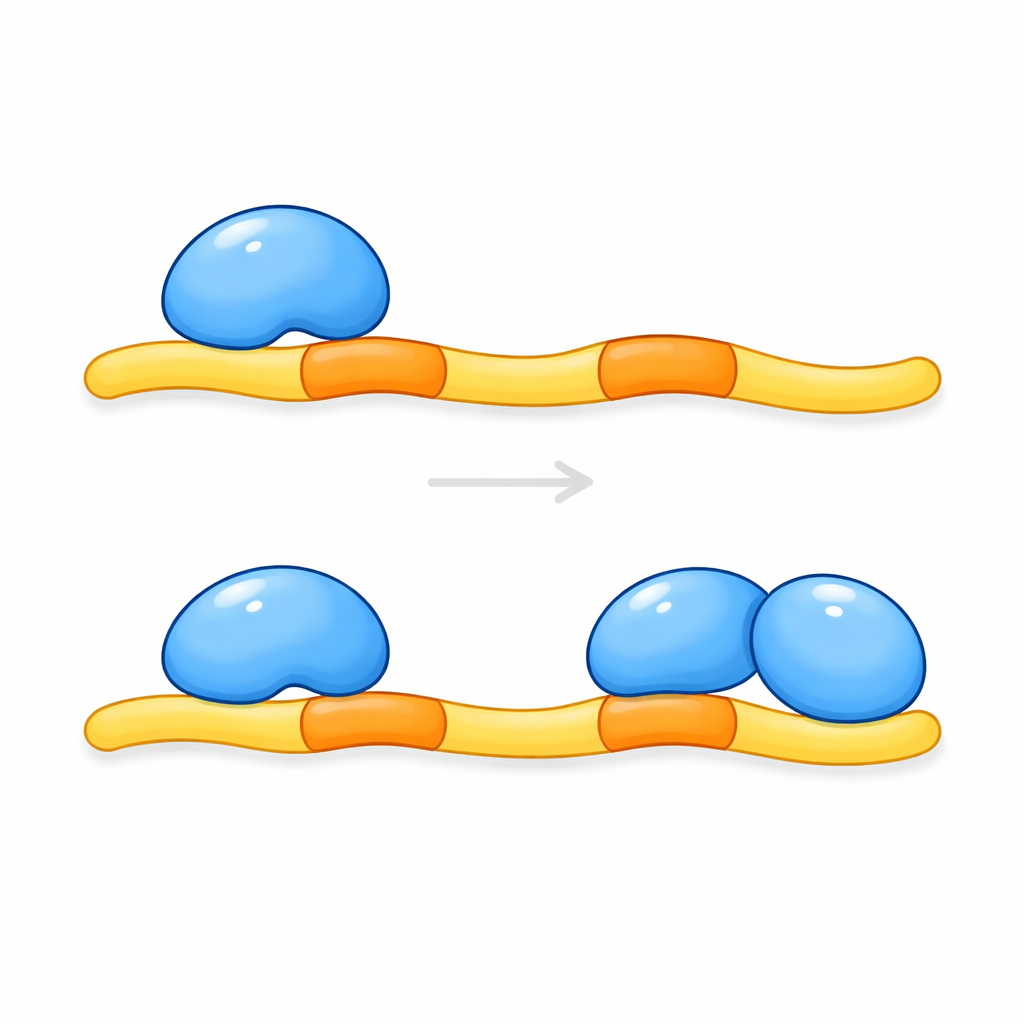
Implications pour les maladies cérébrales et au-delà
Ces résultats montrent que KRIT1 ne se contente pas de lier une seule molécule de CCM2 ; il sert de plateforme qui recrute une paire de protéines CCM2. Ce n’est que lorsque les deux sites d’amarrage sur KRIT1 sont occupés que le complexe peut correctement restreindre la production de KLF4 et, par extension, contribuer à empêcher la croissance de vaisseaux fragiles. Les mutations de KRIT1 qui perturbent l’un ou l’autre site d’amarrage devraient donc affaiblir cette pince protectrice et peuvent expliquer certaines formes héréditaires de malformations caverneuses cérébrales. Étant donné que de nombreuses autres protéines humaines portent des motifs d’amarrage doubles similaires, cette étude suggère également un principe plus général : l’engagement double par des paires de domaines apparentés pourrait être une façon courante pour les cellules d’ajuster finement les réseaux de signalisation. Comprendre cette interaction à trois partenaires pourrait à terme orienter des stratégies pour stabiliser les vaisseaux sanguins chez les personnes à risque d’hémorragie cérébrale.
Citation: Huet-Calderwood, C., Fisher, O.S., Das, S. et al. Dual recruitment of two CCM2 molecules to KRIT1 suppresses KLF4 expression. Nat Commun 17, 2719 (2026). https://doi.org/10.1038/s41467-026-69595-7
Mots-clés: malformations caverneuses cérébrales, cellules endothéliales, KRIT1, CCM2, KLF4