Clear Sky Science · fr
Identification sans produit de contraste de l’état de la barrière hémato‑encéphalique des gliomes via une IA diffusionnelle générative et l’IRM sans contraste
Pourquoi cela compte pour les patients atteints de tumeurs cérébrales
Les personnes atteintes de tumeurs cérébrales passent couramment des IRM, et beaucoup reçoivent également un produit de contraste injecté pour que les médecins puissent déterminer si la barrière protectrice sang‑cerveau a été endommagée. Cette information oriente la chirurgie, la radiothérapie et le pronostic — mais le produit peut comporter des risques, augmenter le temps et le coût et n’est pas toujours disponible. Cette étude présente un système d’intelligence artificielle (IA) qui interprète des IRM de routine sans contraste et recrée virtuellement les images manquantes avec contraste, permettant aux médecins d’inférer l’état de la barrière hémato‑encéphalique sans injection d’agent de contraste.
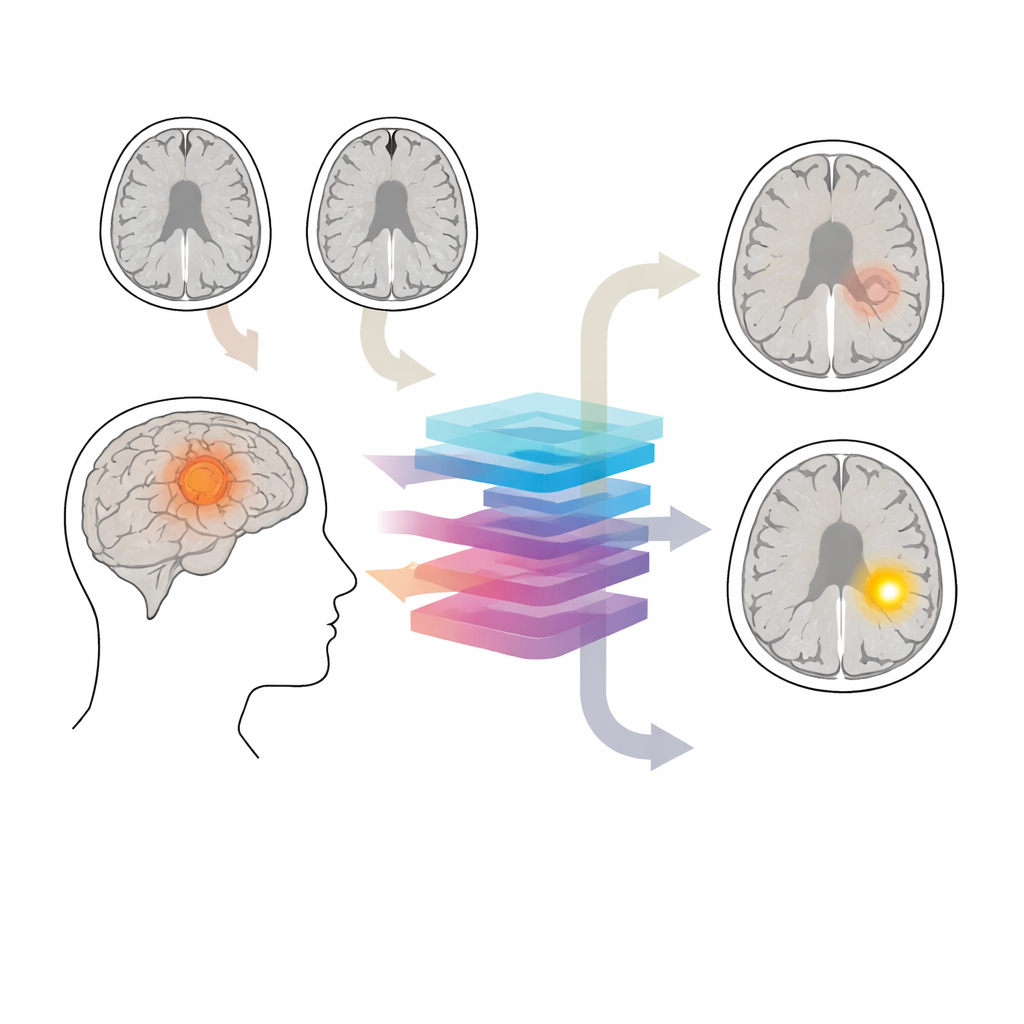
Le gardien protecteur du cerveau
La barrière hémato‑encéphalique agit comme un filtre microscopique autour des vaisseaux cérébraux, ne laissant passer que de très petites molécules. Dans de nombreux gliomes, cette barrière devient perméable. Sur une IRM standard avec contraste, les zones poreuses s’illuminent après injection, tandis que les régions intactes restent sombres. Ces motifs influencent l’intensité du traitement et aident à définir ce qu’il convient d’enlever chirurgicalement ou de cibler par radiothérapie. Pourtant, les examens avec contraste sont parfois évités — par exemple lors d’évaluations initiales ou du suivi à long terme de tumeurs à croissance lente — et certains patients doivent éviter le contraste en raison d’une maladie rénale, d’allergies ou de préoccupations liées au dépôt de gadolinium dans le cerveau.
Transformer des examens ordinaires en contraste virtuel
Les auteurs se sont demandé si les IRM sans contraste, déjà largement réalisées, contenaient suffisamment d’informations subtiles pour que l’IA puisse déduire ce qu’aurait montré une séquence avec contraste. Ils se sont concentrés sur deux séquences courantes : T1 et T2‑FLAIR. Bien que ces séquences ne montrent pas directement les fuites de la barrière hémato‑encéphalique, elles captent la structure de la tumeur, l’œdème environnant et les lésions tissulaires qui accompagnent souvent la rupture de la barrière. L’équipe a construit un système appelé CBSI qui génère d’abord des images synthétiques rehaussées de contraste à partir de ces scans sans contraste, puis les utilise, conjointement avec les images originales, pour décider si la barrière est intacte ou rompue pour chaque gliome.
Comment fonctionne le nouveau système d’IA
Au cœur de CBSI se trouve un modèle de diffusion — un type d’IA qui part d’images bruitées et les « débruite » itérativement pour obtenir des images réalistes. Ici, il apprend à transformer les entrées sans contraste en deux images alternatives de contraste virtuel : l’une supposant une barrière intacte et l’autre une barrière perméable. Un mécanisme de guidage indique au modèle quel schéma de rehaussement viser, et une étape de segmentation auxiliaire l’aide à accorder une attention particulière à la région tumorale. Dans un second stade, un réseau distinct compare les deux résultats synthétiques pour chaque patient et juge lequel est le plus cohérent avec les données IRM d’origine. Cette décision est ensuite traduite en un statut prédit de la barrière hémato‑encéphalique.
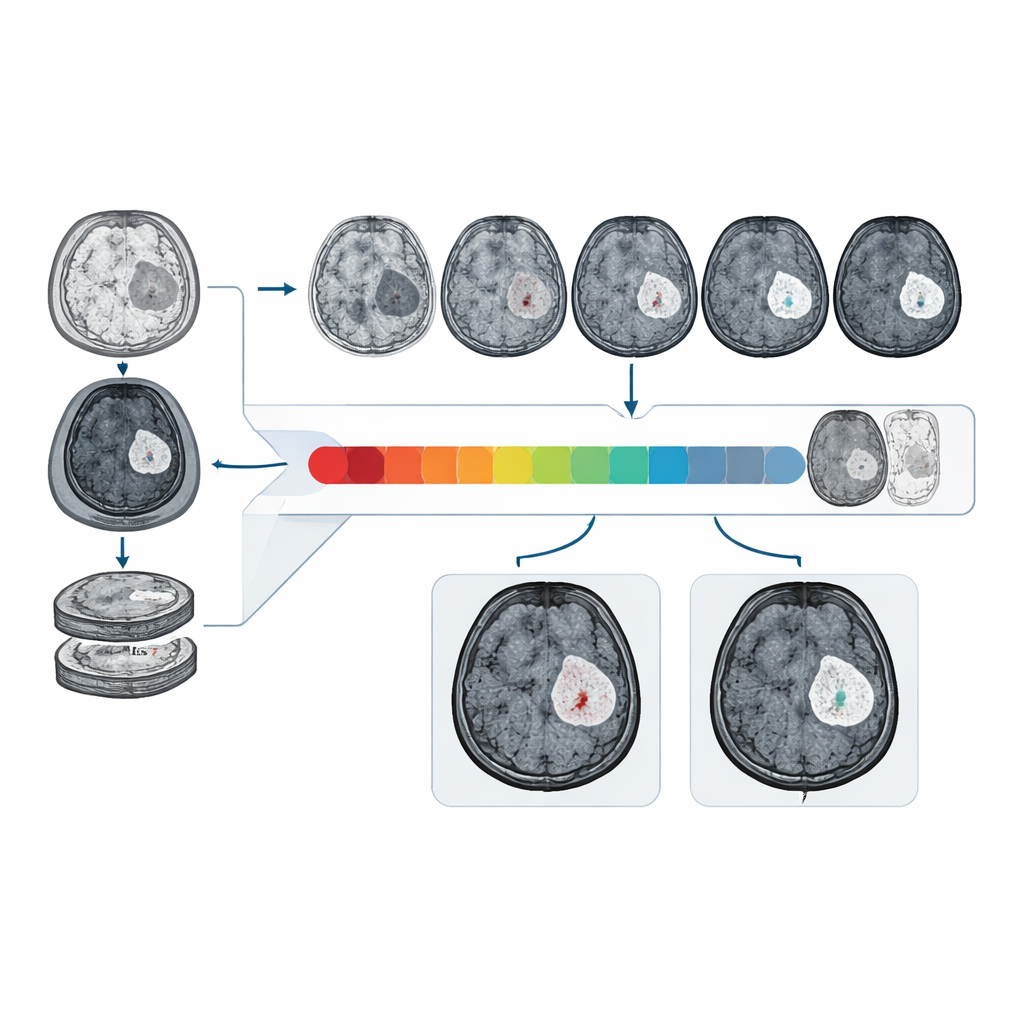
Performances sur des données réelles et diversifiées
Les chercheurs ont entraîné et testé CBSI sur des données IRM de 1 535 patients atteints de gliome, recueillies dans plusieurs hôpitaux et issues de jeux de données publics internationaux. Sur un jeu de test clinique externe, CBSI a distingué barrières intactes et rompues avec une aire sous la courbe d’environ 81 %, nettement supérieure aux modèles se basant uniquement sur les images sans contraste et se rapprochant des performances des modèles disposant des véritables scans avec contraste. Des radiologues, à qui l’on a présenté des mélanges aléatoires d’images réelles et synthétiques produites par le système, ont jugé plus de 90 % des images synthétiques de qualité diagnostique élevée, et leur capacité à identifier le rehaussement de contraste sur les images synthétiques était comparable à leur performance sur des scans réels.
Avantages pour la planification thérapeutique et les soins futurs
Parce que les images de contraste synthétiques produites par CBSI captent les détails tumoraux et les schémas de rehaussement, elles ont également amélioré des tâches en aval comme le délimitation des contours tumoraux et l’estimation du grade tumoral — deux éléments qui dépendent fortement du comportement de la barrière hémato‑encéphalique. La méthode s’est bien généralisée à différents appareils, protocoles d’imagerie et populations de patients, y compris des données d’Afrique subsaharienne et de cohortes internationales plus larges. Si les auteurs reconnaissent qu’un système d’apprentissage profond reste un outil statistique plutôt qu’une fenêtre directe sur la biologie, leurs résultats suggèrent que l’imagerie par contraste virtuel pourrait réduire la dépendance aux agents injectés, notamment pour les patients vulnérables ou dans les contextes où les examens avec contraste sont difficiles à réaliser. Concrètement, cette approche par IA pourrait permettre aux médecins d’extraire des informations clés influençant le traitement sur la barrière hémato‑encéphalique à partir des examens que les patients passent déjà — sans piqûre supplémentaire.
Citation: Zheng, K., Zhang, Y., Shu, H. et al. Contrast-free identification of glioma blood-brain barrier status via generative diffusion AI and non-contrast MRI. Nat Commun 17, 2162 (2026). https://doi.org/10.1038/s41467-026-69578-8
Mots-clés: gliome, barrière hémato‑encéphalique, IRM cérébrale, IA en imagerie médicale, imagerie sans contraste