Clear Sky Science · fr
Des IgG à base de nanocorps inhibent simultanément l’activité allergène et enzymatique de l’allergène dominant du venin d’abeille
Pourquoi les allergies aux piqûres d’abeille comptent
Pour la plupart des personnes, une piqûre d’abeille est douloureuse mais de courte durée. Pour d’autres, elle peut déclencher une réaction potentiellement mortelle touchant tout l’organisme, appelée anaphylaxie. Le principal traitement préventif actuel, l’immunothérapie par venin, fonctionne pour beaucoup de patients mais nécessite des années, implique des injections fréquentes et peut elle‑même provoquer des effets secondaires allergiques. Cette étude explore une nouvelle voie plus ciblée pour protéger les personnes gravement allergiques au venin d’abeille en neutralisant un composant clé du venin avant qu’il ne puisse causer de dommages.
Le principal coupable du venin d’abeille
Le venin d’abeille est un mélange de molécules différentes, mais une protéine, appelée phospholipase A2 (ou Api m 1), se distingue. C’est l’allergène dominant chez les patients allergiques au venin d’abeille et il est présent chez presque tous. Api m 1 joue un double rôle : elle endommage les membranes cellulaires, contribuant à la douleur et à l’inflammation au site de la piqûre, et elle est aussi une cible privilégiée des anticorps responsables d’allergie, les IgE. Quand Api m 1 se lie aux IgE ancrées sur des cellules immunitaires telles que les mastocytes et les basophiles, elle peut déclencher une cascade menant à la libération soudaine de médiateurs inflammatoires et, dans les cas sévères, à l’anaphylaxie.
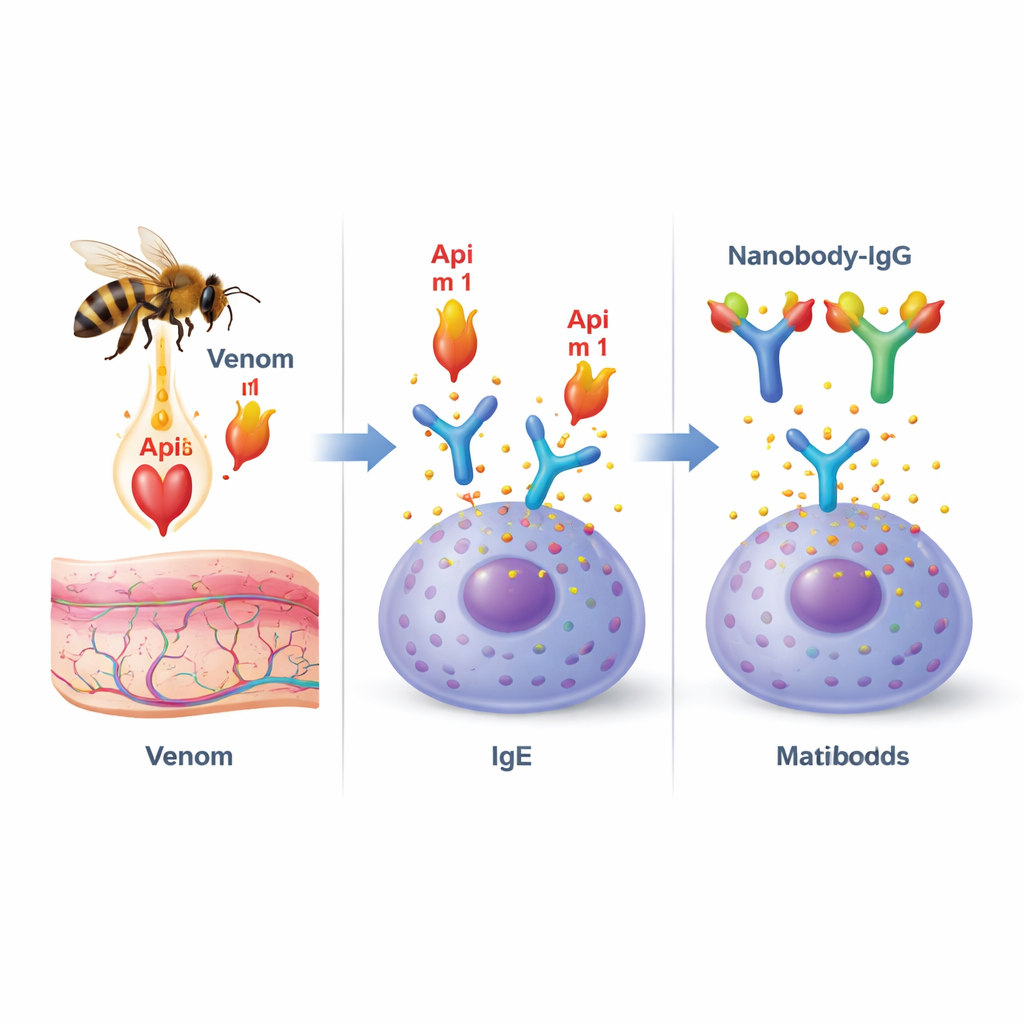
Concevoir de minuscules anticorps pour bloquer l’allergène
Les chercheurs se sont tournés vers les « nanocorps », de petits fragments d’anticorps stables découverts à l’origine chez les camélidés. Du fait de leur petite taille et de leur forme allongée, les nanocorps excellent pour se glisser dans des creux et des poches à la surface des protéines. L’équipe a isolé des nanocorps spécifiques d’Api m 1 à partir d’une bibliothèque immunitaire et a sélectionné deux candidats remarquables, nommés AM1‑1 et AM1‑4. Des travaux structuraux détaillés par cristallographie aux rayons X ont montré que ces deux nanocorps s’accrochent à des faces opposées d’Api m 1 et n’interfèrent pas l’un avec l’autre. L’un d’eux, AM1‑1, se positionne directement au‑dessus du centre actif de l’enzyme, ce qui suggère qu’il pourrait empêcher la fonction destructrice de membranes d’Api m 1, tandis qu’AM1‑4 se loge dans une poche distincte à la surface de la protéine.
Transformer les nanocorps en bloqueurs puissants
Pour transformer ces petits sites de liaison en médicaments de longue durée, les scientifiques ont fusionné chaque nanocorps à la partie effilée (région Fc) de l’IgG1 humaine, créant des molécules plus grandes, semblables à des anticorps, avec une meilleure stabilité dans le sang. Ils ont également conçu une version « bispécifique » portant à la fois AM1‑1 et AM1‑4 dans une seule molécule de type IgG. Des tests en laboratoire ont montré que ces fusions nanocorps‑IgG se lient à Api m 1 avec une affinité extrêmement élevée et qu’elles réduisent fortement, lorsqu’elles sont présentes, la fixation des IgE issues du sang de patients allergiques au venin d’abeille sur Api m 1. Dans des essais cellulaires, elles ont atténué l’activation des basophiles, ces cellules immunitaires qui réagissent habituellement vigoureusement à l’exposition à Api m 1 chez les personnes allergiques.
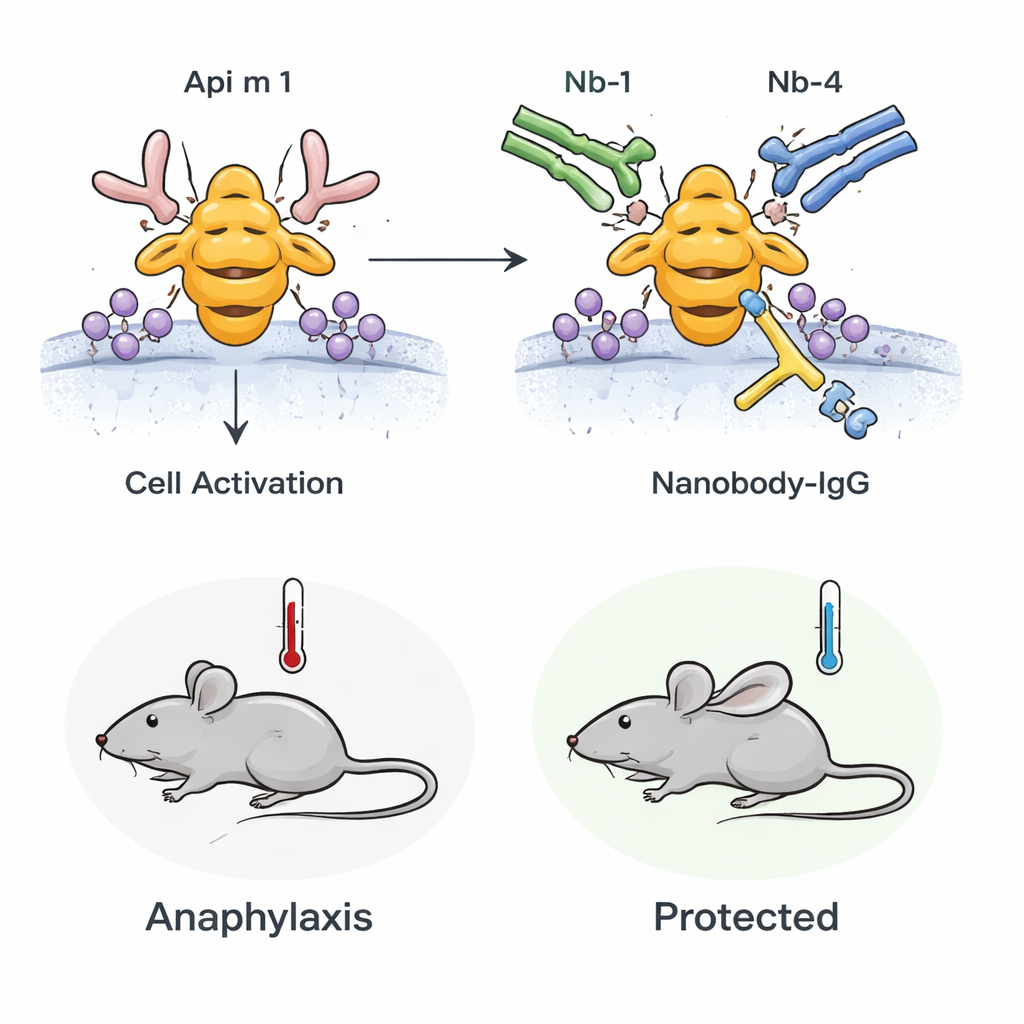
Du tube à essai aux animaux vivants
L’équipe a ensuite vérifié si cet effet bloquant persistait in vivo. Elle a utilisé des souris sensibilisées au venin d’abeille afin que leur système immunitaire réagisse à Api m 1 de façon analogue à l’allergie humaine. Lorsqu’on a exposé ces souris à Api m 1, elles ont développé des signes d’anaphylaxie, notamment une chute de la température corporelle et des marqueurs d’activation des mastocytes dans le sang. Cependant, si les souris avaient été prétraitées avec le nanocorps‑IgG bispécifique, à la fois la chute de température et l’activation des mastocytes ont été significativement réduites. Cela démontre que des anticorps bloquants préexistants et de haute affinité peuvent atténuer la réaction allergique systémique à Api m 1 in vivo.
Quelles implications pour les personnes allergiques au venin d’abeille
Ensemble, les résultats montrent que des molécules d’IgG basées sur des nanocorps et conçues avec soin peuvent bloquer simultanément les actions allergéniques et enzymatiques d’Api m 1, le principal responsable de l’allergie au venin d’abeille. Pour les patients, cela ouvre la possibilité d’une immunisation passive saisonnière : quelques injections de ces anticorps durant les mois où les piqûres d’abeille sont les plus probables pourraient offrir une protection temporaire contre les réactions sévères, sans l’engagement de longue durée et les risques associés à l’immunothérapie conventionnelle par venin. Si des travaux complémentaires sont nécessaires pour étendre l’approche à d’autres composants du venin et pour tester la sécurité et l’efficacité chez l’homme, cette stratégie basée sur les nanocorps propose une manière précise de protéger les personnes vulnérables contre les piqûres d’abeilles dangereuses.
Citation: Aagaard, J.B., Gandini, R., Ballegaard, AS.R. et al. Nanobody-based IgG simultaneously inhibit the allergenic and enzymatic activity of the dominant honeybee venom allergen. Nat Commun 17, 1814 (2026). https://doi.org/10.1038/s41467-026-69572-0
Mots-clés: allergie au venin d’abeille, nanocorps, immunothérapie passive, phospholipase A2, prévention de l’anaphylaxie