Clear Sky Science · fr
Reconnaissance coopérative du promoteur médiée par une pince par l’ARN polymérase poxvirale et son partenaire de type TBP/TFIIB
Comment un virus reconfigure le contrôle des gènes dans nos cellules
Les poxvirus, dont fait partie le virus responsable historiquement de la variole, réalisent toute leur expression génique dans le cytoplasme de nos cellules, loin du centre de contrôle de l’ADN situé dans le noyau. Pour y parvenir, ils apportent leur propre « usine génétique » miniature. Cette étude révèle, à l’échelle atomique, comment l’un de ces virus, le Vaccinia, active une vague spécifique de ses gènes en cours d’infection, en utilisant une protéine en forme de pince inattendue qui travaille de concert avec la machine de copie virale.
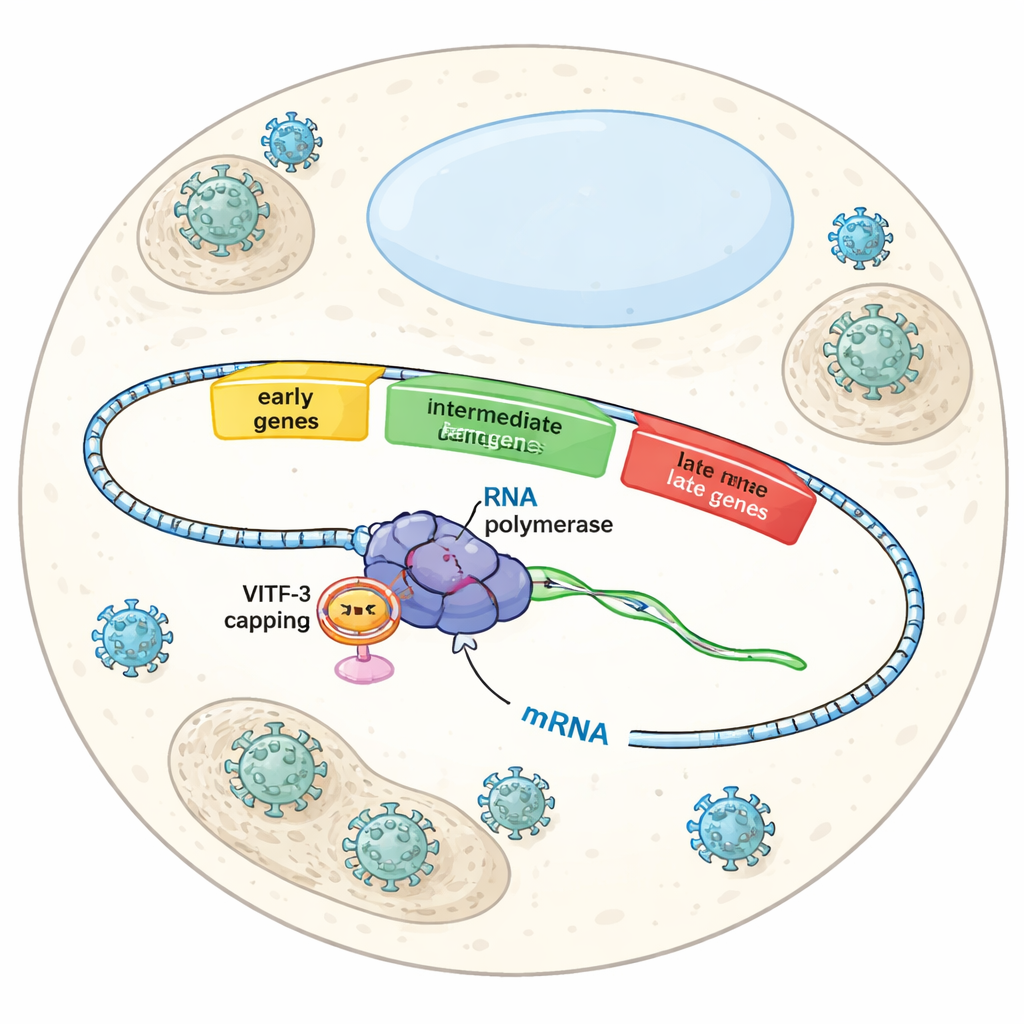
Trois vagues lors de la prise de contrôle virale
Quand le Vaccinia infecte une cellule, il n’active pas tous ses gènes en même temps. Il suit plutôt un script minutieusement chronométré avec des gènes précoces, intermédiaires et tardifs. Les gènes précoces préparent le terrain pour la réplication virale, les gènes intermédiaires contribuent à assembler la machinerie de production des nouvelles particules virales, et les gènes tardifs achèvent l’assemblage et l’emballage. Chaque vague dépend de la même ARN polymérase virale — l’enzyme qui lit l’ADN pour synthétiser l’ARN — mais des facteurs auxiliaires différents indiquent à la polymérase quel groupe de gènes activer à chaque étape. Jusqu’ici, les scientifiques comprenaient assez bien le contrôle des gènes précoces, mais la façon dont le virus reconnaissait et activait spécifiquement les gènes intermédiaires restait un mystère.
Un assistant en anneau qui a besoin d’un partenaire
Les chercheurs se sont concentrés sur une protéine en deux parties appelée VITF‑3, connue pour être nécessaire à l’activation des gènes intermédiaires. De nombreux organismes, y compris l’homme, utilisent une paire de protéines nommées TBP et TFIIB pour guider leur ARN polymérase vers le point de départ sur l’ADN. L’équipe a montré que VITF‑3 est une version fortement modifiée de cette même paire ancienne. Toutefois, contrairement à ses homologues cellulaires, VITF‑3 seule n’adhère pas à l’ADN. Au lieu de cela, ses deux sous‑unités s’emboîtent pour former un anneau fermé qui reste inerte vis‑à‑vis de l’ADN à moins que l’ARN polymérase virale ne soit présente. C’était inattendu, car dans la plupart des systèmes, la composante de type TBP se lie d’abord à l’ADN du promoteur puis recrute la polymérase ; ici, le virus semble avoir reconfiguré l’ordre des événements.
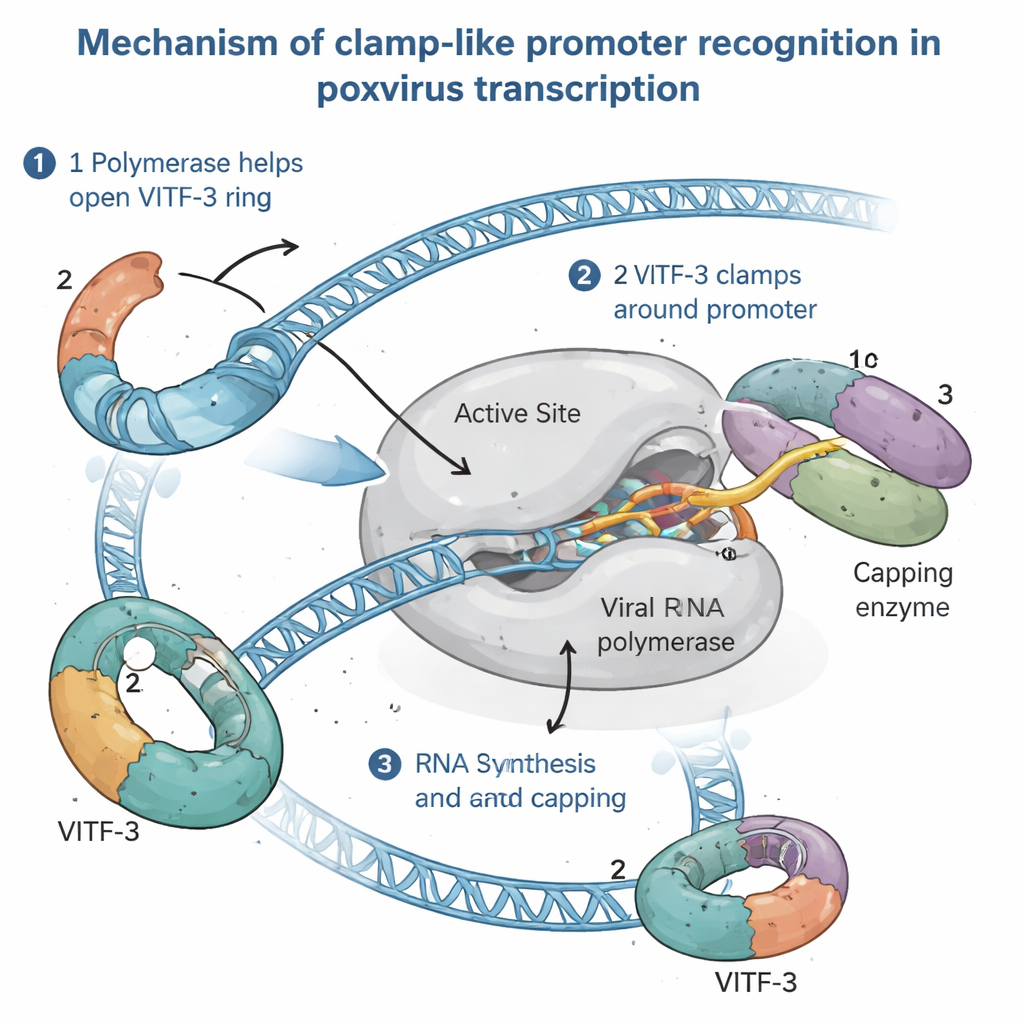
Observer la machine de transcription intermédiaire en action
Pour comprendre le fonctionnement de cet agencement inhabituel, les auteurs ont isolé le complexe d’initiation précoce intermédiaire complet — l’assemblage prêt juste avant le démarrage de la synthèse d’ARN — à partir de cellules humaines infectées. En utilisant la cryo‑microscopie électronique à haute résolution, ils ont visualisé le complexe à environ 2,4 Å de détail, suffisamment précis pour distinguer les chaînes latérales des acides aminés et les bases d’ADN individuelles. Les images ont montré l’ARN polymérase virale saisissant l’ADN du promoteur, avec VITF‑3 formant un anneau serré autour d’une région riche en AT juste en amont du site de démarrage. Cet anneau plie fortement l’ADN d’environ 90 degrés et l’oriente dans une fente de la polymérase. Parallèlement, une enzyme virale de coiffe — responsable de l’ajout de la coiffe protectrice à l’extrémité 5′ des ARN viraux — est arrimée sur la polymérase, prête à modifier les nouveaux transcrits dès leur apparition.
Un mécanisme de « chargeur de pince » emprunté dans l’esprit
En combinant des clichés structuraux et des essais biochimiques, l’étude propose que l’ARN polymérase virale charge activement VITF‑3 sur l’ADN, agissant comme un « chargeur de pince ». D’abord, la polymérase se lie à un promoteur intermédiaire et contribue à ouvrir l’anneau de VITF‑3. Ensuite, conjointement avec l’enzyme de coiffe, elle referme l’anneau autour de la région riche en AT, clampant le complexe en place. L’ADN est localement fondu près du site de démarrage, et la polymérase lit directement un court signal de quatre lettres (un motif TAAA) qui marque précisément l’endroit où la synthèse d’ARN doit débuter. À mesure que l’ARN s’allonge, il suit le même trajet qu’une partie de VITF‑3 dans le complexe initial, si bien que l’ARN naissant pousse probablement VITF‑3 hors du chemin, permettant à la polymérase de quitter le promoteur et de poursuivre le gène tandis que VITF‑3 peut rester en arrière pour faciliter la réutilisation du même promoteur.
Ce que cela signifie pour la compréhension et la lutte contre les poxvirus
En termes simples, ce travail montre que le virus Vaccinia a réorienté un module universel de contrôle génétique en une pince qui n’agrippe l’ADN que quand sa propre ARN polymérase lui en donne l’ordre. Cette astuce ingénieuse permet au virus d’employer une enzyme centrale pour piloter trois programmes de transcription très différents, simplement en échangeant des assistants spécifiques à chaque stade. Parce que ce type de facteurs est conservé chez de nombreux poxvirus, y compris des agents pathogènes humains, le mécanisme de type chargeur de pince désormais révélé et l’anneau unique VITF‑3 offrent des cibles structurales concrètes pour des stratégies antivirales visant à perturber la capacité du virus à synchroniser et contrôler ses gènes pendant l’infection.
Citation: Jungwirth, S., Bartuli, J., Lamer, S. et al. Cooperative clamp-mediated promoter recognition by poxviral RNA polymerase and its TBP/TFIIB-like partner. Nat Commun 17, 1648 (2026). https://doi.org/10.1038/s41467-026-69571-1
Mots-clés: transcription des poxvirus, virus Vaccinia, ARN polymérase, reconnaissance du promoteur, facteurs de transcription