Clear Sky Science · fr
La reprogrammation de la sérine médiée par la phosphoglycérate déshydrogénase aggrave l’hyperinflammation macrophagique dans une pneumonie à Pseudomonas aeruginosa chez la souris
Quand les défenseurs du corps vont trop loin
La pneumonie causée par la bactérie Pseudomonas aeruginosa est réputée difficile à traiter, surtout chez les personnes ayant des poumons fragilisés. Les antibiotiques ciblent le microbe, mais cette maladie est souvent mortelle non seulement à cause des bactéries, mais parce que la réponse immunitaire de l’hôte peut se déchaîner. Cette étude révèle comment un unique « interrupteur » métabolique au sein des cellules immunitaires peut les faire passer d’utiles à nuisibles — et suggère que modifier l’alimentation ou le métabolisme cellulaire pourrait apaiser une inflammation pulmonaire mortelle.
Une danse dangereuse entre germe et système immunitaire
Pseudomonas aeruginosa est une bactérie Gram négatif courante qui peut envahir les voies aériennes inférieures et déclencher une pneumonie sévère. Normalement, des cellules immunitaires résidentes du poumon appelées macrophages patrouillent dans les alvéoles, engloutissent les envahisseurs et lancent l’alerte par des signaux chimiques. Mais quand la charge bactérienne est élevée, ces cellules recrutent de nombreux macrophages supplémentaires depuis le sang. Le résultat peut être une tempête de molécules inflammatoires qui endommage le tissu pulmonaire fragile, compromet les processus de réparation et, dans les cas graves, entraîne une insuffisance respiratoire et la mort. Les auteurs se sont demandé si le métabolisme interne de ces macrophages pouvait être à l’origine de cette réaction excessive néfaste.
Une enzyme métabolique dans le viseur
L’équipe s’est concentrée sur une enzyme appelée phosphoglycérate déshydrogénase (PHGDH), un point d’entrée clé dans la voie que les cellules utilisent pour fabriquer l’acide aminé sérine à partir du glucose. Dans des modèles murins d’infection pulmonaire à Pseudomonas, les niveaux et l’activité de PHGDH augmentaient fortement dans les poumons, en particulier dans les macrophages. Lorsque les souris étaient traitées par un inhibiteur de PHGDH de petite molécule, ou lorsque le gène codant PHGDH était supprimé spécifiquement dans les cellules myéloïdes (qui incluent les macrophages), les animaux s’en sortaient mieux : ils survivaient plus longtemps, présentaient moins de lésions pulmonaires, portaient moins de bactéries et produisaient des quantités moindres de cytokines inflammatoires puissantes telles que l’interleukine‑6 et l’interleukine‑1β. Au niveau cellulaire, le blocage de PHGDH éloignait les macrophages d’un état fortement pro‑inflammatoire sans favoriser l’autre phénotype opposé de réparation.
Alimenter le feu : la sérine et un circuit de signalisation hyperactif
En creusant plus avant, les chercheurs ont montré que l’infection reprogramme les macrophages pour canaliser davantage de glucose vers la production de nouvelle sérine, et que cette sérine aggrave l’inflammation. Un apport supplémentaire en sérine amenait les macrophages à sécréter plus de cytokines inflammatoires et à exprimer davantage de marqueurs d’activation à leur surface, tandis que des régimes restreints en sérine protégeaient les souris infectées et réduisaient la charge bactérienne. Sur le plan mécanistique, la sérine alimentait un cycle métabolique « à un carbone » qui contribue à fournir des groupes méthyle, des étiquettes chimiques utilisées dans la régulation épigénétique. Cela augmentait une marque histone spécifique, la triméthylation de H3K27, à proximité du gène d’une protéine frein appelée DUSP4, qui aide normalement à éteindre la voie de signalisation ERK1/2. Lorsque DUSP4 était supprimée, ERK1/2 restait activée, amplifiant les signaux inflammatoires. Inhiber PHGDH ou réduire la sérine inversait cette chaîne, rétablissait DUSP4 et diminuait la phosphorylation d’ERK1/2.
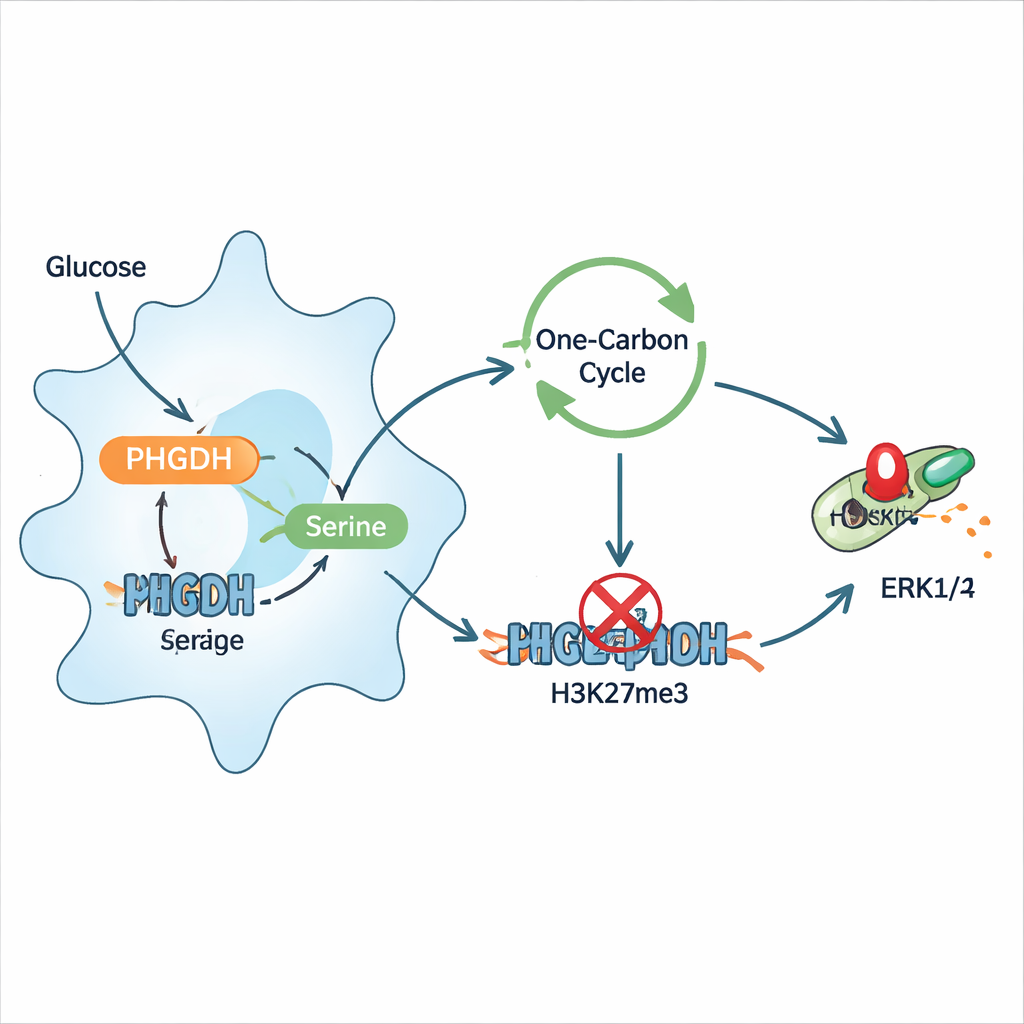
Rééquilibrer les macrophages sans affaiblir la défense
Il est important de noter que réduire PHGDH n’a pas simplement paralysé le système immunitaire. En fait, les macrophages dépourvus de PHGDH étaient meilleurs pour engloutir et tuer Pseudomonas tôt après l’infection, tout en produisant moins de cytokines dommageables. Transférer ces macrophages déficients en PHGDH dans des souris normales améliorait les résultats après le défi bactérien, soulignant que les bénéfices provenaient de la reprogrammation de la réponse de l’hôte plutôt que d’un effet direct sur le microbe. Le travail suggère aussi que des régimes riches en sérine pourraient involontairement favoriser l’hyperinflammation lors de pneumonies bactériennes sévères, tandis qu’une restriction contrôlée en sérine pourrait offrir une nouvelle façon de contenir les dommages pulmonaires excessifs.
Ce que cela signifie pour le traitement des pneumonies difficiles à soigner
De façon accessible, cette étude montre que certains macrophages dans la pneumonie à Pseudomonas métabolisent le sucre de manière à produire de la sérine supplémentaire, et que ce détour métabolique bloque leur machinerie inflammatoire en surrégime. En bloquant l’enzyme PHGDH ou en limitant la sérine, les chercheurs ont pu calmer cette réaction excessive, protéger le tissu pulmonaire et permettre malgré tout aux cellules immunitaires d’éliminer les bactéries. Bien que le travail ait été réalisé chez la souris et soit loin d’un usage clinique, il met en lumière une idée prometteuse : associer les antibiotiques traditionnels à des médicaments ou à des approches alimentaires qui ajustent subtilement le métabolisme des cellules immunitaires pourrait transformer un feu immunitaire destructeur en une flamme contrôlée qui combat les bactéries.
Citation: Chen, R., Zeng, R., Shi, M. et al. Phosphoglycerate dehydrogenase-mediated serine reprogramming aggravates macrophage hyperinflammation in murine Pseudomonas aeruginosa pneumonia. Nat Commun 17, 1944 (2026). https://doi.org/10.1038/s41467-026-69539-1
Mots-clés: Pneumonie à Pseudomonas, métabolisme des macrophages, biosynthèse de la sérine, inflammation pulmonaire, PHGDH