Clear Sky Science · fr
Ustilago maydis perturbe les réseaux de signalisation des glucides pour induire l’hypertrophie des cellules hôtes
Quand les maladies des cultures transforment les cellules en « tumeurs »
Le maïs est l’une des cultures alimentaires et fourragères les plus importantes au monde, et il a un ennemi inhabituel : le champignon de la carie Ustilago maydis, qui provoque des excroissances enflées, semblables à des tumeurs, sur les feuilles et les épis. Au‑delà de l’aspect frappant, ces croissances détournent discrètement les sucres de la plante loin de la croissance et de la défense normales pour en faire profiter le champignon. Cette étude révèle comment une seule protéine fongique aide à inverser les commutateurs énergétiques internes de la plante, transformant des cellules foliaires ordinaires en usines gonflées, remplies d’amidon, qui nourrissent le pathogène.
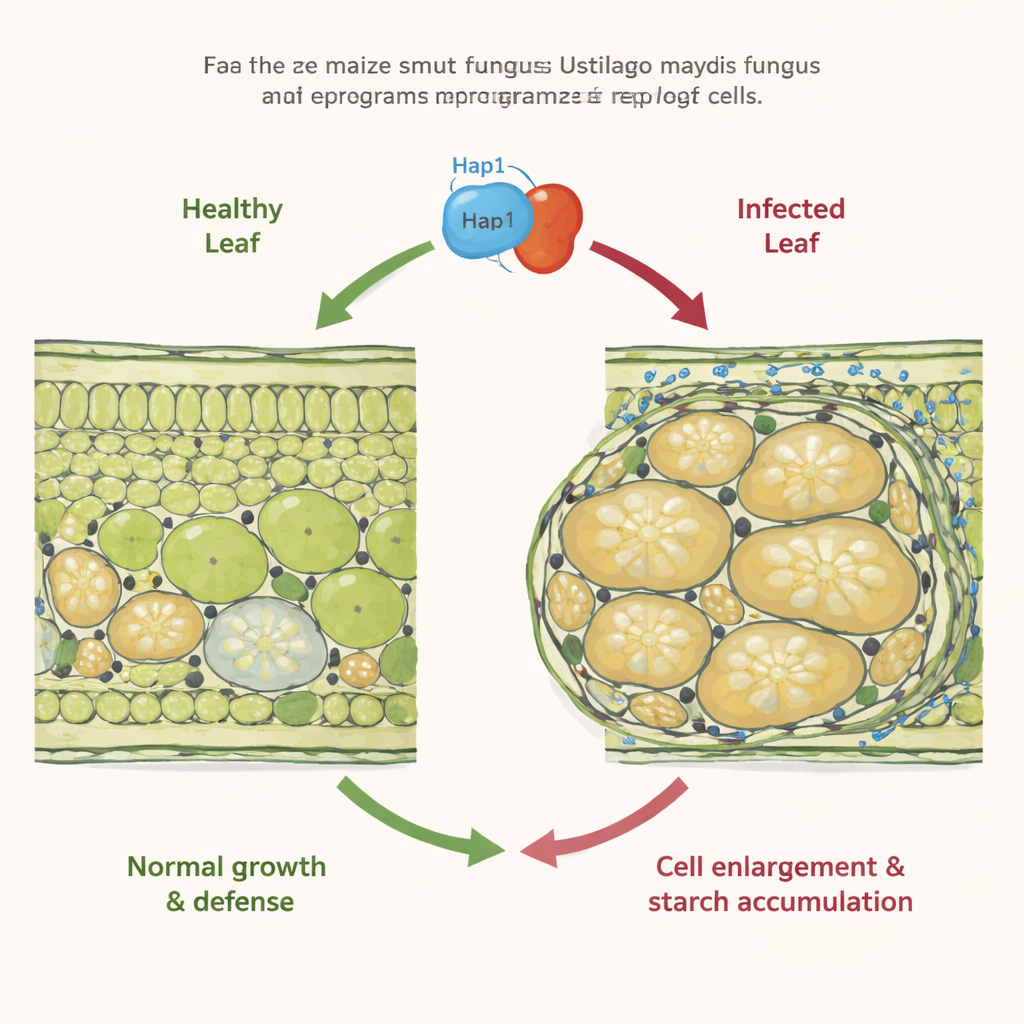
Un champignon qui reprogramme la croissance des plantes
La plupart des champignons de la carie se répandent discrètement dans les céréales et déforment principalement les fleurs. Ustilago maydis est différent : il peut former des tumeurs localisées sur presque toutes les parties aériennes du maïs. Des travaux antérieurs ont montré que, dans les feuilles infectées, certaines cellules commencent à trop se diviser (hyperplasie), tandis que les cellules de mésophylle voisines, qui assurent normalement la photosynthèse, gonflent de façon spectaculaire (hypertrophie) et cessent de se diviser. Ces cellules hypertrophiées se remplissent également de granules d’amidon là où les plantes en C4 comme le maïs n’en stockent généralement pas. Les déclencheurs moléculaires derrière cette extrême augmentation cellulaire et cette accumulation de sucres restaient cependant inconnus.
Identifier le déclencheur fongique du gonflement cellulaire
Les chercheurs se sont concentrés sur les protéines « effectrices » fongiques : des molécules sécrétées dans les tissus de la plante qui reconfigurent la biologie de l’hôte. À partir d’une liste d’effecteurs actifs spécifiquement dans les cellules tumorales hypertrophiées, ils ont utilisé CRISPR‑Cas9 pour supprimer plusieurs gènes candidats d’U. maydis. Un gène, UMAG_02473, s’est distingué : les mutants qui en étaient dépourvus provoquaient beaucoup moins de tumeurs et montraient des cellules végétales avec des noyaux plus petits et beaucoup moins d’amidon dans le mésophylle foliaire. Comme des noyaux agrandis sont une marque d’endoréplication — des cellules qui copient leur ADN sans se diviser — l’équipe en a conclu que cet effecteur, qu’ils ont nommé Hap1 (protéine associée à l’hypertrophie 1), est crucial pour pousser les cellules de mésophylle dans un programme de croissance sans division et pour stimuler l’accumulation d’amidon.
Détourner le thermostat énergétique de la plante
Pour comprendre comment Hap1 reconfigure le métabolisme du maïs, les scientifiques ont cherché ses cibles végétales. Ils ont montré que Hap1 est délivré dans les cellules hôtes et s’accumule à la fois dans le cytoplasme et dans le noyau. À l’aide de pull‑downs protéiques et de spectrométrie de masse, ils ont trouvé que Hap1 se lie à la protéine du maïs SnRK1, un senseur énergétique central qui répond normalement au stress et au faible niveau d’énergie en activant les voies libératrices de sucres, en freinant les synthèses coûteuses en énergie (comme la formation d’amidon) et en renforçant les réponses de défense. Des tests complémentaires ont confirmé que Hap1 interagit physiquement avec les sous‑unités catalytiques de SnRK1. En présence de Hap1, les schémas de phosphorylation des composants de SnRK1 et des protéines cibles connues de SnRK1 ont changé, et un essai direct de kinase a montré que Hap1 atténue la capacité de SnRK1 à phosphoryler un substrat témoin standard. En somme, Hap1 interfère avec le « thermostat » énergétique de la plante, affaiblissant sa réponse habituelle au stress et au manque de nutriments.
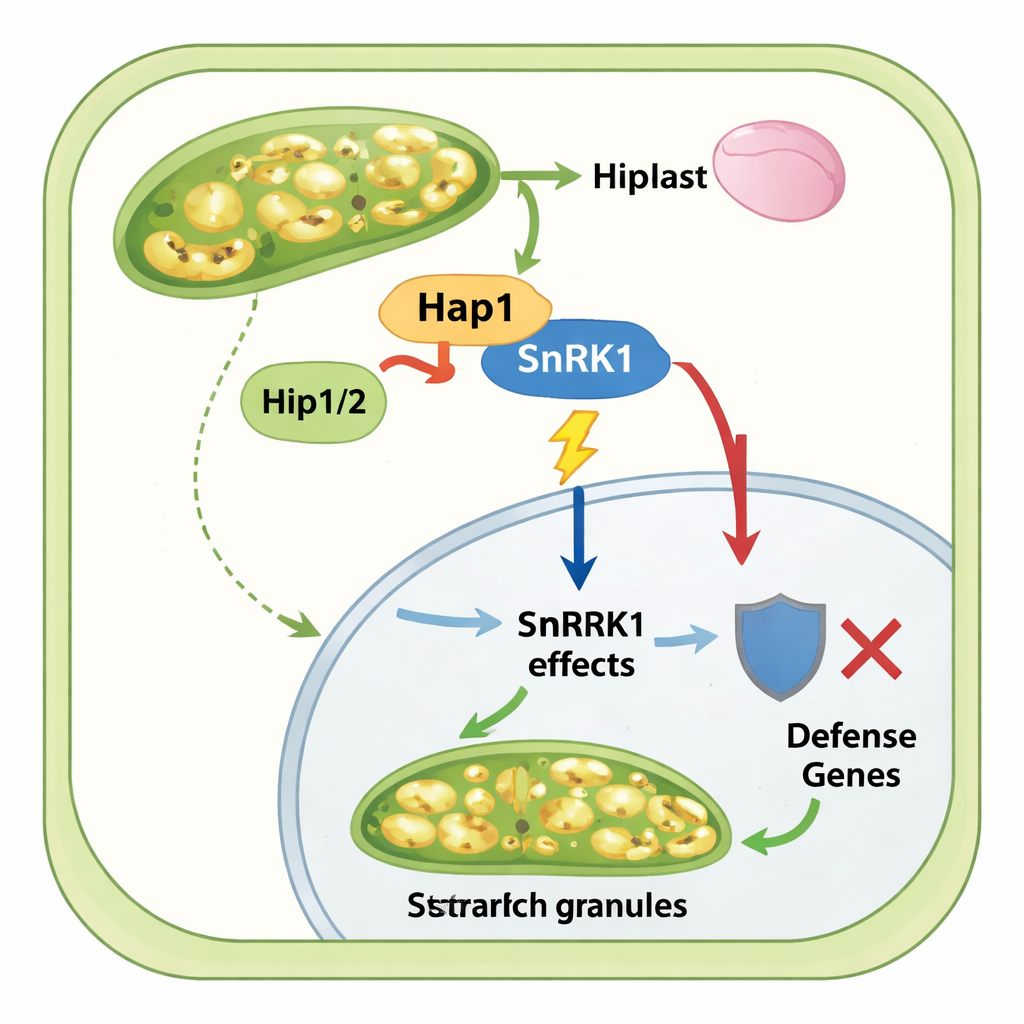
Effecteurs auxiliaires et niche tumorale riche en sucres
L’histoire ne s’arrête pas à Hap1 seul. L’équipe a découvert deux effecteurs fongiques supplémentaires, Hip1 et Hip2, qui interagissent spécifiquement avec Hap1 et sont également exprimés dans les cellules tumorales hypertrophiées. Bien que la suppression de ces aides ait un impact limité sur la sévérité globale de la maladie, des expériences biochimiques ont montré que Hip1 et Hip2 se lient à la fois à Hap1 et au complexe SnRK1, contribuent à maintenir les niveaux de protéine Hap1, et sont nécessaires pour que Hap1 puisse efficacement récupérer SnRK1 à partir de tissus de maïs infectés. La phosphoprotéomique et les données d’expression génique montrent ensemble que, en présence de Hap1, les tumeurs de maïs surexpriment les gènes et enzymes de biosynthèse de l’amidon, tandis que les gènes liés à la défense de la plante et à la machinerie normale de production protéique sont atténués. En l’absence de Hap1, l’accumulation d’amidon dans les cellules du mésophylle chute fortement et les voies de signalisation liées au stress et à la défense deviennent plus actives.
Implications pour le maïs et ses défenses
Pour un lecteur non spécialiste, ce travail montre qu’Ustilago maydis réussit non seulement en endommageant les tissus, mais en manipulant habilement les commandes énergétiques internes de la plante. L’effecteur Hap1, renforcé par ses partenaires Hip1 et Hip2, semble mettre « en sourdine » SnRK1, un gardien clé qui conserve habituellement l’énergie et soutient les défenses immunitaires. Avec cette protection affaiblie, les cellules de mésophylle du maïs cessent de fonctionner comme de normales usines vertes et, au contraire, gonflent, répliquent leur ADN sans se diviser et accumulent de l’amidon. Ces cellules de type tumoral deviennent des îlots riches en nutriments qui nourrissent le champignon. Comprendre cette stratégie fongique ouvre la voie à la sélection ou à l’ingénierie de variétés de maïs dans lesquelles SnRK1 ou les voies associées sont moins vulnérables, aidant ainsi les cultures à résister aux infections formatrices de tumeurs sans sacrifier la croissance.
Citation: Lee, Y.J., Zhang, D., Stolze, S.C. et al. Ustilago maydis disrupts carbohydrate signaling networks to induce hypertrophy in host cells. Nat Commun 17, 1990 (2026). https://doi.org/10.1038/s41467-026-69532-8
Mots-clés: carie du maïs, immunité des plantes, effecteurs fongiques, métabolisme de l’amidon, signalisation SnRK1