Clear Sky Science · fr
Une cellule synthétique intégrant la réplication autonome de l’ADN et la biosynthèse des lipides
Construire la vie à partir de zéro
Qu’est-ce qui distingue une cellule vivante d’un simple sac de molécules ? Une réponse tient à sa capacité à copier ses instructions génétiques et à fabriquer sa propre membrane protectrice. Cette étude franchit une étape importante vers la reproduction de cette aptitude en laboratoire. Les auteurs conçoivent de petites bulles de graisse, appelées liposomes, capables de lire un fragment d’ADN, de copier cet ADN et de produire de nouveaux composants membranaires — le tout à l’intérieur d’un même compartiment miniature. Leur travail nous rapproche d’un pas des cellules artificielles susceptibles de croître, de s’adapter et, peut‑être un jour, d’évoluer de façon autonome.
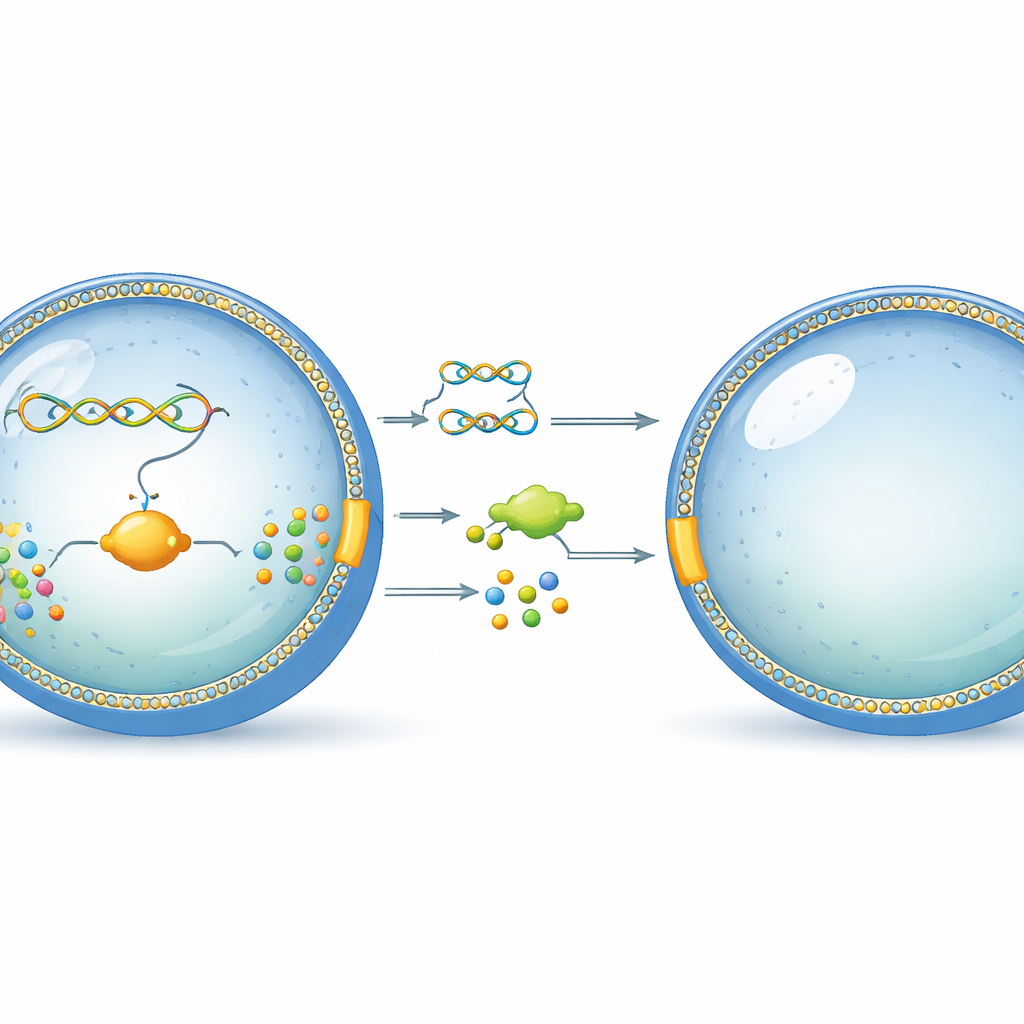
Une minuscule bulle qui agit comme une cellule
Les chercheurs partent de bulles simples, de la taille d’une cellule, constituées de phospholipides, le même type de molécules qui forment l’enveloppe externe des cellules réelles. Dans ces bulles, ils introduisent un brin d’ADN soigneusement conçu et un ensemble de machines cellulaires purifiées capables de lire l’ADN et de fabriquer des protéines. Ce dispositif, appelé système d’expression sans cellule, joue le rôle du noyau réduit d’une cellule vivante : il transforme l’information génétique en molécules fonctionnelles sans nécessiter d’organisme vivant. L’idée centrale est de placer l’ensemble à l’intérieur du liposome afin que le programme génétique et ses produits restent réunis, à l’instar d’une cellule naturelle.
Un programme d’ADN sur mesure avec deux fonctions
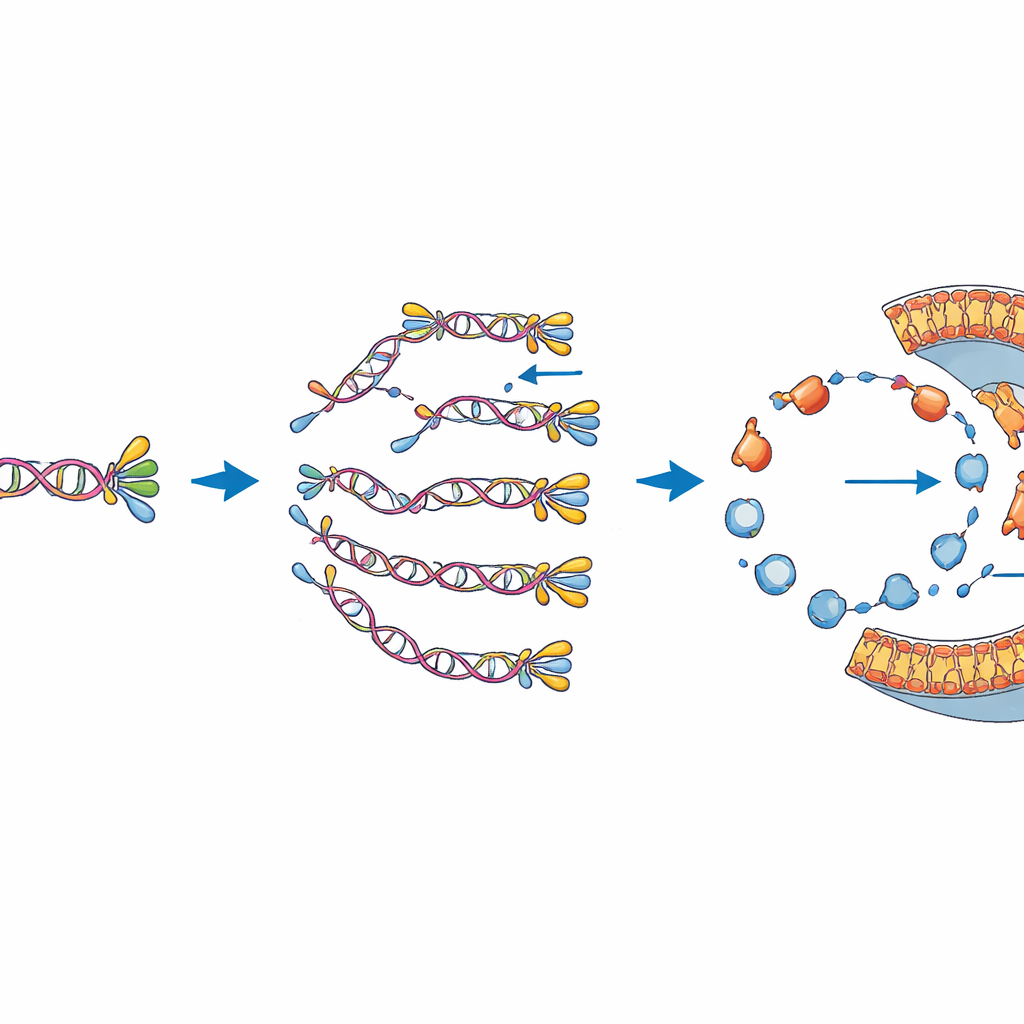
Au cœur de leur cellule synthétique se trouve une molécule d’ADN construite sur mesure que les auteurs nomment DNArep-PLsyn. Cet ADN porte les instructions pour six protéines. Deux d’entre elles proviennent d’un virus infectant les bactéries et, ensemble, sont capables de copier l’ADN lui‑même, fournissant un module d’auto‑réplication intégré. Les quatre autres proviennent de la bactérie intestinale E. coli et forment une chaîne de réactions qui transforme des précurseurs simples en un phospholipide spécifique utilisé dans les membranes. Pour assembler ce génome inhabituel, l’équipe a dû recoller des fragments d’ADN en éprouvette et dans des cellules de levure, puis convertir le résultat en un brin d’ADN linéaire que la machinerie virale de copie peut reconnaître et répliquer.
Produire et tester l’activité synthétique
Une fois l’ADN et la machinerie de production de protéines scellés à l’intérieur des liposomes, les bulles sont chauffées à différentes températures et laissées fonctionner. L’équipe vérifie ensuite le résultat à l’aide de marqueurs fluorescents : un colorant s’allume lorsqu’il se lie à l’ADN, révélant la quantité d’ADN présente, et un autre se fixe au nouveau phospholipide s’il est produit et inséré dans la membrane. Grâce à la cytométrie en flux et à la microscopie à haute résolution, ils peuvent analyser des dizaines de milliers de vésicules individuelles. Ils constatent que de nombreuses bulles copient avec succès le génome, que d’autres fabriquent de nouveaux éléments de membrane, et qu’une fraction plus petite mais significative réalise les deux activités simultanément. Des tests complémentaires par quantification de l’ADN et spectrométrie de masse confirment que le génome en longueur complète est amplifié et que de nouvelles molécules de phospholipides sont effectivement synthétisées, bien que dans des quantités modestes.
Équilibrer deux tâches essentielles
Les auteurs examinent ensuite comment ces deux fonctions s’influencent mutuellement. En activant ou en désactivant la chimie de copie de l’ADN ou de synthèse membranaire via les ingrédients requis, ils montrent que chaque processus peut fonctionner en grande partie sans perturber l’autre. Cependant, lorsque les deux modules sont codés sur le même ADN, le volet synthèse membranaire s’avère plus fragile : moins de vésicules présentent cette activité comparé aux vésicules portant uniquement les gènes liés aux lipides. De même, le génome combiné ne se copie pas aussi efficacement qu’une version plus petite contenant seulement les gènes de réplication de l’ADN. Cela suggère que, même dans ce système simplifié, il existe une compétition pour des ressources partagées et pour l’espace physique sur l’ADN, faisant écho aux compromis observés dans les cellules réelles.
Se préparer à l’évolution en éprouvette
Pour dépasser une démonstration ponctuelle, l’équipe conçoit son système de manière à pouvoir, en principe, être amélioré par évolution. Ils génèrent des versions d’ADN plus propres et plus fiables en utilisant des plasmides cultivés dans la levure et des bactéries, ce qui augmente la fraction de cellules synthétiques pleinement fonctionnelles. Ils montrent également qu’il est possible d’encapsuler, de sélectionner et de récupérer des génomes à partir de vésicules qui réalisent à la fois la copie de l’ADN et la synthèse membranaire. Cela prépare le terrain pour de futurs cycles au cours desquels des génomes légèrement différents entrent en compétition, et ceux qui performent le mieux sont enrichis et copiés.
Pourquoi cela compte pour la compréhension de la vie
En termes simples, les chercheurs ont construit une bulle microscopique capable de lire sa propre recette, d’en produire davantage et de s’en servir pour réparer et étendre son enveloppe externe. Bien que ces cellules synthétiques ne puissent pas encore croître considérablement ni se diviser comme des organismes vivants, le travail démontre que des caractéristiques fondamentales de la vie — stockage de l’information, auto‑copie et auto‑construction élémentaire — peuvent être combinées dans un système simple et contrôlable. Cela crée une base importante pour explorer comment la vie aurait pu émerger à partir de la chimie inanimée et pour concevoir des cellules artificielles réalisant des tâches utiles, de la délivrance ciblée de médicaments à de minuscules usines auto‑renouvelables.
Citation: Restrepo Sierra, A.M., Ramirez Gomez, F., van Tongeren, M. et al. A synthetic cell with integrated DNA self-replication and lipid biosynthesis. Nat Commun 17, 2727 (2026). https://doi.org/10.1038/s41467-026-69531-9
Mots-clés: cellules synthétiques, auto-réplication de l’ADN, biosynthèse des lipides, vie artificielle, biologie ascendante