Clear Sky Science · fr
Thérapie thermique interstitielle au laser et pembrolizumab adjuvant dans les astrocytomes de haut grade récurrents : essai de phase 1 / phase 2b randomisé
Pourquoi cette étude sur le cancer du cerveau est importante
L’astrocytome de haut grade récurrent, y compris le glioblastome, est l’un des cancers cérébraux les plus mortels, et les traitements actuels le contrôlent rarement longtemps. Cette étude teste une stratégie en deux étapes qui utilise la chaleur d’un laser pour détruire le tissu tumoral et ouvrir les défenses du cerveau, suivie d’un médicament immunitaire qui aide les propres cellules T du patient à attaquer les cellules cancéreuses résiduelles. Pour les patients et les familles confrontés à ce diagnostic, le travail explore si une procédure peu invasive peut transformer un cancer quasi non réceptif en une tumeur qui réponde enfin à l’immunothérapie.
Une nouvelle façon d’aborder les tumeurs cérébrales récalcitrantes
Les patients de cet essai présentaient tous des astrocytomes de haut grade ayant récidivé après la thérapie standard, qui comprend généralement chirurgie, radiothérapie et chimiothérapie. Les chercheurs se sont concentrés sur deux outils. Le premier, la thérapie thermique interstitielle au laser (LITT), est une procédure par trou de serrure dans laquelle une sonde fine est guidée par IRM dans la tumeur et utilisée pour chauffer et détruire le tissu cancéreux tout en épargnant une grande partie du cerveau environnant. Le second outil est le pembrolizumab, un médicament d’immunothérapie largement utilisé qui bloque PD-1, un « frein » moléculaire qui empêche souvent les cellules T d’attaquer les tumeurs. Les tentatives antérieures d’utiliser ces médicaments seuls dans ces cancers cérébraux ont été décevantes. L’équipe s’est donc demandé si l’utilisation du laser en premier pouvait amorcer la tumeur et le système immunitaire pour mieux répondre au pembrolizumab. 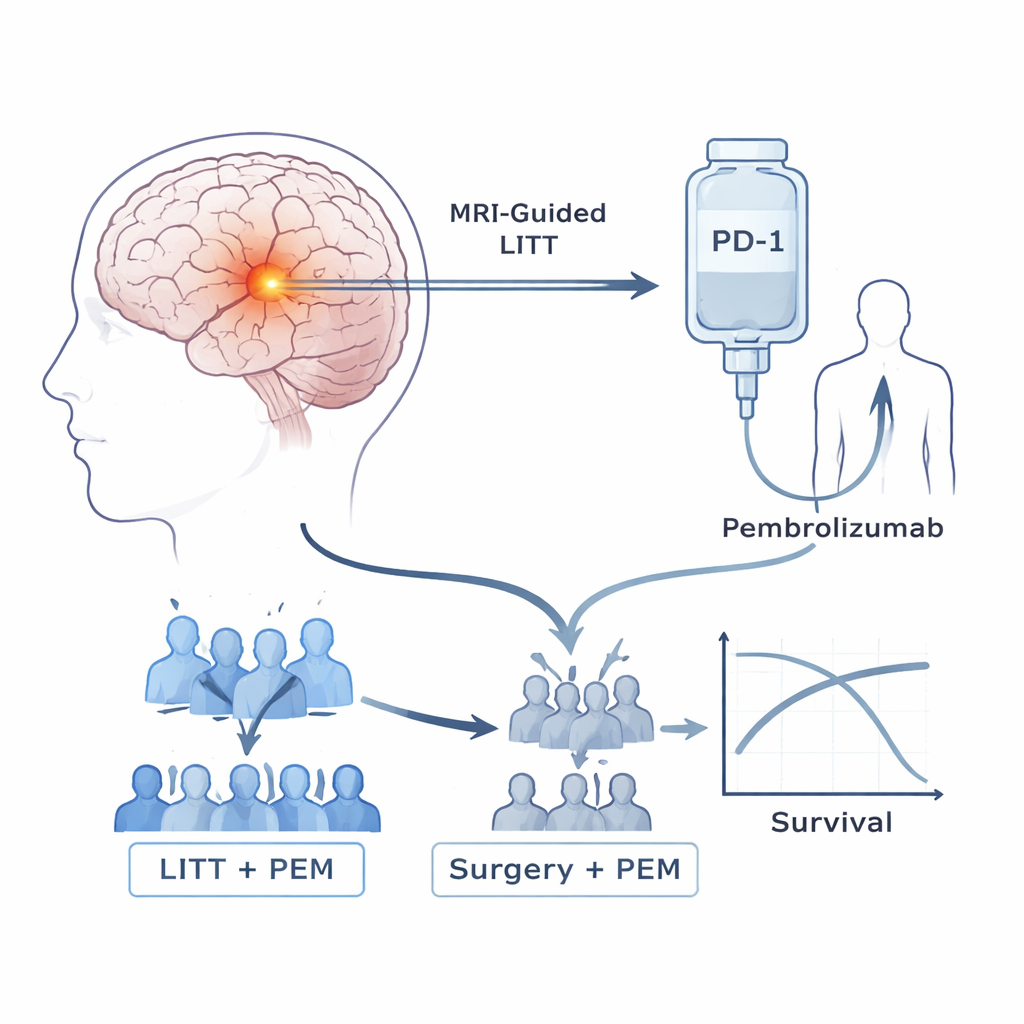
Comment l’essai clinique a été conduit
L’étude a débuté par une petite phase de sécurité, montrant que les patients pouvaient recevoir sans danger le pembrolizumab toutes les trois semaines après LITT, sans effets indésirables limitant la dose. Elle est ensuite passée à un essai de phase 2b. Initialement, les patients étaient assignés au hasard à l’un des deux groupes : LITT suivi de pembrolizumab, ou reprise chirurgicale conventionnelle sans laser, suivie de pembrolizumab. À mesure que des données externes montraient que la chirurgie associée à l’immunothérapie offrait peu de bénéfice par elle-même, un comité indépendant a examiné les premiers résultats de cet essai. Voyant des signes que le groupe sans laser se portait mal tandis que le groupe LITT semblait vivre plus longtemps, ils ont interrompu la randomisation et tous les patients recrutés par la suite ont reçu la combinaison laser-plus-médicament.
Ce qu’il est advenu de la survie et du contrôle tumoral
Parmi 39 patients ayant reçu le traitement prévu, ceux traités par LITT plus pembrolizumab ont vécu sensiblement plus longtemps que ceux ayant subi une chirurgie plus pembrolizumab. La survie globale médiane était d’environ 11,8 mois avec l’approche combinée LITT, contre 5,2 mois avec la seule chirurgie, et aucun patient du groupe chirurgie n’était vivant à 18 mois contre 42 % de ceux du groupe LITT. Le délai avant la reprise de la croissance tumorale s’est également amélioré, passant de 1,6 mois dans le groupe chirurgie à 4,5 mois avec LITT. Environ 27 % des patients traités par LITT ont présenté une réduction mesurable de leurs tumeurs et 70 % ont obtenu au moins un contrôle temporaire de la maladie, tandis que tous les patients ayant eu une chirurgie non laser plus pembrolizumab ont présenté une progression. Les effets indésirables de la combinaison étaient principalement légers et gérables, avec quelques cas de diarrhée, faiblesse musculaire et élévation des enzymes hépatiques, mais aucun décès lié au traitement.
Ce que faisait le système immunitaire
Pour comprendre pourquoi la combinaison pourrait fonctionner, les scientifiques ont examiné de près les cellules sanguines au fil du temps en utilisant le séquençage ARN unicellulaire et le suivi des récepteurs des cellules T. Après LITT, ils ont observé qu’un groupe spécifique de cellules immunitaires innées, appelées monocytes non classiques, passait à un état plus actif lié à la migration, l’inflammation et l’interaction avec les cellules T — changements non observés après une chirurgie standard. Lorsque le pembrolizumab a été ensuite initié, les patients ayant survécu plus longtemps ont montré de fortes vagues d’activation des cellules T CD8 et d’expansion clonale, signifiant que de nombreuses cellules T identiques ciblant les mêmes antigènes se multipliaient. Ces cellules T avaient tendance à évoluer vers des états mémoire et effecteurs capables de reconnaître et tuer les cellules tumorales, plutôt que de devenir épuisées et inefficaces. Les survivants à long terme ont également présenté une baisse de l’IDO-1, une molécule associée à la suppression immunitaire, suggérant que la combinaison pourrait lever plusieurs couches de freins immunitaires. 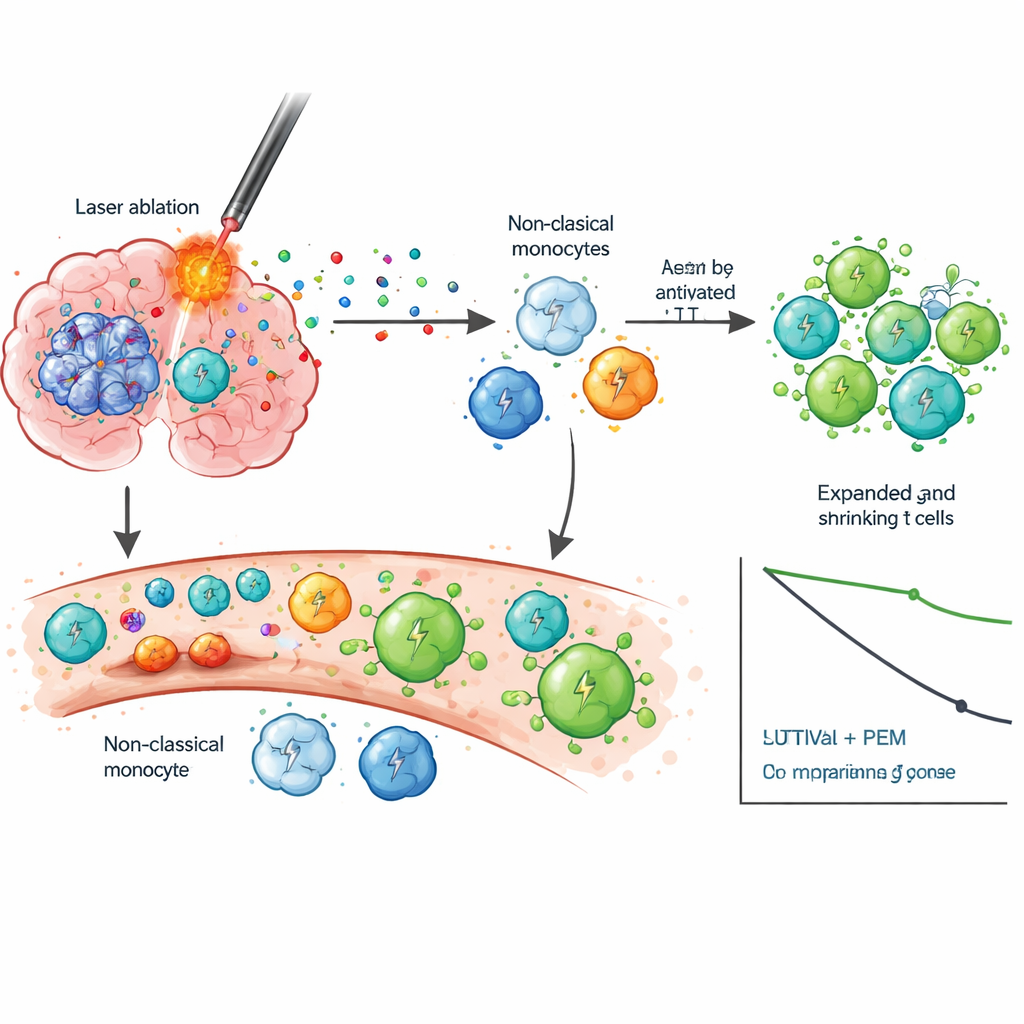
Ce que cela pourrait signifier pour les patients
Pour les personnes vivant avec un astrocytome de haut grade récurrent, ce travail suggère que l’utilisation d’une ablation au laser guidée par IRM pour réduire la masse tumorale, assouplir brièvement la barrière hémato-encéphalique et libérer des fragments tumoraux en circulation peut préparer le terrain pour que l’immunothérapie fonctionne là où elle échoue habituellement. En lançant un « signal » pour le système immunitaire puis en supprimant le frein PD-1 avec le pembrolizumab, la combinaison semble générer des réponses des cellules T plus durables et prolonger la survie face à un cancer ayant très peu d’options. Comme l’étude était relativement petite et que la randomisation a été interrompue tôt, les auteurs insistent sur le fait que des essais plus larges et entièrement contrôlés sont encore nécessaires. Néanmoins, les résultats pointent vers une stratégie prometteuse : associer une destruction tumorale physique précisément ciblée à des médicaments immunitaires pour transformer une tumeur cérébrale froide et résistante en une cible que l’organisme peut enfin reconnaître et combattre.
Citation: Campian, J.L., Le, S.B., Ghiaseddin, A. et al. Laser interstitial thermal therapy and adjuvant pembrolizumab in recurrent high-grade astrocytoma: a Phase 1/randomized Phase 2b trial. Nat Commun 17, 1763 (2026). https://doi.org/10.1038/s41467-026-69522-w
Mots-clés: glioblastome, ablation au laser, pembrolizumab, immunothérapie, tumeur cérébrale