Clear Sky Science · fr
Une signalisation FGFR3 excessive dans l’achondroplasie perturbe le renouvellement des chondrocytes de la zone de repos via la voie CREB
Pourquoi cette étude sur la croissance osseuse est importante
L’achondroplasie est la cause la plus fréquente de nanisme des membres d’origine génétique. Elle affecte non seulement la taille, mais aussi la santé de la colonne vertébrale, la mobilité et la qualité de vie. Les traitements actuels apportent des améliorations mais ne restaurent pas entièrement la croissance osseuse. Cette étude utilise un modèle murin sophistiqué pour mettre au jour une région problématique jusque-là peu explorée dans les os en croissance et identifie un nouvel interrupteur de signalisation, appelé CREB, comme cible prometteuse pour de futures thérapies.
Comment les os s’allongent normalement
Les os longs, comme le fémur, s’allongent au niveau des plaques de croissance situées près de leurs extrémités. Ces plaques sont organisées en trois couches principales de cellules cartilagineuses. Au sommet se trouve la zone de repos, où les cellules se comportent comme un réservoir de cellules souches, se divisant lentement et envoyant leurs descendantes vers le bas. En dessous, la zone proliférative contient des cellules qui se divisent rapidement et s’empilent en colonnes ordonnées assurant l’allongement. Plus loin, la zone hypertrophique réunit des cellules matures et élargies qui favorisent la formation d’os. L’équilibre entre ces zones maintient la croissance osseuse au bon rythme et à la bonne forme.
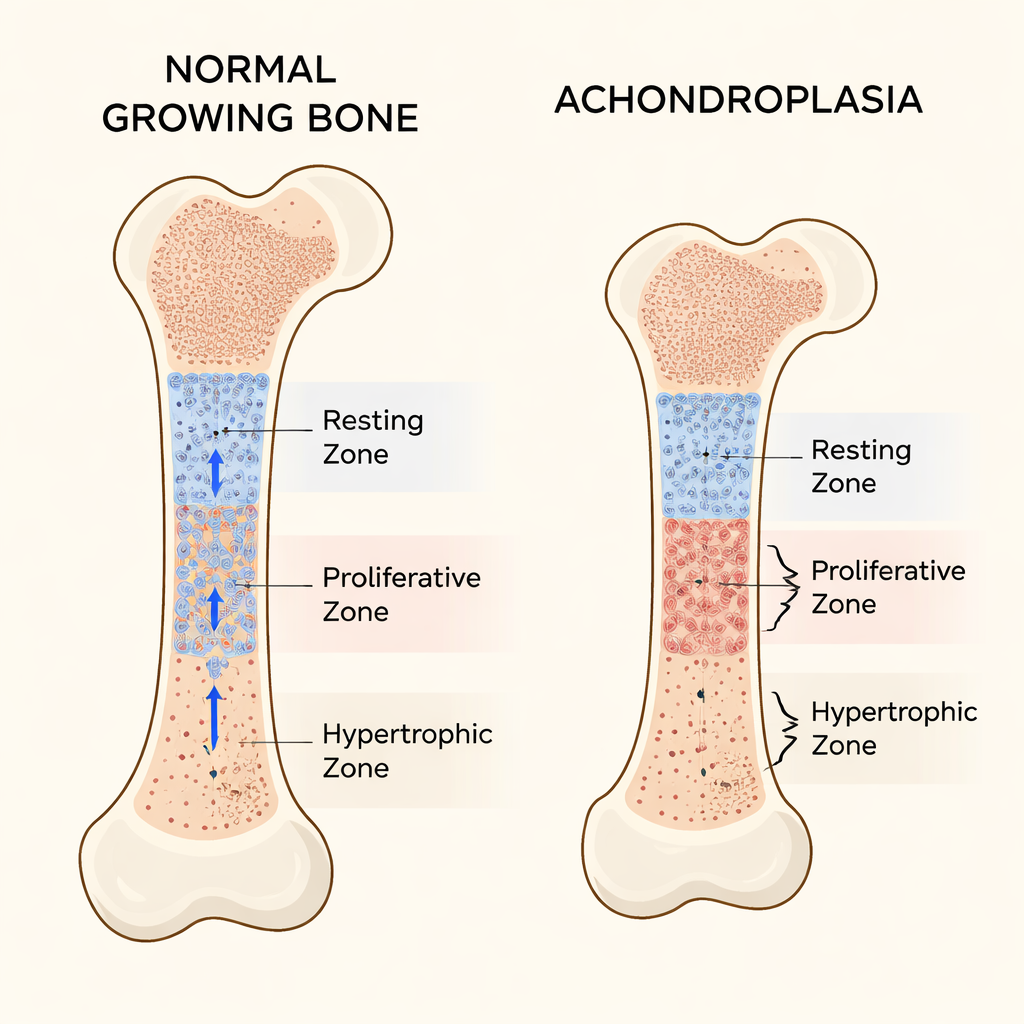
Ce qui tourne mal dans l’achondroplasie
Chez la plupart des personnes atteintes d’achondroplasie, une mutation unique du gène FGFR3 rend son récepteur hyperactif, freinant la croissance osseuse. Des travaux antérieurs ont montré que cette signalisation ralentit la division cellulaire dans la zone proliférative et bloque l’élargissement final des cellules dans la zone hypertrophique. En utilisant des souris génétiquement modifiées portant la mutation humaine d’achondroplasie, les auteurs ont confirmé des membres très courts et des plaques de croissance raccourcies. Mais des mesures détaillées ont révélé un aspect largement négligé : la zone de repos elle‑même devenait anormalement épaisse. Au lieu de fonctionner comme un réservoir de cellules souches stable et bien régulé, cette région s’étendait et contenait des cellules pauvres en matrice cartilagineuse normale.
Les cellules de la zone de repos perdent leur comportement « souche »
Pour comprendre cette expansion, l’équipe a suivi la division et le déplacement des cellules des plaques de croissance au fil du temps. Chez les souris normales, les cellules de la zone de repos se divisaient rarement, et leurs descendantes migrent vers le bas en colonnes droites pour reconstituer la zone proliférative. Chez les souris mutantes, beaucoup plus de cellules de la zone de repos se divisaient lentement et restaient sur place, formant une couche encombrée qui n’alimentait pas correctement les zones inférieures. Le traçage de lignée avec des étiquettes génétiques multicolores a montré que les colonnes clonales étaient courtes et désorganisées, les cellules filles errant dans des directions aléatoires au lieu de former des empilements ordonnés. Des marqueurs d’identité de type cellule souche, tels que la protéine CD73, étaient perdus dans la zone de repos élargie, suggérant qu’une FGFR3 hyperactive avait corrompu le microenvironnement stem‑cellulaire normal.
Un nouveau coupable de signalisation : CREB
Les chercheurs ont alors utilisé le séquençage ARN unicellulaire pour profiler des milliers de cellules individuelles des plaques de croissance. Ils ont identifié un groupe distinct correspondant à la zone de repos élargie, riche en expression du gène Spon1, entre autres. L’analyse des voies a mis en évidence l’activation de CREB, une protéine qui active des gènes lorsqu’elle est phosphorylée. La microscopie a montré que les cellules de la zone de repos chez les souris mutantes exprimaient fortement CREB activé et son co‑activateur CBP, ainsi que de forts niveaux de FGFR3 et de molécules en aval comme STAT5. En culture cellulaire, la stimulation de la voie FGFR3 augmentait l’activité de CREB et élevait SPONDIN1 (la protéine SPON1), tandis que le blocage de FGFR3 ou de CREB réduisait ces signaux. Cela place CREB comme un relais clé entre le récepteur hyperactif à la surface cellulaire et le comportement défaillant des cellules de la zone de repos.
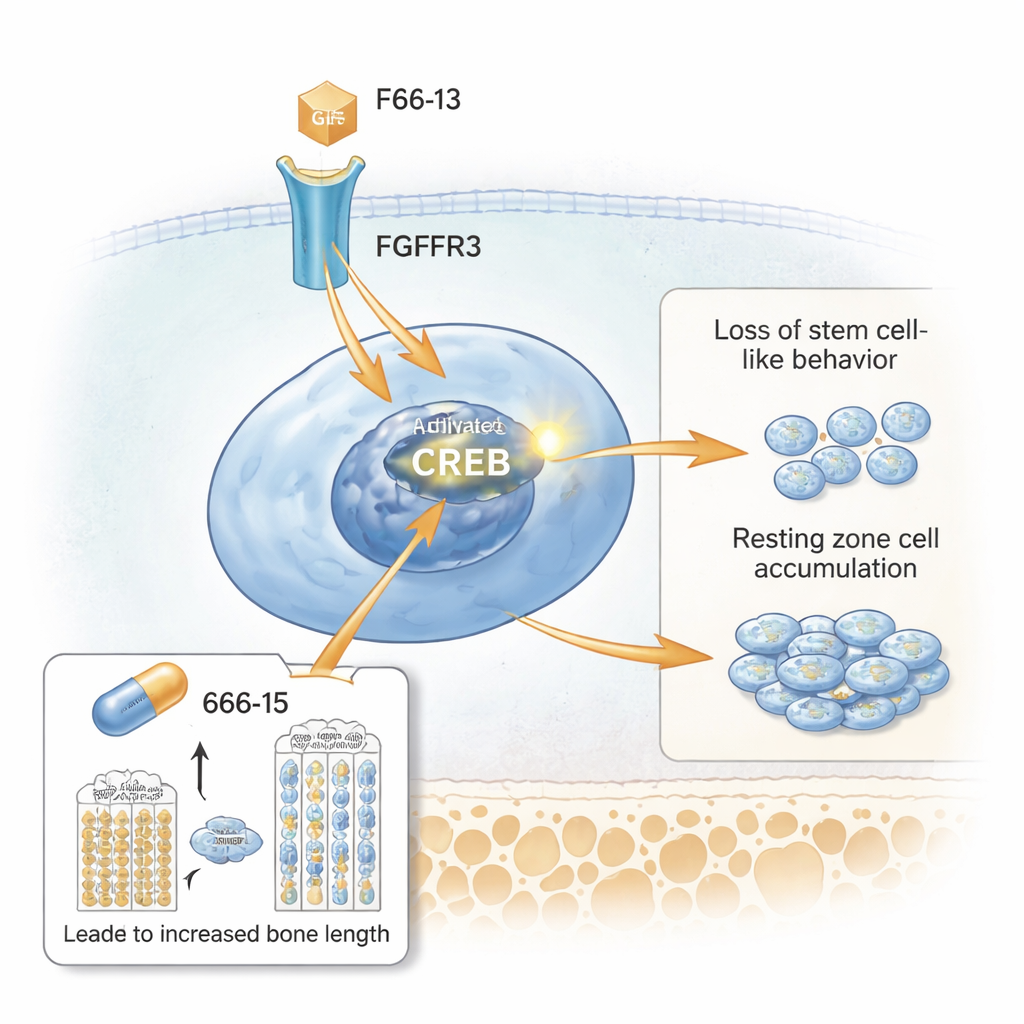
Test d’un médicament qui réduit l’activité de CREB
Enfin, l’équipe s’est demandé si l’atténuation de CREB pouvait améliorer les problèmes de croissance. Ils ont traité des souris modèles d’achondroplasie avec un inhibiteur de CREB de petite molécule, nommé 666‑15, pendant la période de croissance rapide après la naissance. Par rapport aux souris mutantes non traitées, celles ayant reçu 666‑15 présentaient un poids corporel plus élevé et des fémurs plus longs. Leurs plaques de croissance semblaient plus normales : la zone de repos s’était amincie, les zones proliférative et hypertrophique avaient retrouvé de la hauteur, et les protéines de la matrice cartilagineuse réapparaissaient. Les marqueurs d’une signalisation CREB excessive, incluant la phospho‑CREB, SPONDIN1 et STAT5, déclinaient dans la zone de repos, tandis que le marqueur de type cellule souche CD73 réapparaissait. Fait important, le même médicament avait peu d’effet sur des souris témoins saines à la dose testée, suggérant qu’il agit principalement lorsque CREB est anormalement élevé.
Ce que cela signifie pour les traitements futurs
L’étude montre que dans l’achondroplasie, une FGFR3 hyperactive fait plus que freiner la division et l’élargissement cellulaire : elle perturbe aussi la zone de repos calme et de type cellule souche en activant CREB. Cette perturbation prive les couches inférieures de la plaque de croissance de nouvelles cellules et contribue à la brièveté des os. Les médicaments existants comme le vosoritide ciblent principalement d’autres voies dans les zones proliférative et hypertrophique et ne restaurent que partiellement la longueur osseuse. En ajoutant CREB à la liste des cibles—en particulier dans la zone de repos—des thérapies combinées à l’avenir pourraient normaliser plus complètement la croissance chez les enfants atteints d’achondroplasie.
Citation: Horike, N., Oura, S., Koyamatsu, S. et al. Excess FGFR3 signaling in achondroplasia disrupts turnover of resting zone chondrocytes via CREB signaling. Nat Commun 17, 1856 (2026). https://doi.org/10.1038/s41467-026-69507-9
Mots-clés: achondroplasie, FGFR3, plaque de croissance, cellules souches cartilagineuses, signalisation CREB