Clear Sky Science · fr
Conception synergique d’électrodes pour une électrolyse du CO2 efficace vers des produits multicarbonés à températures élevées
Transformer la chaleur résiduelle en chimie utile
Des usines qui convertissent le dioxyde de carbone en carburants et produits chimiques utiles peuvent sembler de la science‑fiction, mais elles sont déjà en construction. À mesure que ces dispositifs deviennent plus grands et plus puissants, ils se réchauffent—un peu comme un ordinateur portable en charge. Cette étude montre que, au lieu de combattre cette chaleur avec des systèmes de refroidissement coûteux, une conception intelligente des électrodes peut exploiter des températures plus élevées pour transformer le CO2 plus efficacement en produits riches en énergie et à plusieurs atomes de carbone, tels que l’éthylène et les alcools.
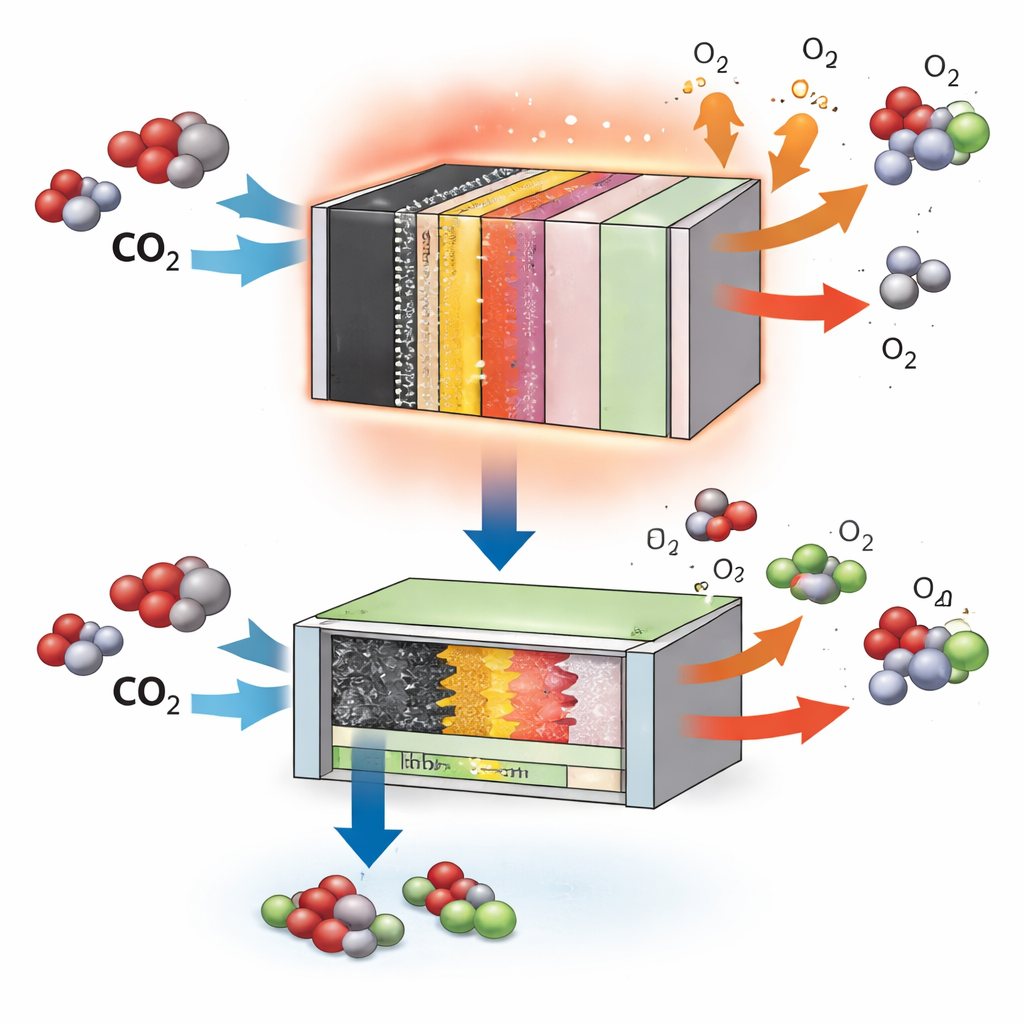
Pourquoi des réacteurs plus chauds sont une arme à double tranchant
L’électrolyse industrielle du CO2 fait circuler de l’électricité à travers de l’eau et du CO2 pour fabriquer de nouvelles molécules. La montée en échelle de ces systèmes accroît la résistance électrique et réduit l’évacuation de la chaleur, ce qui élève la température de la cellule bien au‑dessus de la température ambiante. Une température plus élevée accélère les réactions chimiques et abaisse les barrières énergétiques—en principe une bonne nouvelle—mais elle introduit aussi des problèmes sérieux. Le cuivre, le métal phare qui aide à relier les atomes de carbone, modifie sa structure de surface lorsqu’il est chauffé. Les électrodes à diffusion de gaz, qui équilibrent soigneusement les régions gazeuses, liquides et solides, commencent à s’engorger de vapeur d’eau. Parallèlement, des intermédiaires réactionnels à base de CO se détachent trop tôt de la surface, et le système produit alors de l’hydrogène et des produits simples à un seul carbone, gaspillant à la fois électricité et CO2.
Identifier les maillons faibles dans la cellule chaude
Les chercheurs ont chauffé systématiquement un réacteur à cellule à flux de la température ambiante à 75 °C et observé le comportement d’électrodes à base de cuivre. À l’aide d’un ensemble de sondes structurales, ils ont constaté que le cuivre nu s’oxyde rapidement et se restructure subtilement à haute température, déplaçant la production de molécules utiles à deux carbones vers le méthane et l’hydrogène. Une forme plus stable, des nanocubes d’oxyde cuivreux (Cu2O), a mieux conservé sa structure mais a tout de même mal performé à chaud. Le coupable s’est avéré ne pas être seulement le catalyseur lui‑même, mais aussi l’environnement alentour : l’augmentation de la pression de vapeur d’eau a inondé l’électrode à diffusion de gaz, obstruant l’accès au CO2 et agrandissant la zone où seul l’hydrogène peut se former. Même lorsque l’inondation était maîtrisée, une température plus élevée favorisait la désorption des intermédiaires CO avant qu’ils ne puissent se coupler en produits multicarbonés.
Concevoir une électrode plus intelligente et répulsive à l’eau
Pour transformer cet environnement hostile en avantage, l’équipe a redesigné la cathode en une structure en couches « en tandem ». D’abord, ils ont mélangé le catalyseur Cu2O avec de minuscules particules de polytétrafluoroéthylène (PTFE)—un matériau fortement déperlant—pour stabiliser l’interface gaz–liquide–solide fragile et prévenir l’inondation, même à haute température et à fort courant. Ensuite, ils ont ajouté une couche d’argent qui excelle à convertir le CO2 en CO, fournissant un flux constant d’intermédiaires CO vers le Cu2O. Enfin, ils ont décoré la surface de Cu2O avec des atomes isolés de palladium, qui lient le CO plus fortement et le maintiennent suffisamment longtemps en surface pour permettre la formation de liaisons carbone–carbone. Ensemble, ces couches gèrent l’eau, la concentration locale en gaz et la force de liaison des intermédiaires de sorte que l’énergie thermique supplémentaire abaisse la barrière pour le couplage carbone–carbone au lieu d’accélérer simplement les réactions parasites.
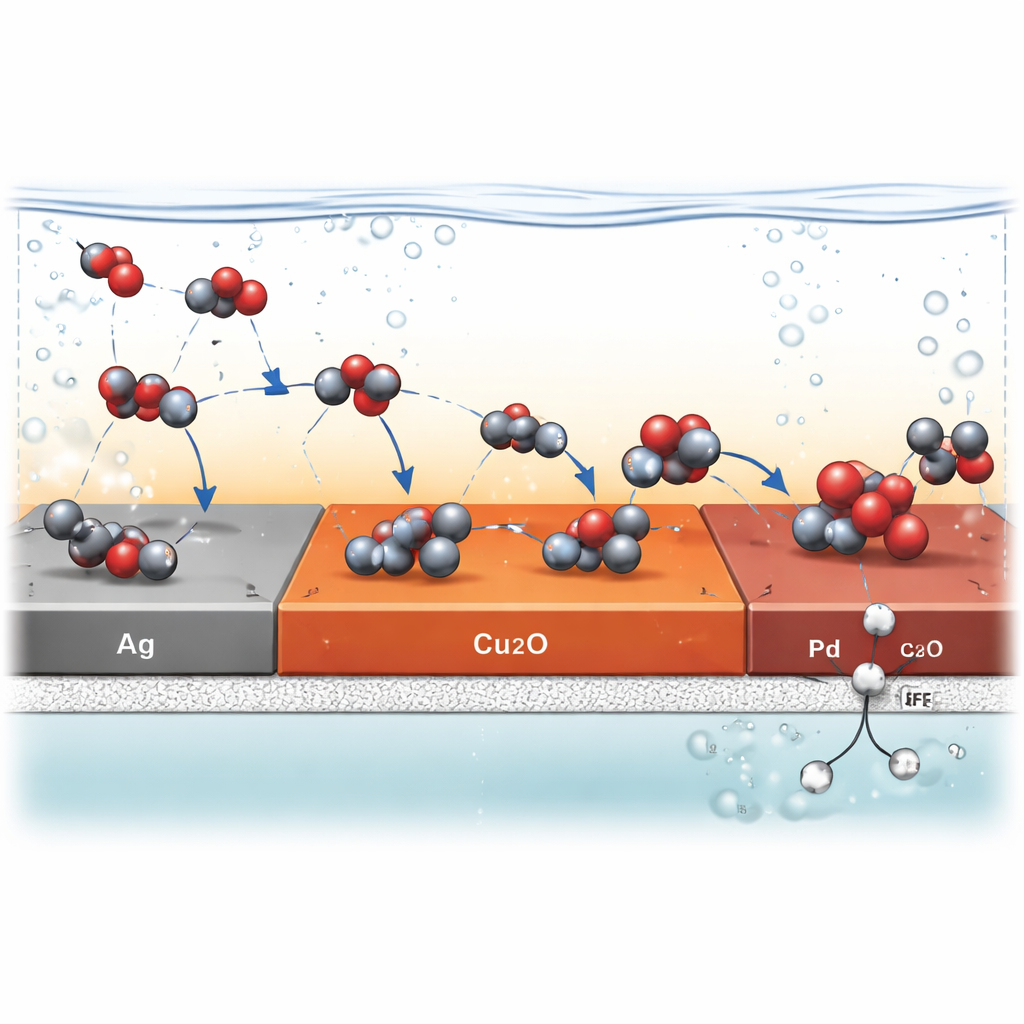
Faire de la chaleur un allié plutôt qu’un ennemi
Avec cette conception synergique d’électrode, le réacteur a atteint plus de 70 % d’efficacité faradique pour les produits multicarbonés à des densités de courant pertinentes industriellement à 75 °C, tout en fonctionnant de manière stable pendant de nombreuses heures. La cellule plus chaude n’a pas seulement produit des produits plus désirables, elle a aussi utilisé l’électricité plus efficacement : l’efficacité énergétique vers les produits multicarbonés s’est améliorée d’environ 30 % par rapport au fonctionnement à température ambiante. Une analyse économique préliminaire a indiqué que fonctionner à chaud et éliminer le refroidissement actif pourrait réduire près de 15 % des coûts d’exploitation liés au contrôle de la température. En termes simples, l’étude montre que la chaleur résiduelle dans de grandes usines de conversion du CO2 en produits chimiques peut être transformée, de source de problèmes de fiabilité, en un puissant allié—si l’électrode est soigneusement conçue pour contrôler l’eau, l’accès aux gaz et la force d’adsorption des intermédiaires réactionnels à la surface.
Citation: Hu, L., Yang, Y., Wang, J. et al. Synergistic electrode design for efficient CO2 electrolysis to multicarbon products at elevated temperatures. Nat Commun 17, 2684 (2026). https://doi.org/10.1038/s41467-026-69506-w
Mots-clés: électrolyse du CO2, carburants multicarbonés, électrocatalyse, décarbonation industrielle, réacteurs à cellule à flux