Clear Sky Science · fr
Densité de charge du métal hydraté comme descripteur universel expliquant les variations mécanistiques de l’activation du périodate pour la dégradation des polluants
Assainir l’eau par une chimie intelligente
Beaucoup de médicaments et de produits chimiques industriels passent à travers les stations d’épuration classiques et se retrouvent dans les rivières et les eaux potables. Cette étude explore une voie prometteuse pour décomposer ces polluants tenaces en utilisant un oxydant courant, le périodate, et montre qu’une propriété simple des ions métalliques en solution peut prédire l’efficacité — et la sécurité — de cette chimie. Comprendre cette règle pourrait aider les ingénieurs à concevoir des systèmes de traitement plus propres et plus efficaces pour des eaux réelles et variées.
Pourquoi le choix du métal compte pour la dégradation des polluants
Les procédés d’oxydation avancés utilisent des espèces réactives puissantes pour déchiqueter les molécules organiques. Le périodate est un de ces oxydants, et il peut être « activé » par des ions métalliques dissous. Les auteurs ont comparé trois métaux étroitement liés — le fer, le ruthénium et l’osmium — qui appartiennent à la même colonne du tableau périodique et qui pourraient a priori se comporter de façon similaire. Les trois peuvent activer le périodate et aider à détruire un polluant test, la carbamazépine. Pourtant, les expériences ont révélé des différences marquées : le ruthénium agit extrêmement vite, le fer est plus lent, et l’osmium se situe entre les deux. Plus surprenant encore, l’osmium éliminait une large variété de polluants sans grande préférence, tandis que le fer et le ruthénium étaient sélectifs, attaquant certains composés beaucoup plus facilement que d’autres.
Deux voies chimiques très différentes
Pour comprendre l’origine de ces différences, l’équipe a suivi quelles espèces oxydantes de courte durée de vie apparaissaient dans chaque système métal–périodate. Avec le fer et le ruthénium, les acteurs dominants étaient des unités « métal–oxygène » qui fonctionnent comme des outils de précision, transférant un atome d’oxygène directement à des sites spécifiques d’un polluant. Ces voies formaient souvent des produits époxy — structures cycliques incorporant un seul atome d’oxygène — indiquant que la réaction est assez sélective. Dans le système à l’osmium, en revanche, les principaux acteurs étaient des radicaux hydroxyle, des fragments extrêmement réactifs qui attaquent presque n’importe quelle molécule organique voisine, conduisant à des produits hydroxylés et à de petits fragments résultant de l’ouverture de cycles. Des tests avec des sondes chimiques et la spectroscopie de piégeage de spins ont confirmé que les radicaux hydroxyle et des espèces réactives apparentées de l’oxygène, et non des unités osmium–oxygène à valence élevée, pilotent la majeure partie de la destruction des polluants en présence d’osmium.
Comment les conditions de l’eau modulent les réactions
L’équipe a également examiné comment le pH et les constituants naturels de l’eau influencent ces processus. Pour l’osmium, l’élimination des polluants s’intensifiait avec l’augmentation de l’alcalinité, car la coordination d’ions hydroxyle supplémentaires autour du métal facilite le mouvement des électrons et la formation de radicaux. À fortes concentrations de métal ou d’oxydant, toutefois, le système à l’osmium se « s’éteignait » : les radicaux nouvellement formés étaient neutralisés par l’excès de réactifs plutôt que par les polluants. La matière organique naturelle, qui interfère souvent avec les réactions d’oxydation, avait étonnamment peu d’impact sur la dégradation pilotée par l’osmium, ce qui suggère que la voie radicalaire reste robuste dans des eaux réalistes. En revanche, le fer et le ruthénium donnaient les meilleurs résultats en conditions acides, et la matière organique naturelle supprimait fortement leur activité en piégeant les oxydants métal–oxygène clés.
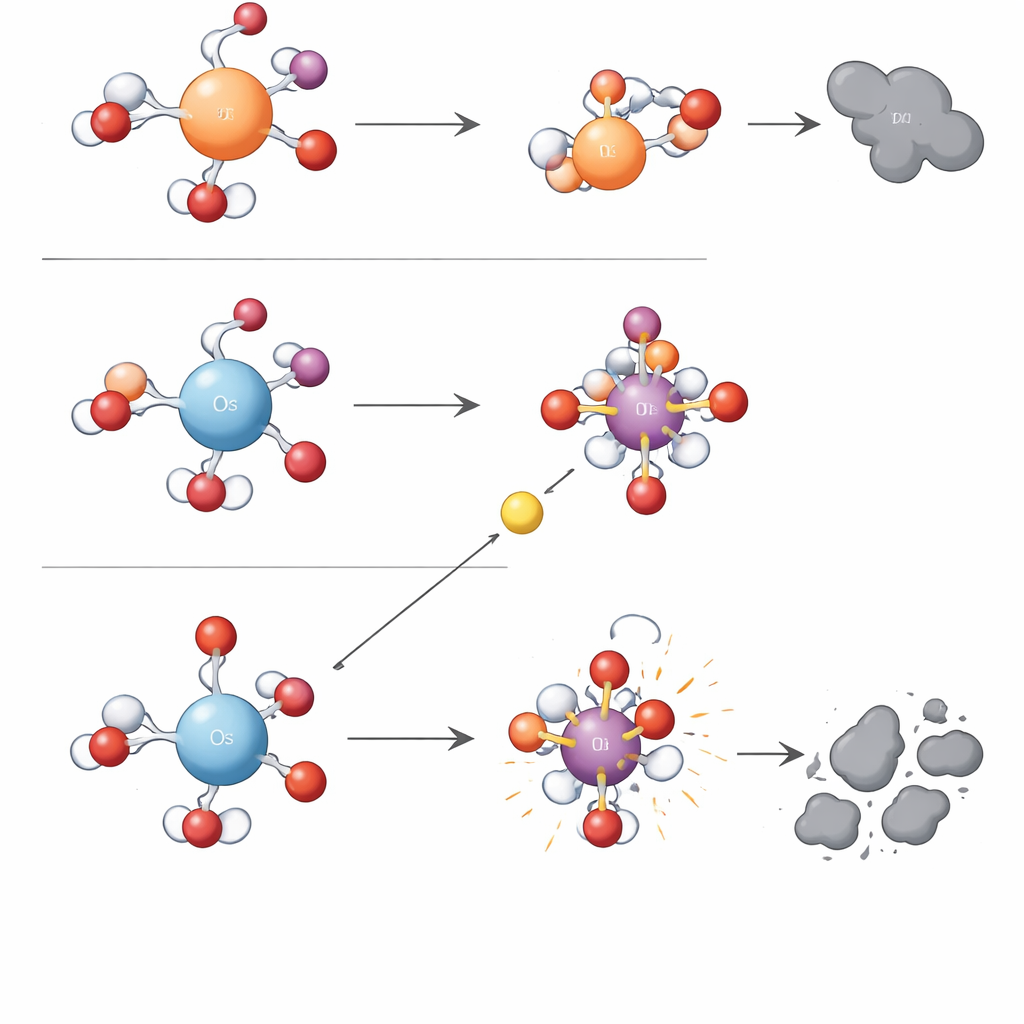
Une règle simple de charge derrière une chimie complexe
Pour dépasser l’approche empirique, les chercheurs ont eu recours à des calculs quantum-chimiques. Ils ont trouvé qu’une seule caractéristique électronique — la densité de charge positive du centre métallique hydraté — pouvait expliquer la séparation entre les deux types de réaction. L’osmium en solution porte une charge positive plus concentrée que le fer ou le ruthénium. Ce centre fortement positif retient fermement son atome d’oxygène lié, rendant son unité métal–oxygène stable mais peu encline au transfert direct d’oxygène. Dans le même temps, la forte attraction exercée sur l’eau et les ions voisins abaisse la barrière énergétique pour les étapes à électron unique qui finissent par rompre une liaison d’oxygène dans le périodate et libérer des radicaux hydroxyle. Les métaux à densité de charge plus faible, comme le fer et le ruthénium, tiennent les électrons plus étroitement, favorisant la formation et l’utilisation des oxydants métal–oxygène sélectifs plutôt que des radicaux libres. Les auteurs appellent cette idée organisatrice le « mécanisme de contrôle par densité de charge » et montrent qu’elle rationalise également des tendances rapportées pour d’autres métaux tels que le manganèse.
Concevoir de meilleurs traitements de l’eau à partir d’un seul réglage
En reliant un ensemble d’observations complexes à un seul descripteur simple — la densité de charge d’un métal entouré d’eau — ce travail offre une feuille de route pour adapter les procédés d’oxydation avancés. Les métaux à haute densité de charge devraient favoriser une dégradation large et radicalaire des mélanges complexes de polluants, notamment dans des eaux alcalines ou riches en matière organique. Les métaux à densité de charge plus faible conviennent mieux lorsque l’on souhaite une oxydation sélective et plus douce, par exemple pour transformer des contaminants spécifiques sans réagir excessivement avec tout le reste. En termes pratiques, cela signifie que chimistes et ingénieurs peuvent sélectionner ou concevoir des catalyseurs pour la purification de l’eau en ajustant la façon dont les centres métalliques retiennent la charge dans leur environnement aqueux, plutôt que d’optimiser chaque système par essais et erreurs.
Citation: Qian, Y., Sun, Y., Xu, J. et al. Hydrated metal charge density as a universal descriptor explaining mechanistic variations in periodate activation toward pollutant degradation. Nat Commun 17, 2683 (2026). https://doi.org/10.1038/s41467-026-69496-9
Mots-clés: procédés d’oxydation avancés, activation du périodate, traitement de l’eau, catalyse par métaux de transition, radicaux hydroxyle