Clear Sky Science · fr
Flux de travail de protéomique chimique à haut débit pour profiler la dynamique de la citrullination des protéines
Pourquoi la modification des éléments constitutifs des protéines compte
Nos cellules ajustent en permanence le comportement des protéines en leur ajoutant de petites modifications chimiques après leur synthèse. L’une de ces modifications, appelée citrullination, change subtilement la charge d’un acide aminé courant et peut remodeler la façon dont les protéines se replient, se lient à l’ADN ou interagissent avec d’autres molécules. Ces petites éditions sont de plus en plus associées aux maladies auto‑immunes, aux infections, au cancer et aux fonctions cérébrales — mais elles sont notoirement difficiles à détecter. Cette étude présente un protocole de laboratoire à haut débit qui permet enfin de cartographier la citrullination à l’échelle de milliers de protéines, révélant quand et où elle apparaît dans les tissus et les cellules immunitaires.
Un interrupteur caché sur les protéines
La citrullination se produit lorsque des enzymes appelées PAD modifient chimiquement l’acide aminé arginine, en lui retirant sa charge positive. Ce changement apparemment minime peut desserrer l’empaquetage de l’ADN, modifier la rigidité des protéines structurelles ou altérer la façon dont le système immunitaire reconnaît nos propres tissus. Une citrullination anormale a été impliquée dans la polyarthrite rhumatoïde, les troubles neurodégénératifs, les infections virales et le cancer. Pourtant, les protéines citrullinées sont rares et facilement confondues avec d’autres modifications plus courantes, de sorte que les méthodes standard de spectrométrie de masse les manquent souvent. Le résultat est que les chercheurs n’avaient jusqu’à présent qu’une vision fragmentaire du « citrullinome » du corps — l’ensemble des protéines citrullinées.
Une stratégie en deux étapes « marquer‑et‑capturer »
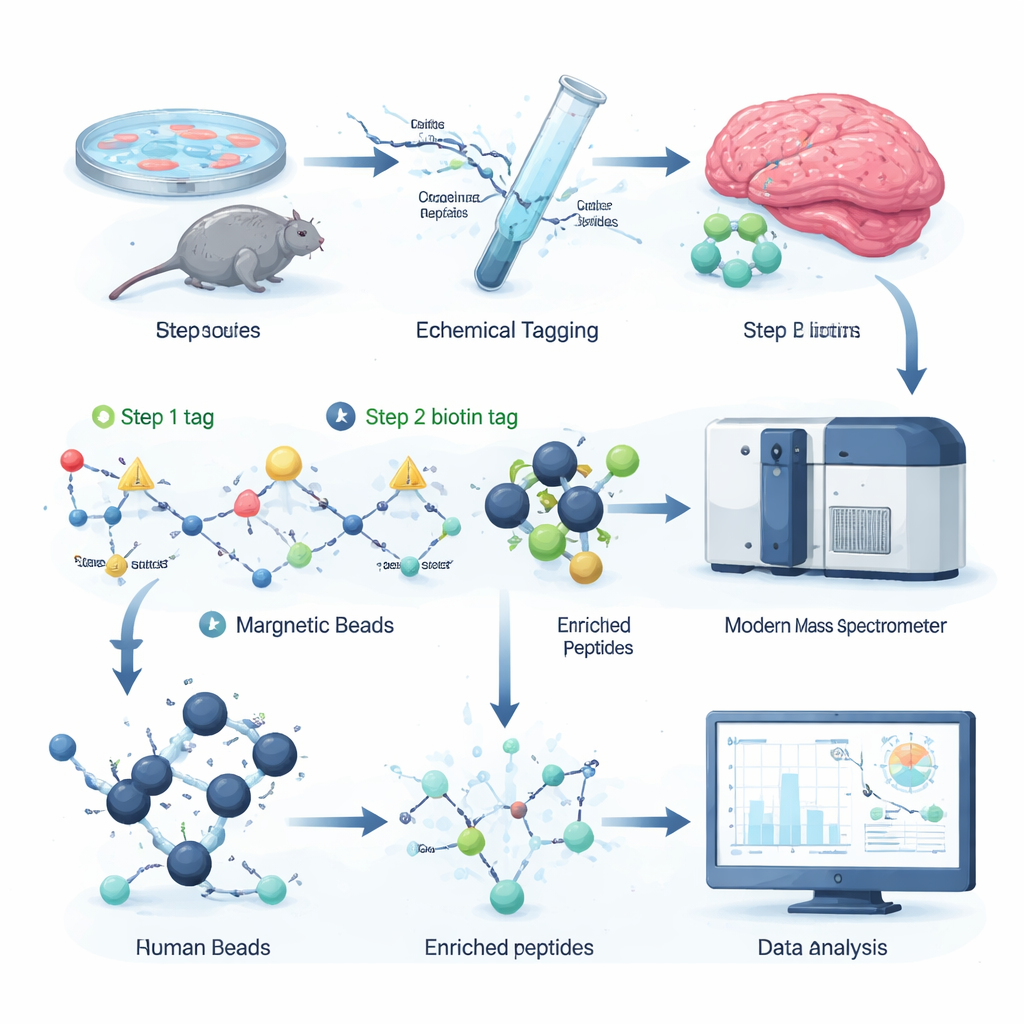
Les auteurs ont conçu une stratégie de marquage chimique qui attache sélectivement une « poignée » amovible aux sites citrullinés des peptides, les fragments de protéines analysés par spectrométrie de masse. Dans la première étape, une petite molécule réactive reconnaît la citrulline et installe un petit tag. Dans la seconde, un plus grand tag à la biotine est cliqué, permettant de récupérer les peptides marqués hors d’un mélange complexe à l’aide de billes d’avidine/streptavidine, un outil biochimique courant. Un traitement chimique doux coupe ensuite la partie encombrante du tag, ne laissant qu’un léger décalage de masse bien défini que le spectromètre de masse peut détecter facilement. Comme tous les réactifs sont commerciaux et que le protocole entier tient dans des plaques 96 puits, le flux de travail est rapide, évolutif et compatible avec les installations de protéomique existantes.
Voir davantage du citrullinome
En ajoutant des peptides citrullinés connus dans des extraits cellulaires puis en les diluant systématiquement, l’équipe a montré que leur stratégie d’enrichissement augmente le signal des peptides citrullinés de plus de dix fois, même lorsqu’ils représentent moins d’un sur mille molécules. Dans des échantillons complexes, le nombre de sites citrullinés détectés et leurs intensités mesurées augmentent fortement après enrichissement. L’application de la méthode à du tissu cérébral de souris a révélé deux à trois fois plus de sites distincts de citrullination qu’une approche de pointe précédente, y compris de nombreux sites sur la protéine basique de la myéline, qui isole les fibres nerveuses, et sur des protéines impliquées dans la communication synaptique. Cela suggère que la citrullination peut influencer à la fois la façon dont les cellules nerveuses communiquent et la maintenance du câblage cérébral.
Des cellules immunitaires qui projettent des toiles protéiques collantes
Les neutrophiles, un type de globules blancs en première ligne, peuvent combattre les envahisseurs en déployant des toiles collantes d’ADN et de protéines appelées pièges extracellulaires de neutrophiles, ou NETs. La formation des NET dépend de PAD4, une enzyme citrullinante qui desserre la chromatine pour permettre la libération d’ADN. En utilisant leur nouveau flux de travail, les chercheurs ont suivi comment la citrullination évoluait dans des neutrophiles humains exposés à des doses croissantes d’un activateur chimique. Ils ont détecté jusqu’à 1 700 fragments peptidiques citrullinés répartis sur 580 protéines, avec des centaines de sites augmentant ou diminuant de façon dépendante de la dose tandis que les niveaux protéiques globaux restaient constants. Les histones — les protéines qui emballent l’ADN — présentaient une citrullination généralisée, pas seulement à quelques sites classiques, et les variantes de l’histone linker H1 étaient particulièrement modifiées. Des protéines structurelles telles que des régulateurs de l’actine et la lamin B, qui façonne l’enveloppe nucléaire, devenaient également fortement citrullinées, indiquant un ramollissement coordonné à la fois de la chromatine et de l’ossature cellulaire lors de la libération des NET.
Une signature centrale de citrullination lors de l’infection
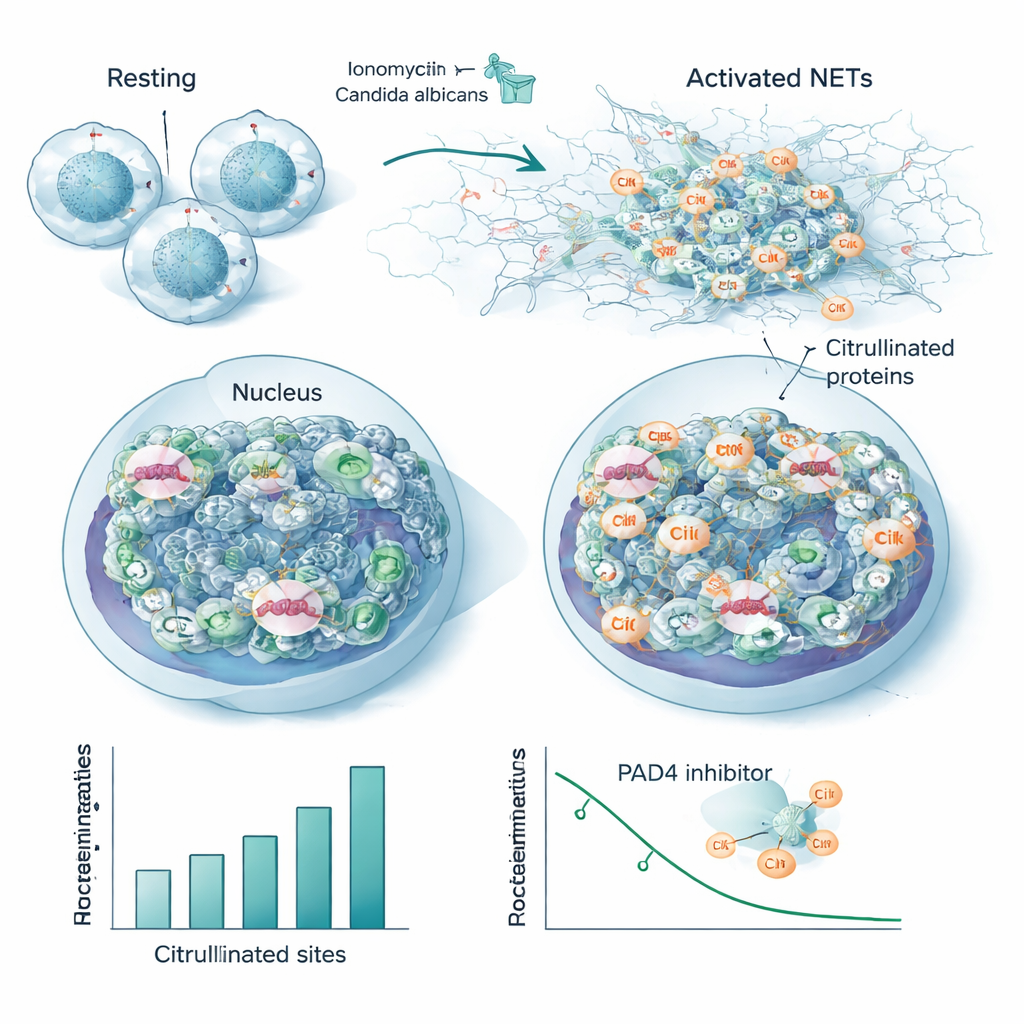
Pour imiter une infection réelle, l’équipe a stimulé des neutrophiles avec Candida albicans tué par la chaleur, un pathogène fongique courant. Bien que cela ait produit moins de sites modifiés au total que le fort activateur chimique, la grande majorité des protéines et positions citrullinées se chevauchaient entre les deux déclencheurs. Ce chevauchement définit un « citrullinome central » conservé associé à la formation des NET, incluant de nombreuses protéines nucléaires et cytosquelettiques ainsi que plusieurs auto‑antigènes connus — les cibles mêmes des anticorps dans les maladies auto‑immunes. Lorsque les chercheurs ont ajouté un médicament bloquant PAD4, bon nombre de ces mêmes sites ont perdu leur citrullination de façon dépendante de la dose, les reliant directement à l’activité de l’enzyme et suggérant qu’ils pourraient servir d’indicateurs sensibles de l’inhibition de PAD4.
Ce que cela signifie pour la santé et la maladie
En transformant une modification insaisissable en un signal mesurable, ce flux de travail permet désormais de cartographier où et quand la citrullination survient dans les tissus, les réponses immunitaires et les modèles de maladie. Pour le non‑spécialiste, le message clé est que la citrullination agit comme un variateur moléculaire subtil sur les protéines, et pouvoir visualiser ses motifs en haute résolution pourrait aider à expliquer comment les maladies auto‑immunes démarrent, comment les infections reprogramment les cellules immunitaires et comment les protéines cérébrales évoluent avec le temps. L’évolutivité de la méthode et son recours à du matériel de laboratoire standard signifient qu’elle peut être largement adoptée, ouvrant la voie à la découverte de nouvelles cibles médicamenteuses, à des diagnostics de précision et à une compréhension approfondie de la manière dont de petites modifications chimiques peuvent avoir de grandes conséquences biologiques.
Citation: Meelker González, R., Laposchan, S., Riedel, E. et al. High-throughput chemical proteomics workflow for profiling protein citrullination dynamics. Nat Commun 17, 1982 (2026). https://doi.org/10.1038/s41467-026-69490-1
Mots-clés: citrullination, maladie auto-immune, filets extracellulaires de neutrophiles, spectrométrie de masse, modification post‑tradutionnelle