Clear Sky Science · fr
Signification pathophysiologique de l’altération de l’acétylation de l’histone H3K14 dépendante de KAT7 lors d’une carence en zinc
Pourquoi de minuscules nutriments comptent pour notre santé
Le zinc est un oligo‑élément dont notre organisme a besoin en très petites quantités, et pourtant il soutient discrètement des centaines de protéines essentielles au fonctionnement cellulaire. Lorsque le zinc manque — en raison de l’alimentation, d’une maladie ou du vieillissement — cela a été associé à des troubles allant d’une croissance ralentie à une immunité affaiblie ou à la stéatose hépatique. Cette étude pose une question plus profonde : comment les cellules détectent‑elles concrètement la baisse de zinc, et comment cette pénurie peut‑elle se traduire en modifications durables de l’activité génique et de la santé des organes ?
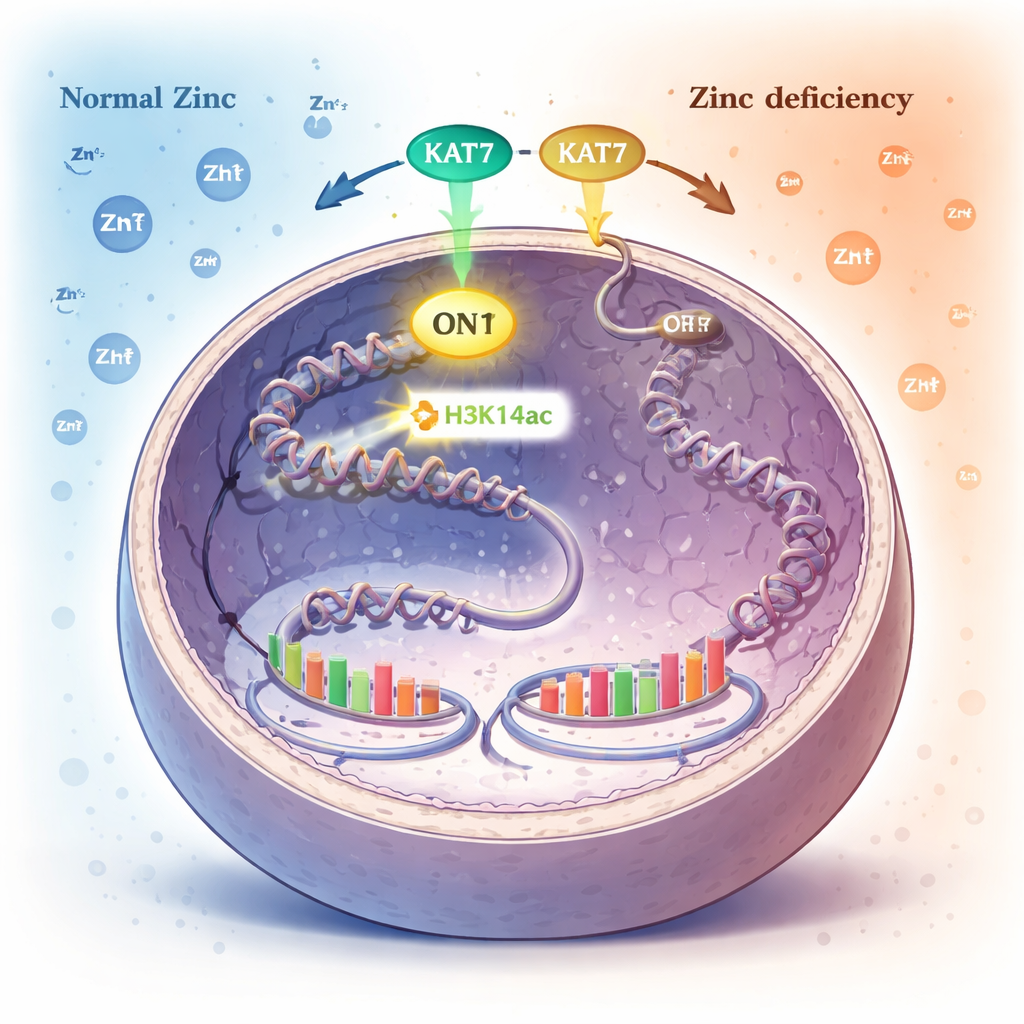
Une marque chimique sur l’emballage de l’ADN comme alarme interne au zinc
Dans le noyau, l’ADN s’enroule autour de bobines protéiques appelées histones. Les cellules régulent l’expression des gènes en ajoutant ou en retirant de petites marques chimiques sur ces histones. L’une de ces marques, l’acétylation en un point précis de l’histone H3 (H3K14ac), est déposée par une enzyme nommée KAT7. Les auteurs ont découvert que lorsque le zinc devient rare, les niveaux de cette marque H3K14ac chutent fortement, tandis que de nombreuses autres modifications histones courantes restent inchangées. Cela a désigné H3K14ac, et l’enzyme KAT7 qui la crée, comme un capteur clé du statut en zinc.
Comment le zinc maintient une enzyme clé activée
En désactivant systématiquement différentes enzymes, les chercheurs ont montré que KAT7 est la principale source de H3K14ac dans les cellules humaines. KAT7 contient une petite structure de liaison au zinc dans son site actif. Lorsque les cellules ont été soumises à une carence en zinc, la capacité de KAT7 à déposer la marque H3K14ac a diminué, bien que la protéine reste présente dans le noyau et associée à ses partenaires. Des tests approfondis sur des fragments purifiés de KAT7 ont révélé que le zinc correctement lié dans cette région est essentiel à son activité ; perturber la liaison au zinc éteint l’enzyme, et réintroduire soigneusement du zinc restaure sa fonction. En substance, KAT7 agit comme un interrupteur dépendant du zinc qui contrôle une modification histone spécifique.
Transformer la perte de zinc en changements géniques qui restaurent les apports
Que provoque concrètement la perte de cette marque histone ? Grâce à un cartographie à l’échelle du génome, l’équipe a montré que H3K14ac est particulièrement enrichie aux régions enhancers — des segments régulateurs d’ADN qui modulеnt finement les gènes voisins. En condition de carence en zinc, H3K14ac était retirée de nombreux enhancers, et plus la perte était importante, plus l’activité des gènes voisins changeait. Un gène s’est distingué : ZIP10, qui code pour une protéine membranaire assurant l’importation du zinc. Lorsque H3K14ac chutait à l’enhancer de ZIP10, le niveau de ZIP10 à la membrane augmentait, permettant davantage d’entrée de zinc dans la cellule. Bloquer KAT7 ou empêcher la perte de H3K14ac perturbait cette réponse et réduisait l’absorption de zinc, même après réapport de zinc. Cela montre que les cellules convertissent la rareté du zinc en un signal épigénétique qui renforce la machinerie d’import du zinc pour rétablir l’équilibre.
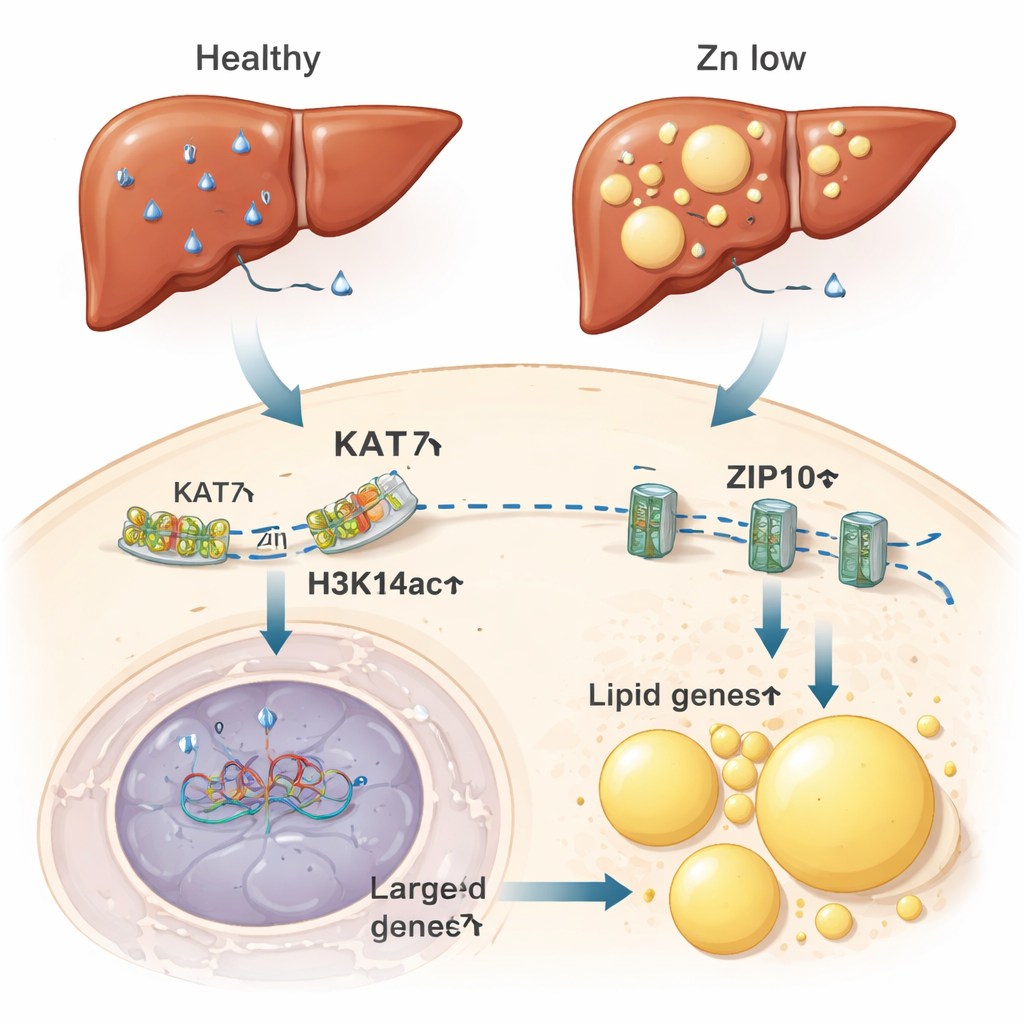
De cellules en manque de zinc à des foies gras
Les auteurs se sont ensuite demandé si cet interrupteur sensible au zinc avait des conséquences chez l’animal entier. Chez des souris nourries avec un régime pauvre en zinc, le foie — centre névralgique du métabolisme du zinc et des lipides — présentait des niveaux réduits de zinc, une baisse de H3K14ac et une activité atténuée de KAT7. Ces changements coïncidaient avec une expression accrue de gènes favorisant le stockage lipidique et la formation de gouttelettes lipidiques, ces micro‑compartiments de graisse intracellulaires. Les foies des souris carencées en zinc accumulaient des lipides à un degré comparable à celui observé chez des animaux soumis à un régime riche en graisses. De manière remarquable, réduire simplement l’activité de KAT7 à l’aide d’un médicament, sans modifier l’apport alimentaire en zinc, suffisait à favoriser l’accumulation de graisse dans les cellules hépatiques. Inversement, un apport supplémentaire en zinc atténuait l’accumulation de lipides induite par un régime riche en graisses.
Ce que cela implique pour le risque de maladie chez l’humain
En resituant leurs résultats dans un contexte clinique, les chercheurs ont passé en revue des études humaines ayant mesuré le zinc dans le tissu hépatique. Dans plusieurs travaux, les personnes atteintes de stéatose hépatique et de troubles associés présentaient significativement moins de zinc dans le foie que des sujets sains. Avec les expériences chez la souris, cela suggère qu’une carence chronique en zinc peut favoriser la maladie du foie gras en désactivant KAT7, en effaçant la marque H3K14ac et en augmentant de façon durable l’expression de gènes qui favorisent le stockage des lipides. En termes simples, ce travail révèle un circuit interne « zinc‑vers‑épigénétique » : lorsque le zinc baisse, une enzyme dépendante du zinc perd de son activité, remodelant l’emballage de l’ADN d’une manière qui aide d’abord les cellules à accroître l’importation de zinc, mais qui, à la longue, peut aussi pousser le foie vers une accumulation lipidique pathologique.
Citation: Fujisawa, T., Takenaka, S., Maekawa, L. et al. Pathophysiological significance of impaired KAT7-dependent histone H3K14 acetylation during zinc deficiency. Nat Commun 17, 1710 (2026). https://doi.org/10.1038/s41467-026-69476-z
Mots-clés: carence en zinc, épigénétique, stéatose hépatique, acétylation des histones, transporteurs du zinc