Clear Sky Science · fr
Aperçus mécanistiques sur la thermodynamique hors d’équilibre de la fixation de l’azote via la cavitation acoustique
Transformer l’air en engrais utile grâce au son
L’azote de l’air est essentiel pour les engrais et la production alimentaire, mais convertir ce gaz réticent en formes utilisables exige généralement d’immenses usines, des températures extrêmes et de fortes pressions. Cette étude explore une approche très différente : utiliser des ondes sonores intenses pour créer de minuscules bulles explosant dans l’eau qui peuvent « fixer » l’azote dans des conditions loin de l’équilibre. En observant et en modélisant ce qui se passe à l’intérieur de ces points chauds fugitifs, les chercheurs montrent comment des bulles entraînées par le son pourraient offrir une nouvelle voie pour fabriquer des composés azotés sans catalyseurs traditionnels ni réacteurs gigantesques.
Pourquoi la fixation de l’azote est si difficile
Notre atmosphère est majoritairement composée de diazote, mais ses atomes sont soudés par l’une des liaisons chimiques les plus fortes de la nature. Briser cette liaison de manière efficace explique pourquoi le procédé Haber–Bosch repose sur des équipements puissants et consomme d’énormes quantités d’énergie dans le monde entier. Les méthodes conventionnelles doivent trouver un compromis délicat : des températures suffisamment élevées pour activer l’azote, sans être si élevées que les produits souhaités se décomposent ou que l’équilibre poussé la réaction en arrière. Cet article soutient que plutôt que de maintenir une température constante, il peut être plus efficace de la dépasser brièvement — en utilisant des bouffées ultrarapides de chaleur — puis de refroidir si rapidement que les produits utiles sont piégés avant de se décomposer.
Utiliser les ultrasons pour créer de minuscules chambres de réaction
Lorsque des ultrasons puissants traversent l’eau, ils génèrent des bulles de gaz microscopiques qui croissent puis s’effondrent violemment, un phénomène connu sous le nom de cavitation acoustique. Chaque bulle effondrante se comporte comme un réacteur miniature et éphémère. En l’espace de milliardièmes de seconde, le gaz à l’intérieur est comprimé à des températures supérieures à 5000 kelvins puis refroidi à nouveau à des vitesses proches de 1012 kelvins par seconde. Dans ces conditions, les molécules d’azote à l’intérieur de la bulle peuvent se dissocier en fragments réactifs, qui se combinent ensuite avec des fragments issus de l’oxygène, de l’hydrogène ou de l’eau pour former du nitrite, du nitrate ou de l’ammonium. Les nouveaux produits sont alors projetés dans le liquide environnant, où ils s’accumulent au fil du temps tandis que se forment et s’effondrent de nouvelles générations de bulles. 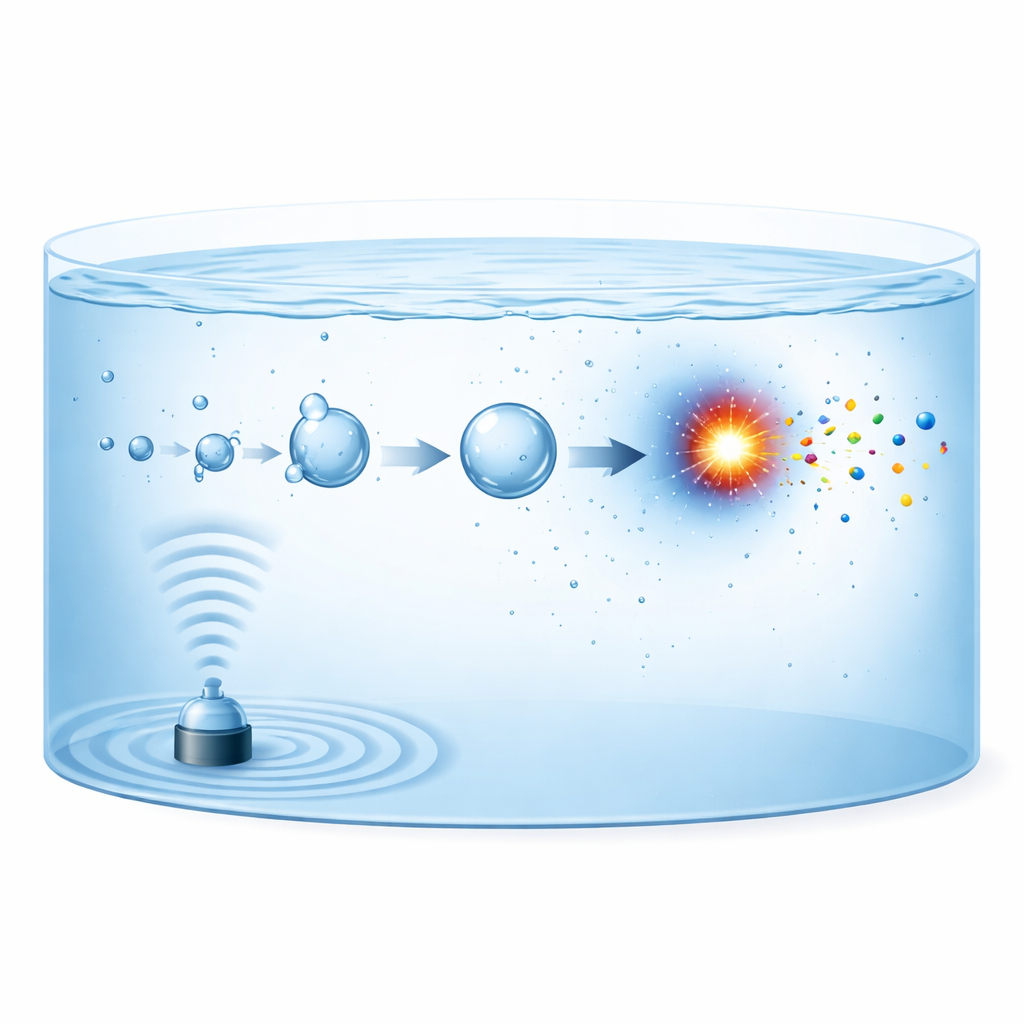
Accorder les bulles pour choisir entre différents produits
L’équipe a fait varier systématiquement les gaz alimentant les bulles (azote plus oxygène ou hydrogène), l’amplitude et la fréquence des ultrasons, ainsi que la présence de particules solides qui favorisent la formation de bulles. Avec des mélanges azote–oxygène, le système produisait principalement des produits oxydés tels que nitrite et nitrate ; avec des mélanges azote–hydrogène, il favorisait l’ammonium. De petites quantités de particules de talc ont joué le rôle de « graines » de bulles, abaissant le seuil de cavitation et rendant les réactions plus reproductibles. En ajustant la pression acoustique et le temps de réaction, les chercheurs ont pu déplacer l’équilibre entre nitrite et nitrate, montrant qu’une partie de la chimie se déroule à l’intérieur de la bulle effondrante et qu’une partie se poursuit dans l’eau environnante alors que des fragments réactifs convertissent lentement le nitrite en nitrate plus oxydé.
Plonger au cœur de l’impulsion thermique à l’échelle nanométrique
Pour comprendre pourquoi des conditions aussi extrêmes et fugaces produisent néanmoins des produits stables, les auteurs ont combiné mesures, simulations détaillées et calculs chimico-quantiques. Ceux-ci montrent qu’à très haute température, l’azote peut se scinder directement en phase gazeuse, ouvrant des voies normalement inaccessibles. Mais les mêmes calculs révèlent aussi que maintenir le gaz chaud rendrait les produits finaux instables. La clé réside dans la trempe rapide : le pic de température de la bulle active l’azote, puis le refroidissement quasi instantané stabilise les fragments intermédiaires et les molécules formées comme l’ammoniac et l’acide nitreux avant qu’elles ne puissent se décomposer ou revenir à l’azote. La modélisation de bulles individuelles, notamment lorsqu’elles sont dopées à l’argon pour augmenter les températures d’effondrement, a confirmé que des températures de pointe plus élevées modifient la répartition des produits et augmentent les taux globaux de fixation. 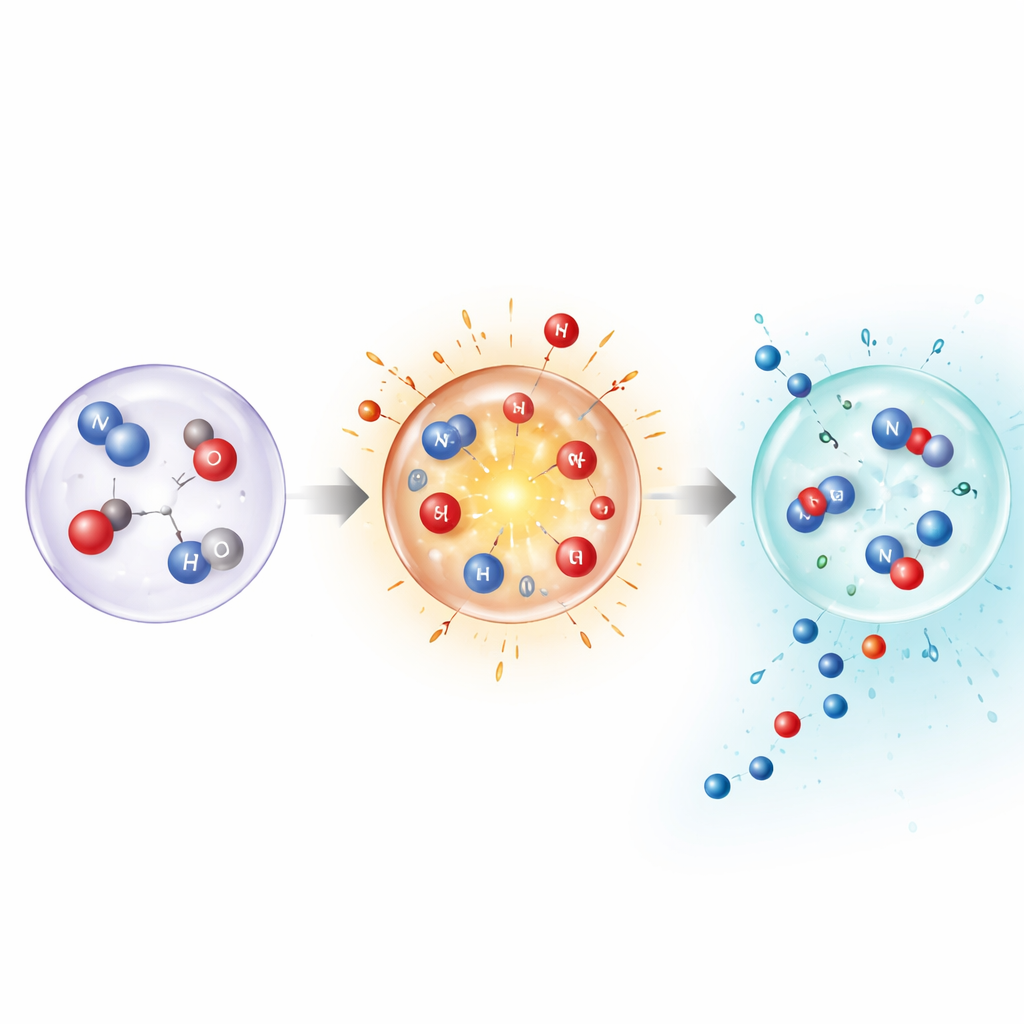
Consommation d’énergie et perspectives
Bien que cette méthode pilotée par le son ne soit pas encore aussi économe en énergie que les meilleurs procédés industriels, ses performances rivalisent déjà avec des approches historiques à arc électrique et certains systèmes plasma modernes, tout en opérant dans des conditions ambiantes et sans catalyseurs solides. Fait important, les mêmes événements de cavitation fendent aussi l’eau, libérant hydrogène, oxygène et peroxyde d’hydrogène — des sous-produits riches en énergie qui pourraient être récupérés parallèlement à l’azote fixé. Les auteurs soulignent que leur dispositif est conçu pour révéler des mécanismes plutôt que pour maximiser la production, mais le travail établit la cavitation acoustique comme une voie distincte de fixation de l’azote en exploitant des cycles thermiques extrêmement rapides dans des bulles microscopiques. Pour les non-spécialistes, la conclusion est que le son contrôlé avec soin peut transformer l’eau et l’air ordinaires en ingrédients d’engrais via une série de petites explosions invisibles, ouvrant la voie à des méthodes plus vertes et plus flexibles pour produire à l’avenir des composés azotés essentiels.
Citation: Pan, X., Preso, D.B., Liu, Q. et al. Mechanistic insights into the non-equilibrium thermodynamics of nitrogen fixation via acoustic cavitation. Nat Commun 17, 2682 (2026). https://doi.org/10.1038/s41467-026-69466-1
Mots-clés: fixation de l’azote, cavitation acoustique, sonochimie, production d’engrais, chimie par ultrasons