Clear Sky Science · fr
Plasmodium ARK1 régule la formation du fuseau lors d’une mitose atypique et forme un complexe des passagers chromosomiques divergent
Comment les parasites du paludisme se divisent d’une manière surprenante
Les parasites du paludisme passent leur vie à aller et venir entre humains et moustiques, se multipliant rapidement dans le sang et dans l’intestin du moustique. Pour ce faire, ils divisent leurs cellules d’une manière qui diffère fortement des schémas classiques de la division cellulaire humaine. Cette étude révèle comment une enzyme clé, appelée ARK1, contrôle ces processus de division inhabituels et pourquoi elle pourrait constituer une cible intéressante pour de nouveaux antipaludiques.
Deux manières très différentes de se multiplier
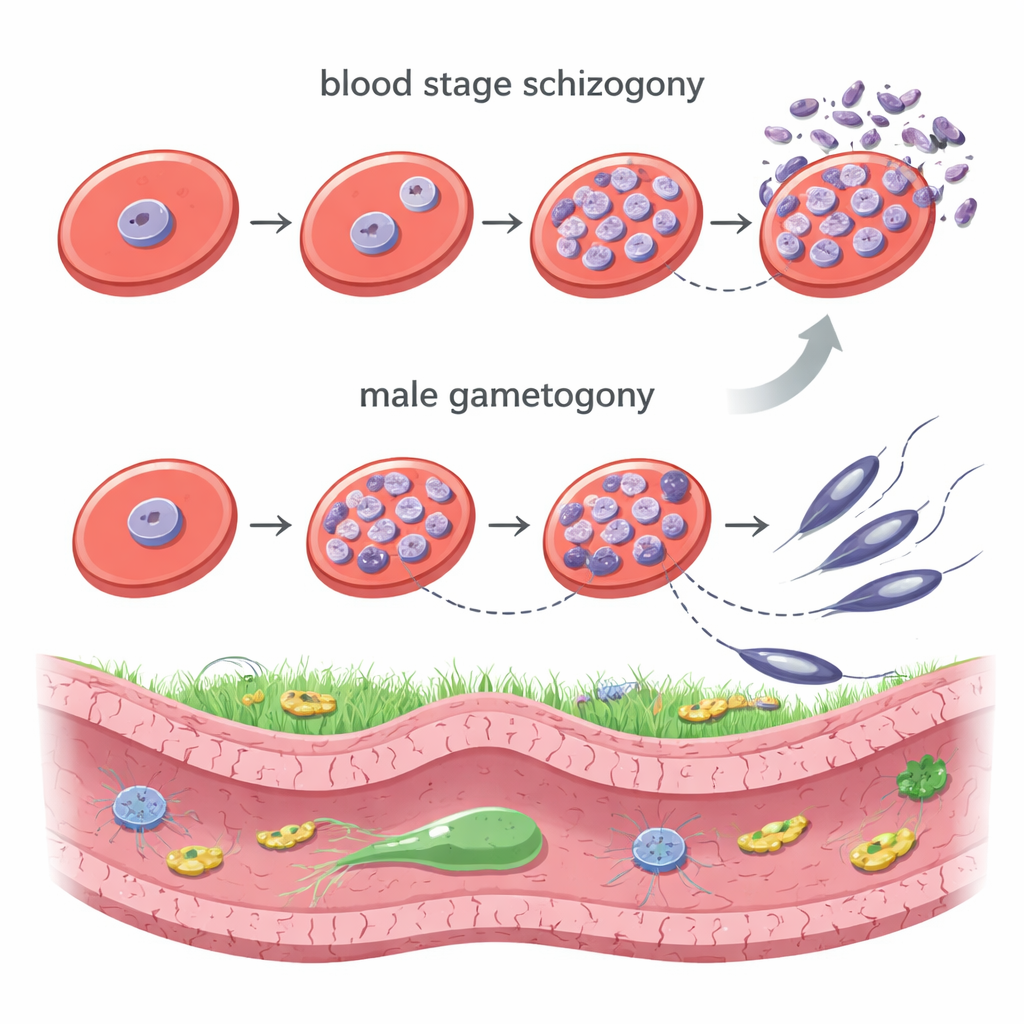
Les parasites du genre Plasmodium utilisent au moins deux styles de division cellulaire remarquablement différents. À l’intérieur des globules rouges humains, ils subissent la schizogonie : un noyau parasitaire se divise plusieurs fois sans que la cellule ne se sépare, créant une « poche » contenant de nombreux noyaux qui bourgeonnent ensuite pour former des dizaines de nouveaux parasites. Dans le moustique, les cellules sexuelles mâles traversent une division ultrarapide appelée gamétogonie mâle, où l’ADN est répliqué trois fois en quelques minutes seulement pour former un génome octaploïde, puis emballé rapidement en huit cellules flagellées semblables à des spermatozoïdes. Les deux formes de division se déroulent à l’intérieur d’un noyau intact et reposent sur une structure spécialisée connue sous le nom de centre organisateur de microtubules (MTOC), qui assemble les fins fibres qui séparent les chromosomes.
Un interrupteur maître pour construire la machinerie de division
Les auteurs se sont concentrés sur une enzyme appelée kinase apparentée à Aurora 1 (ARK1), membre d’une famille de protéines qui, chez de nombreux organismes, agit comme un interrupteur maître pour la division cellulaire. À l’aide de manipulations génétiques dans deux espèces de paludisme — Plasmodium falciparum, qui infecte les humains, et Plasmodium berghei, qui infecte les rongeurs — ils ont marqué ARK1 par des traceurs fluorescents pour observer sa localisation, puis l’ont partiellement ou complètement supprimée pour voir ce qui dysfonctionne. L’imagerie en direct haute résolution et la microscopie d’expansion ont montré qu’ARK1 n’apparaît que lorsque les noyaux sont en cours de division. Il se concentre dans la partie interne du MTOC et le long du fuseau mitotique — le faisceau de fibres qui sépare les chromosomes — plutôt que d’être diffus dans toute la cellule.
Que se passe-t-il lorsque ARK1 est éliminée
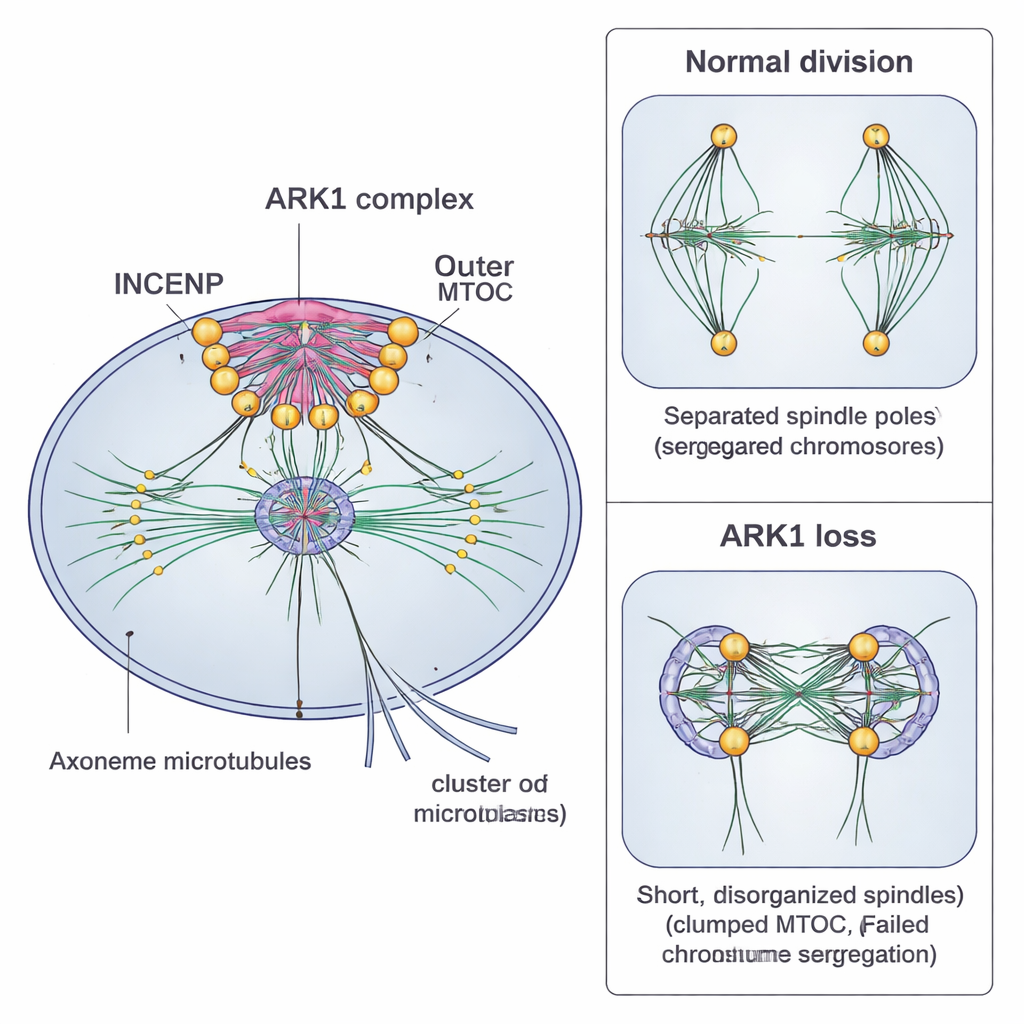
Lorsque les chercheurs ont interrompu ARK1 dans des parasites en phase sanguine, le développement initial s’est poursuivi, mais des problèmes sont apparus lorsque les parasites ont tenté de diviser leurs noyaux et de se segmenter en cellules filles individuelles. Les fuseaux étaient rabougris ou désorganisés, les noyaux ne se séparaient pas correctement, et les amas de futurs parasites-filles restaient souvent fusionnés ou déformés. Au microscope, des structures de surface et membranaires essentielles qui devraient former des grappes nettes de nouveaux parasites apparaissaient au lieu de cela irrégulières et chaotiques. Le nombre de parasites a diminué fortement lors du cycle infectieux suivant, montrant qu’ARK1 est nécessaire à une croissance efficace dans le sang.
Bloquer la transmission par le moustique
L’équipe a également réduit les niveaux d’ARK1 pendant le développement sexuel dans le moustique. Chez les gamétocytes mâles, qui produisent normalement des cellules flagellées en environ 15 minutes après activation, la réduction d’ARK1 a provoqué plusieurs échecs simultanés. Les parties interne et externe du MTOC se sont agglomérées au lieu de se séparer, les fuseaux sont restés courts, et les longs axonèmes en forme de fouet qui assurent le mouvement étaient mal formés. En conséquence, très peu de gamètes mâles fonctionnels ont émergé, moins d’œufs fécondés ont évolué en ookinetes et en oocystes, et beaucoup moins de sporozoïtes infectieux ont atteint les glandes salivaires du moustique. La plupart des moustiques portant ces parasites affaiblis n’ont pas réussi à transmettre l’infection à de nouveaux souris.
Un complexe de contrôle réorganisé et de nouvelles opportunités thérapeutiques
Pour comprendre comment ARK1 est guidée, les chercheurs l’ont isolée à partir des parasites et ont identifié des protéines partenaires par spectrométrie de masse. Ils ont découvert qu’ARK1 forme le noyau d’un « complexe des passagers chromosomiques » inhabituel avec deux protéines d’échafaudage, nommées INCENP-A et INCENP-B. Chez de nombreux autres organismes, ce complexe inclut également deux sous-unités supplémentaires, Survivin et Borealine, qui aident à le cibler sur les chromosomes. Plasmodium et les parasites apparentés semblent avoir perdu ces composants et ont à la place dupliqué l’échafaudage INCENP, réorganisant le complexe autour d’ARK1 et du MTOC interne. Des analyses comparatives de génomes suggèrent que cette réorganisation est survenue à plusieurs reprises dans différentes lignées de parasites, soulignant la grande plasticité de l’outillage de la division cellulaire au cours de l’évolution.
Pourquoi cela compte pour la lutte contre le paludisme
Pour le non-spécialiste, le message clé est que les parasites du paludisme se divisent en utilisant des systèmes de contrôle à la fois essentiels et différents de ceux des humains. ARK1 se trouve au cœur de cette machinerie de division spécifique aux parasites, coordonnant la séparation des chromosomes et la production des stades infectieux chez l’homme comme chez le moustique. Parce que bloquer ARK1 perturbe la croissance des parasites dans le sang et freine presque totalement la transmission via les moustiques, des médicaments ciblant le complexe ARK1–INCENP pourraient, en principe, agir à plusieurs stades du cycle de vie. Cela fait d’ARK1 un candidat prometteur pour de futures stratégies antipaludiques visant non seulement à traiter la maladie mais aussi à réduire sa propagation.
Citation: Nagar, A., Yanase, R., Zeeshan, M. et al. Plasmodium ARK1 regulates spindle formation during atypical mitosis and forms a divergent chromosomal passenger complex. Nat Commun 17, 1598 (2026). https://doi.org/10.1038/s41467-026-69460-7
Mots-clés: division cellulaire du paludisme, kinase Aurora ARK1, mitose de Plasmodium, complexe des passagers chromosomiques, cibles médicamenteuses antipaludiques