Clear Sky Science · fr
Ciblage triple de STING, TGF-β et PD-L1 renforçant la signalisation CXCL16–CXCR6 pour une réponse antitumorale puissante
Transformer les tumeurs froides en tumeurs chaudes
L’immunothérapie contre le cancer a transformé le traitement de certains patients, mais de nombreuses tumeurs résistent encore à ces médicaments puissants. Cette étude examine pourquoi certains cancers échappent aux inhibiteurs de points de contrôle modernes et propose une attaque plus intelligente en trois volets qui réveille les défenses de l’organisme, attire des lymphocytes T cytotoxiques d’élite et les maintient actifs directement au sein de la tumeur.
Pourquoi les immunothérapies actuelles ne suffisent pas
La plupart des immunothérapies approuvées ciblent un seul frein des cellules immunitaires, comme la voie PD-1/PD-L1. Une classe plus récente de médicaments cherche à aller plus loin en bloquant aussi le TGF-β, une molécule qui supprime fortement l’immunité dans les cancers avancés. Un de ces médicaments, YM101, combine le blocage du TGF-β et de PD-L1 dans un seul anticorps et a montré des résultats prometteurs chez la souris. Mais même chez des animaux génétiquement identiques, certaines tumeurs régressaient à peine. En comparant tumeurs sensibles et résistantes, les chercheurs ont trouvé que le succès du traitement s’accompagnait d’une forte activation de l’immunité « innée », en particulier du signalement via une voie appelée STING, qui détecte l’ADN anormal et déclenche des signaux d’alerte de type antiviral.
Ajouter un troisième levier : la voie STING
Soupçonnant qu’une activation innée insuffisante était la pièce manquante, l’équipe a combiné YM101 avec un agoniste oral de STING appelé MSA-2 dans plusieurs modèles tumoraux murins, y compris des tumeurs « froides » difficilement traitables. L’approche triple — activation de STING plus blocage de TGF-β et PD-L1 — a réduit les tumeurs plus efficacement, prolongé la survie et souvent protégé les souris contre la rechute après une nouvelle mise en contact, indiquant une mémoire immunitaire durable. Ceci a surpassé l’association plus conventionnelle d’un agoniste STING avec un blocage de PD-L1 seul, et a même renforcé la thérapie par agoniste STING lorsque seul le TGF-β était bloqué, révélant que le TGF-β agit lui-même comme un frein majeur à l’immunité conduite par STING. 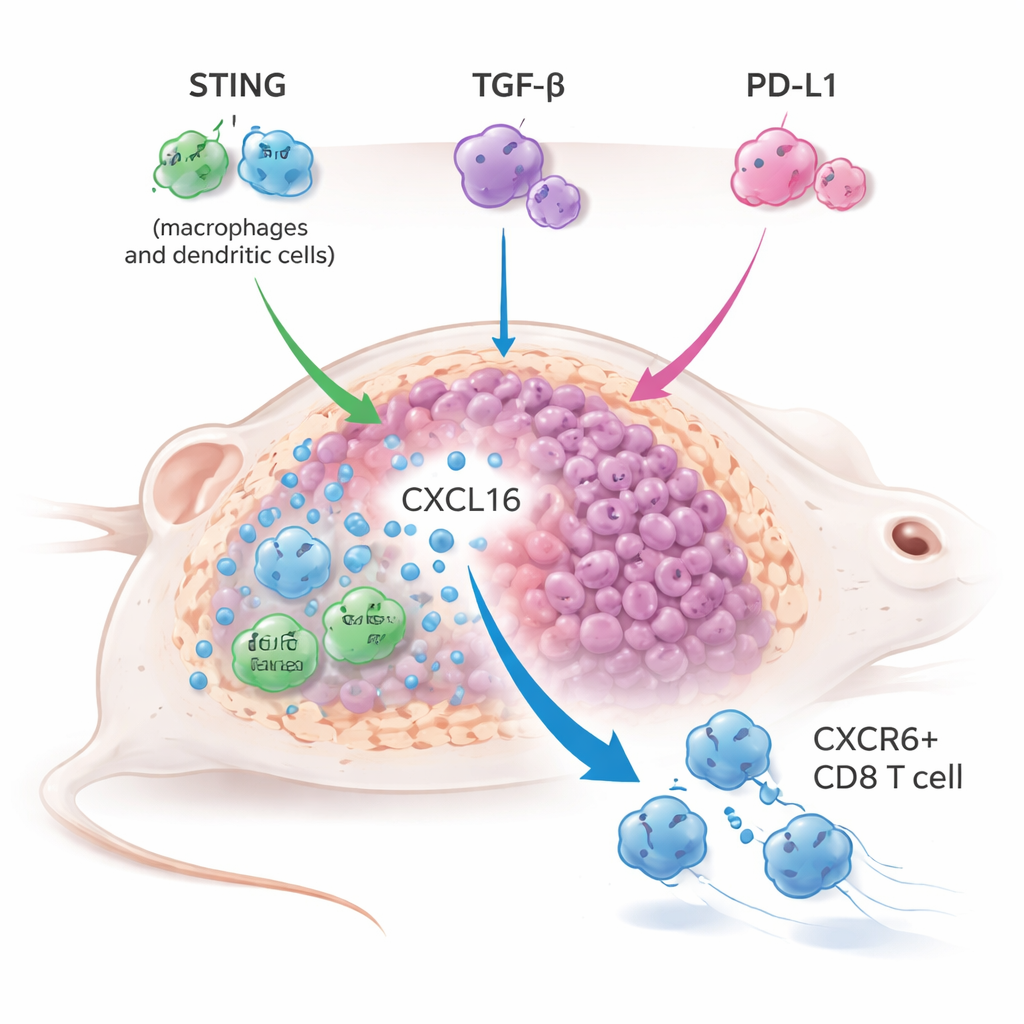
Recruter une escouade spécialisée de tueurs
Pour comprendre comment cette stratégie triple fonctionnait, les chercheurs ont utilisé le séquençage ARN unicellulaire et un profilage immunitaire détaillé des tumeurs traitées. Ils ont découvert une expansion marquée d’un sous-ensemble de lymphocytes T cytotoxiques caractérisé par le récepteur CXCR6. Ces cellules CD8+ CXCR6+ étaient fortement armées, exprimant des niveaux élevés de granzymes, de perforine et de molécules inflammatoires, et présentaient de forts signes d’activation et de prolifération. Parallèlement, les macrophages et cellules dendritiques associés à la tumeur ont augmenté la production d’une chimiokine appelée CXCL16, qui se lie à CXCR6 et aide à retenir ces lymphocytes T dans la tumeur. Lorsque l’axe CXCL16–CXCR6 était rompu — soit en bloquant CXCL16 soit en supprimant génétiquement CXCR6 dans les lymphocytes T — le traitement combiné perdait en grande partie son efficacité antitumorale, prouvant que cet axe est central au succès de la thérapie.
Comment la cascade de signalisation est activée
En approfondissant, l’équipe a cherché comment l’activation de STING et le blocage du TGF-β renforcent conjointement CXCL16. Dans des cellules immunitaires humaines et murines, les agonistes de STING augmentaient fortement CXCL16 et la cytokine antivirale IFN‑β, tandis que l’ajout de TGF-β réduisait nettement les deux. Les chercheurs ont montré que STING déclenche la signalisation IFN‑I, qui active le facteur de transcription STAT1 ; STAT1 se lie alors directement à la région régulatrice du gène CXCL16, l’activant. Le TGF-β perturbe cette chaîne en interférant avec une étape clé du signalement STING, probablement via une protéine nommée HDAC4 et des espèces réactives de l’oxygène, atténuant l’activation d’IRF3 et la production en aval d’IFN‑β et de CXCL16. Le blocage du TGF-β supprime ce frein, permettant aux agonistes STING d’enclencher pleinement la voie STAT1–CXCL16 dans les cellules myéloïdes et ainsi d’alimenter les cellules T CXCR6+ avec les signaux nécessaires pour rester et combattre dans la tumeur.
Concevoir un médicament de précision unique
Pour rendre ce schéma complexe plus pratique et ciblé sur la tumeur, les chercheurs ont conçu un seul « conjugué anticorps‑stimulant immunitaire » appelé Y101S. Cette molécule combine l’anticorps double bloquant TGF-β/PD-L1 avec un agoniste STING attaché par un lien clivable. Y101S se dirige vers les cellules myéloïdes PD-L1–positives dans la tumeur, est internalisé, puis libère le médicament STING à l’intérieur de ces cellules. Dans plusieurs cancers murins, Y101S a égalé ou dépassé l’efficacité de l’administration de YM101 plus une forte dose d’agoniste STING libre, bien qu’il ne transporte qu’une fraction minime de cette dose STING. Il a augmenté les macrophages et cellules dendritiques CXCL16+, expansé les cellules CD8+ CXCR6+, induit une mémoire immunitaire durable et concentré les signaux inflammatoires dans les tumeurs tout en épargnant les organes sains, avec un profil de sécurité favorable chez la souris. 
Ce que cela signifie pour les traitements futurs du cancer
Pour les non‑spécialistes, le message clé est que combattre le cancer en n’activant qu’un ou deux interrupteurs immunitaires peut ne pas suffire — surtout lorsque les tumeurs étouffent activement les systèmes d’alarme précoces. Ce travail montre que combiner l’activation de STING avec le blocage du TGF-β et de PD-L1 peut reconfigurer l’environnement tumoral, attirer et maintenir puissamment un groupe spécialisé de lymphocytes T cytotoxiques, et obtenir des réponses plus profondes et durables dans des modèles précliniques. L’anticorps‑médicament à ciblage triple Y101S incarne cette stratégie en un seul médicament ciblé et offre une feuille de route pour les immunothérapies de nouvelle génération visant les tumeurs qui résistent actuellement aux inhibiteurs de points de contrôle standard.
Citation: Yi, M., Li, T., Gu, Y. et al. Triple targeting of STING, TGF-β, and PD-L1 boosts CXCL16–CXCR6 signaling for potent antitumor response. Nat Commun 17, 1441 (2026). https://doi.org/10.1038/s41467-026-69456-3
Mots-clés: immunothérapie du cancer, voie STING, blocage du TGF-bêta, anticorps anti–PD-L1, CXCL16 CXCR6 cellules T