Clear Sky Science · fr
Une sous-population de cellules mésenchymateuses exprimant Fcer1g induite par les macrophages contribue à la fibrose post‑lésion
Pourquoi certaines blessures laissent des cicatrices durables
La plupart d’entre nous portent des cicatrices de coupures, d’opérations ou d’accidents. Pourquoi certaines plaies cicatrisent sans laisser de trace tandis que d’autres forment des marques épaisses et surélevées reste une énigme. Cette étude examine la question en se concentrant sur les cellules qui reconstruisent la peau endommagée. Les chercheurs mettent au jour un groupe jusqu’ici méconnu de cellules productrices de cicatrices qui s’activent tôt après la blessure, sous l’influence de cellules immunitaires appelées macrophages. Comprendre ce partenariat caché pourrait indiquer des voies thérapeutiques permettant à la peau de cicatriser avec moins de cicatrices tout en fermant efficacement les plaies. 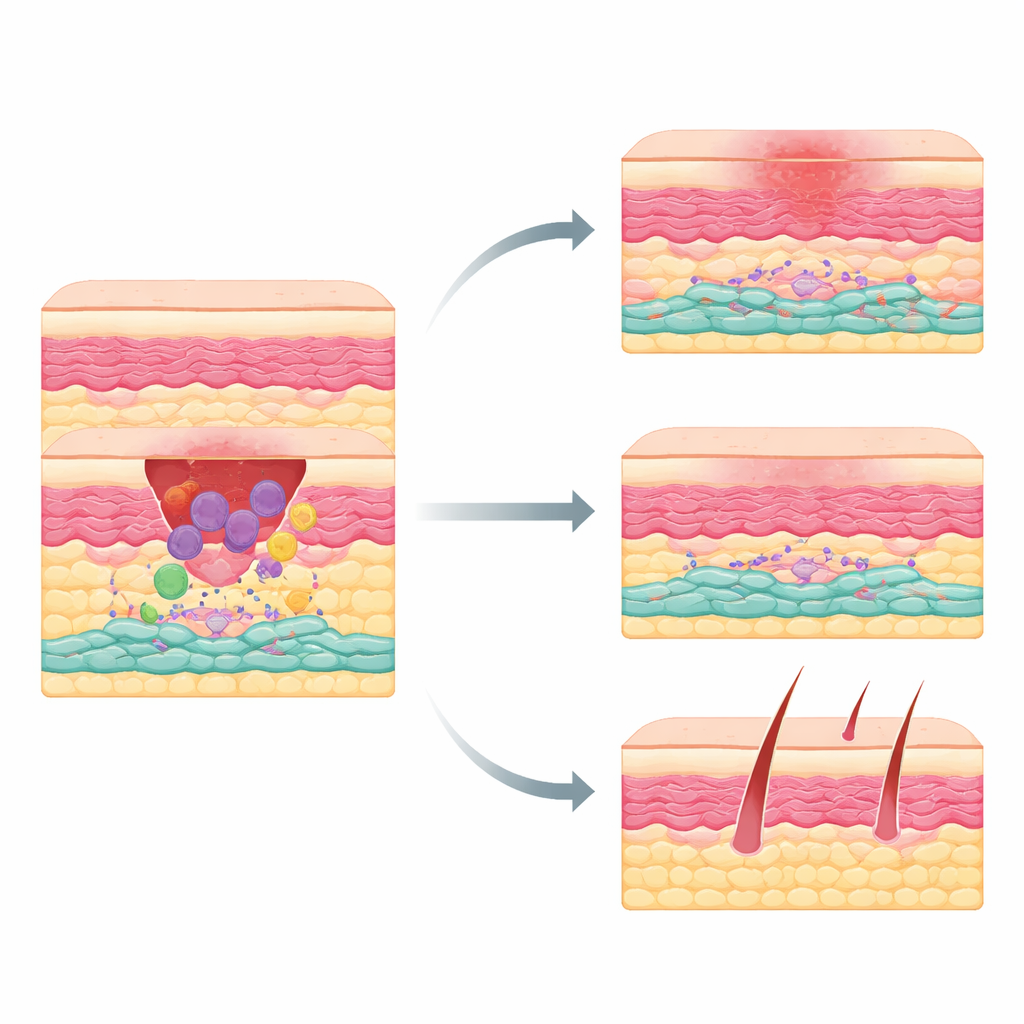
Les acteurs discrets au cœur de la peau qui guérit
Lorsqu’on coupe la peau, l’organisme suit une séquence orchestrée : d’abord une inflammation pour nettoyer les dégâts, puis la formation de tissu, enfin le remodelage. Les macrophages arrivent tôt pour éliminer les débris et émettre des signaux chimiques qui mobilisent d’autres cellules. Parmi les répondants se trouvent des cellules mésenchymateuses — des bâtisseurs de type fibroblastique qui déposent du collagène et d’autres matériaux de soutien. Ces bâtisseurs ne sont pas tous identiques : certains favorisent la régénération, d’autres ont tendance à surproduire du tissu cicatriciel. Jusqu’à présent, les scientifiques n’avaient pas clairement identifié quelles cellules mésenchymateuses de la peau adulte étaient principalement responsables des cicatrices épaisses.
Des cellules immunitaires qui préparent discrètement le terrain à la cicatrisation excessive
Pour explorer comment les macrophages influencent la formation de cicatrices, l’équipe a utilisé des souris dont les macrophages peuvent être éliminés sélectivement pendant les premiers jours après la blessure. Lorsque ces macrophages précoces ont été supprimés, les plaies se refermaient toujours mais formaient des cicatrices bien plus petites, avec un collagène moins dense. Le séquençage ARN unicellulaire — une méthode pour profiler l’activité génique cellule par cellule — a montré que la plupart des sous-groupes mésenchymateux restaient inchangés en l’absence de macrophages. Une exception ressortait : un sous-ensemble distinct de cellules mésenchymateuses PDGFRα‑positives qui activait un gène appelé Fcer1g. Ce sous‑ensemble a quasiment disparu lorsque les macrophages manquaient, suggérant que les macrophages sont nécessaires à la création ou au maintien de ces cellules.
Une population cellulaire prolifique et promotrice de cicatrices
Des expériences supplémentaires ont cartographié où et quand ces cellules mésenchymateuses Fcer1g‑positives apparaissent. Dans la peau non blessée elles étaient rares, mais après la lésion elles se sont rapidement étendues, d’abord autour des bords de la plaie puis en se concentrant dans le lit de la plaie, où elles représentaient la majorité des cellules PDGFRα‑positives au septième jour. Ces cellules se divisaient plus rapidement que les autres mésenchymateuses et montraient une faible migration, indiquant que leur augmentation est alimentée par la prolifération locale. Quand les chercheurs ont utilisé un système génétique astucieux pour éliminer sélectivement les cellules exprimant à la fois PDGFRα et Fcer1g, la fermeture de la plaie s’est déroulée normalement — mais les cicatrices ont diminué de plus de 20 %, la teneur en collagène a chuté d’environ 30 % et le réseau de collagène de la peau réparée ressemblait davantage à celui d’une peau non blessée. Les follicules pileux étaient plus nombreux dans ces plaies privées de ces cellules, suggérant une cicatrisation plus régénérative. 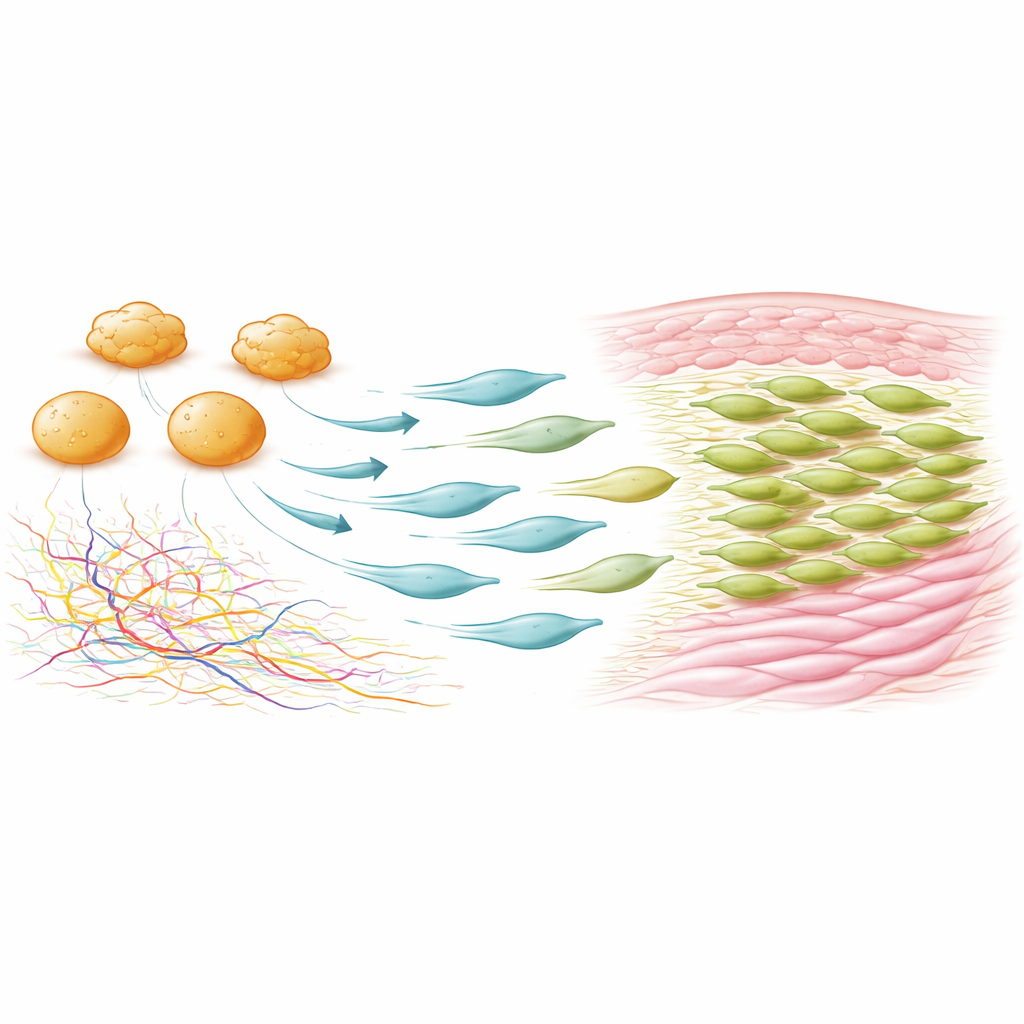
Comment les macrophages signalent aux bâtisseurs de sur‑cicatriser
Pour comprendre comment les macrophages déclenchent cet état propice aux cicatrices, l’équipe a analysé les voies de communication probables entre types cellulaires. Un candidat majeur était la fibronectine, une protéine adhésive qui fait partie de la matrice temporaire des plaies fraîches. Les macrophages dans les plaies précoces étaient une source importante de fibronectine, et ses niveaux ont fortement diminué lorsque les macrophages ont été éliminés. Chez des souris génétiquement modifiées pour ne pas produire une forme de fibronectine associée aux plaies (la forme EDA), les cellules mésenchymateuses Fcer1g‑positives étaient fortement réduites et les cicatrices étaient plus légères. En culture, le contact direct avec des macrophages suffisait à convertir des fibroblastes dermiques ordinaires en cellules PDGFRα‑positives et Fcer1g‑positives, soulignant que les macrophages peuvent directement induire cet état.
Un programme cicatriciel commun chez la souris et l’homme
Pour vérifier si ce type cellulaire est pertinent chez l’humain, les chercheurs ont réexaminé des jeux de données existants sur la peau humaine blessée, aux résolutions unicellulaire et tissulaire. Ils ont retrouvé un sous‑groupe mésenchymateux correspondant dans les plaies humaines exprimant FCER1G et un profil génique similaire, culminant environ une semaine après la blessure — le même calendrier que chez la souris. Sur plus d’une centaine d’échantillons humains comprenant peau normale, plaies aiguës, plaies chroniques et cicatrices surélevées, le programme génique lié à FCER1G séparait nettement les tissus blessés et cicatrisés de la peau non lésée et était le plus fort tôt après la blessure. Cette similarité inter‑espèces suggère que l’état cellulaire récemment défini est un moteur évolutivement conservé de la réparation fibrotique.
Vers une cicatrisation plus douce et moins marquée
Pris ensemble, les résultats dévoilent une chaîne d’événements jusque‑là sous‑estimée : les macrophages arrivant précocement enrichissent la plaie en fibronectine, la fibronectine aide à convertir les cellules mésenchymateuses locales en un état FCER1G‑positif à forte prolifération, et ce sous‑ensemble spécialisé dépose ensuite un excès de collagène qui devient tissu cicatriciel. Parce que l’élimination de ces cellules chez la souris a réduit la cicatrisation sans ralentir la fermeture des plaies, elles représentent une cible attrayante pour de futures thérapies. Des médicaments ou des produits biologiques interrompant les signaux qui créent ou maintiennent cet état cellulaire — par exemple en modulant le comportement des macrophages ou l’environnement en fibronectine — pourraient un jour aider les patients à cicatriser leurs blessures cutanées avec des cicatrices minimales et moins visibles.
Citation: Ma, X., Wang, E., Puviindran, V. et al. A macrophage-induced subpopulation of mesenchymal cells expressing Fcer1g contributes to wound-induced fibrosis. Nat Commun 17, 2686 (2026). https://doi.org/10.1038/s41467-026-69449-2
Mots-clés: guérison des plaies, fibrose cutanée, macrophages, fibroblastes, formation de cicatrices