Clear Sky Science · fr
Coopérativité positive entre les domaines de liaison à RAS et riches en cystéine régule la cinétique d’ancrage de RAF à la membrane via la reconnexion latérale
Pourquoi cette minuscule danse moléculaire compte
À l’intérieur de nos cellules, les décisions vitales concernant la croissance, la division et la survie se prennent souvent à la surface de la membrane cellulaire. Un acteur clé de ces décisions est une protéine appelée RAF, qui relaie les signaux de croissance et dont le fonctionnement est fréquemment détourné dans le cancer. Cette étude révèle, avec un niveau de détail cinétique sans précédent, comment RAF se fixe à la membrane cellulaire, combien de temps il y reste, et pourquoi des zones encombrées d’une autre protéine, RAS, peuvent maintenir RAF actif plus longtemps qu’on ne l’attendrait.
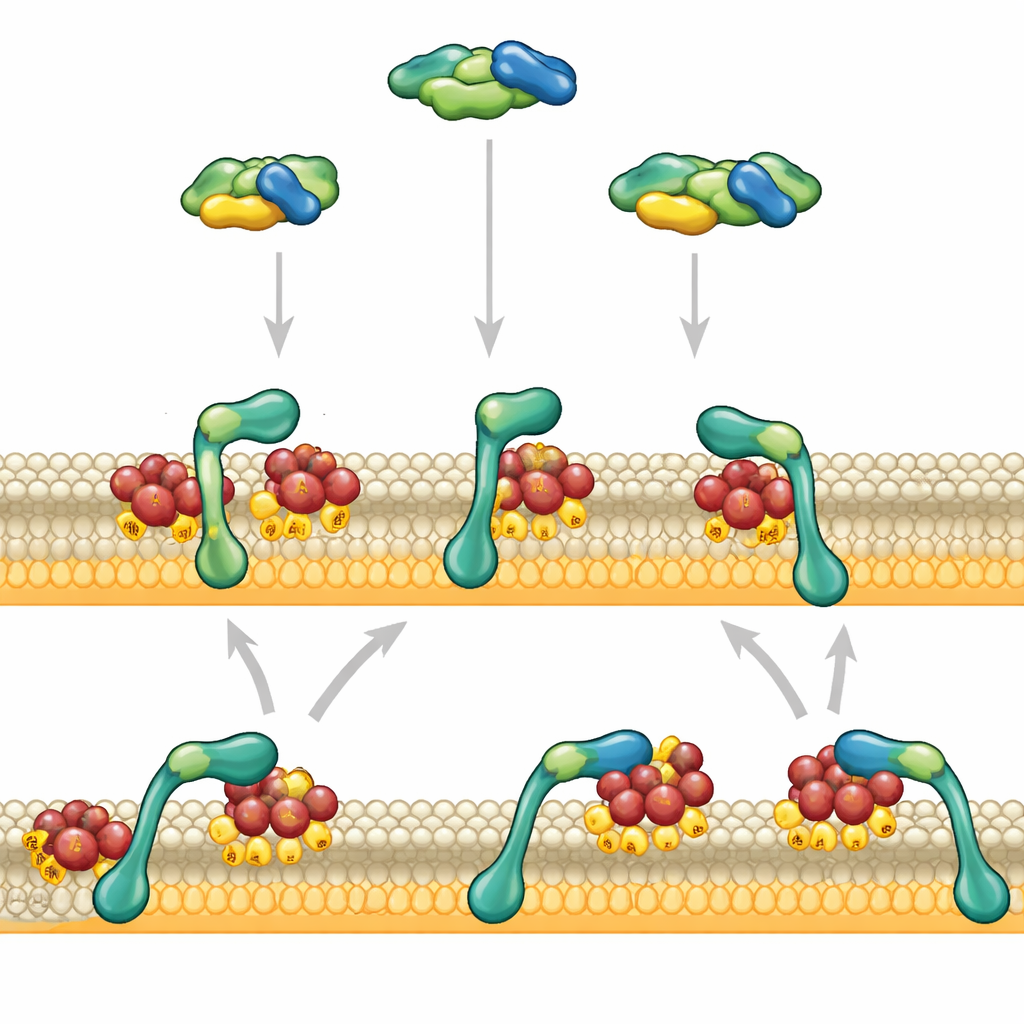
Des signaux qui se rencontrent à la surface cellulaire
RAF agit dans un axe de signalisation majeur appelé voie MAPK, qui relie des signaux externes tels que les facteurs de croissance à des changements dans l’activité génétique. À l’état de repos, RAF circule à l’intérieur de la cellule dans une conformation repliée et auto-inhibée. Il n’est activé que lorsqu’il rencontre RAS, un petit interrupteur moléculaire ancré à la face interne de la membrane cellulaire. RAS doit être dans son état « on » et inséré dans le bon type de lipides pour que RAF soit recruté et activé. Parce que les molécules de RAF sont relativement rares par rapport à de nombreux autres composants de signalisation, la manière précise dont elles s’attachent à la membrane et évitent un relâchement prématuré influence fortement si une cellule répond faiblement ou fortement à un signal de croissance.
Deux mains pour saisir la membrane
Les auteurs se sont concentrés sur deux régions à l’extrémité avant de RAF : une qui saisit RAS et une autre qui préfère les lipides chargés négativement de la membrane. En utilisant des membranes artificielles et des protéines purifiées, ils ont observé des fragments individuels de RAF se liant à des surfaces décorées de RAS à l’aide d’une microscopie avancée. Quand la région de liaison à RAS agissait seule, elle touchait brièvement la membrane et se détachait en environ une seconde. La région aimant les lipides, isolément, s’accrochait à peine. Mais lorsque ces deux régions étaient reliées, leur comportement changeait radicalement : RAF s’attachait alors fortement et restait sur la membrane pendant des dizaines de secondes, notamment quand la membrane contenait de nombreux lipides chargés négativement similaires à ceux des cellules réelles.
Une coopération qui ralentit la sortie
Ce changement spectaculaire n’est pas dû au fait que RAF atteint la membrane plus rapidement, mais parce qu’il s’en éloigne plus lentement. D’abord, le segment de RAF qui lie RAS reconnaît RAS activé et ancre RAF à la membrane. Ce n’est qu’après cette première poignée de main que la région de liaison aux lipides s’engage pleinement avec les lipides environnants, ralentissant le mouvement latéral de RAF et l’ancrant plus fermement. Ce second contact stabilise à son tour l’interaction RAS–RAF initiale, créant une boucle de rétroaction positive entre contacts protéine–protéine et protéine–lipide. Des expériences modifiant le court linker qui relie les deux régions ont montré que leur coordination spatiale étroite est cruciale : rendre le linker plus flexible ou plus long affaiblissait la capacité de RAF à rester à la membrane.
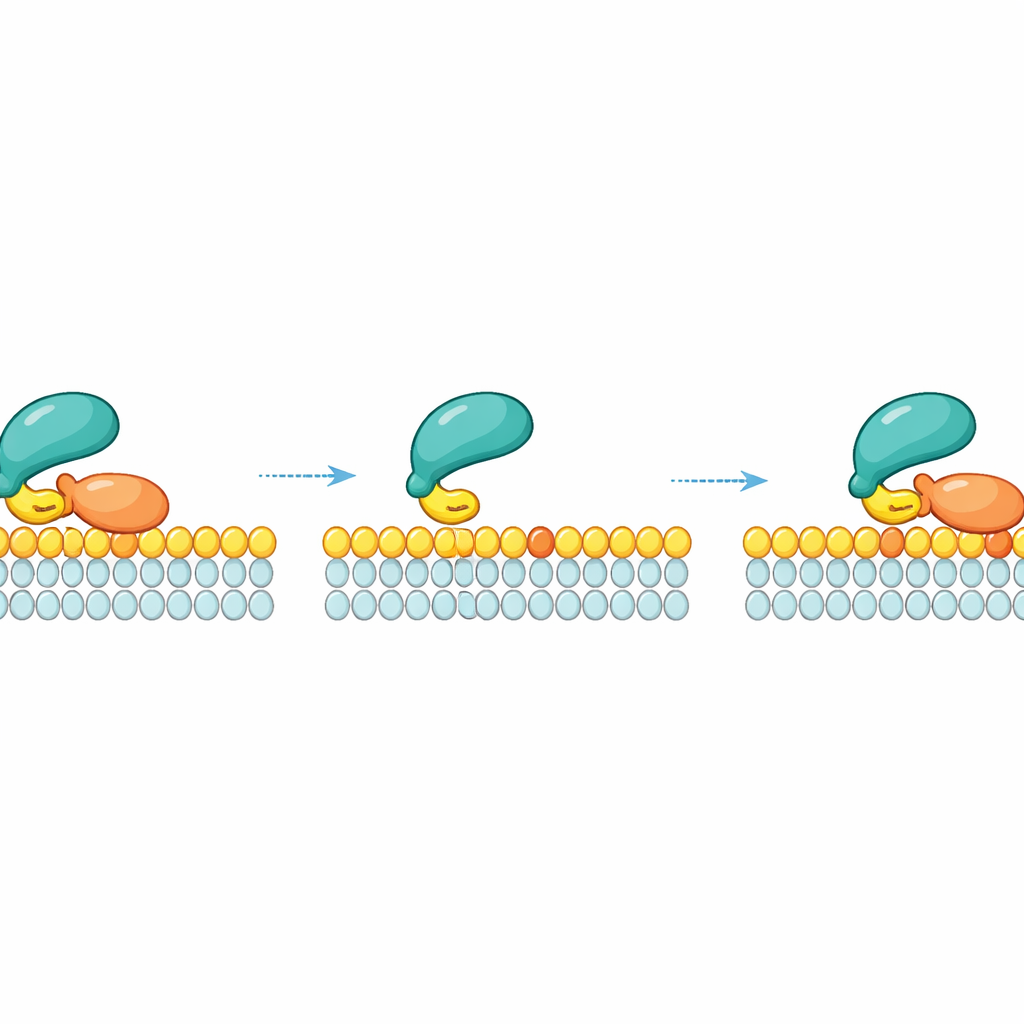
Reconnexion latérale : glisser plutôt que tomber
Un aperçu clé du travail est que RAF ne se détache pas simplement dans le fluide environnant lorsqu’il lâche une molécule de RAS donnée. Au contraire, après la libération de RAS, RAF peut rester brièvement attaché à la membrane via son faible contact lipidique et glisser latéralement. Dans cet état transitoire, il peut « reprendre » une molécule de RAS voisine sur la même zone membranaire. Cette reconnexion latérale crée un filet de sécurité cinétique : à forte densité locale de RAS—comme dans les nanoclusters où les molécules de RAS sont emballées serrées—RAF a de nombreuses occasions de se relier à nouveau à RAS avant de dériver. Mesures et simulations ont montré que plus la densité de RAS actif sur la membrane est élevée, plus RAF reste lié à la membrane longtemps grâce à ces réattachements locaux répétés.
De visites prolongées à une activation fiable
Le temps prolongé que RAF passe à la membrane a des conséquences importantes. L’activation de RAF n’est pas un événement unique mais une séquence en plusieurs étapes qui inclut des changements de conformation, l’élimination de marques inhibitrices et l’association de deux molécules de RAF en un dimère actif. L’étude suggère que seules les molécules de RAF qui résident suffisamment longtemps à la membrane peuvent accomplir cette séquence, une forme de « relecture cinétique » qui aide les cellules à éviter des activations accidentelles dues à des signaux fugaces et faibles. En révélant comment l’interaction entre la liaison à RAS, l’engagement lipidique et la reconnexion latérale fixe la durée de résidence de RAF à la membrane, le travail décrit une stratégie générale par laquelle les cellules peuvent utiliser de nombreuses interactions faibles et locales sur les membranes pour régler finement des voies de signalisation puissantes.
Citation: Jimenez Salinas, A., Tevdorashvili, K., Grim, J. et al. Positive cooperativity between RAS-binding and cysteine-rich domains regulates RAF membrane binding kinetics via lateral rebinding. Nat Commun 17, 2593 (2026). https://doi.org/10.1038/s41467-026-69437-6
Mots-clés: RAS, kinase RAF, signalisation à la membrane cellulaire, reconnexion latérale, relecture cinétique