Clear Sky Science · fr
L’absence de MDA5 retarde le vieillissement hématopoïétique en modulant l’inflammaging et la protéostasie chez la souris
Pourquoi il est important de préserver la jeunesse du sang avec l’âge
En vieillissant, le système qui produit nos cellules sanguines s’use progressivement. Les cellules souches de la moelle osseuse qui reconstituent normalement les globules rouges, les cellules immunitaires et les plaquettes deviennent plus enclines à l’inflammation et plus susceptibles de générer certains types cellulaires au détriment d’autres. Ce basculement contribue à l’anémie, à l’affaiblissement de l’immunité et à un risque accru de cancer chez les personnes âgées. L’étude résumée ici met en lumière un acteur surprenant de ce processus : un senseur antiviral appelé MDA5. En supprimant cette molécule chez la souris, les chercheurs ont constaté qu’ils pouvaient maintenir plus longtemps les cellules souches hématopoïétiques dans un état fonctionnellement plus jeune.
Un senseur conçu pour combattre les virus qui se retourne contre nous avec l’âge
MDA5 est un senseur de l’immunité innée qui détecte l’ARN double brin, un motif moléculaire fréquent chez les virus mais aussi produit par notre propre génome, notamment par les éléments mobiles dont l’activité augmente avec l’âge. Lorsque MDA5 repère cet ARN, il déclenche une cascade de signaux inflammatoires et de réponses antivirales. L’équipe s’est demandé si cette activation chronique à faible intensité chez les animaux âgés pouvait alimenter l’« inflammaging » — l’inflammation persistante et diffuse associée au vieillissement — au sein de la moelle osseuse. En comparant des souris normales et des souris dépourvues de MDA5, ils ont mesuré de nombreux molécules de signalisation immunitaire dans le liquide médullaire. Les souris âgées sans MDA5 présentaient des niveaux nettement plus faibles de cytokines inflammatoires clés, y compris l’interféron-β et l’interleukine-1, et montraient une activation réduite de régions d’ADN inflammatoires dans les cellules souches, indiquant un environnement plus calme et moins enflammé.
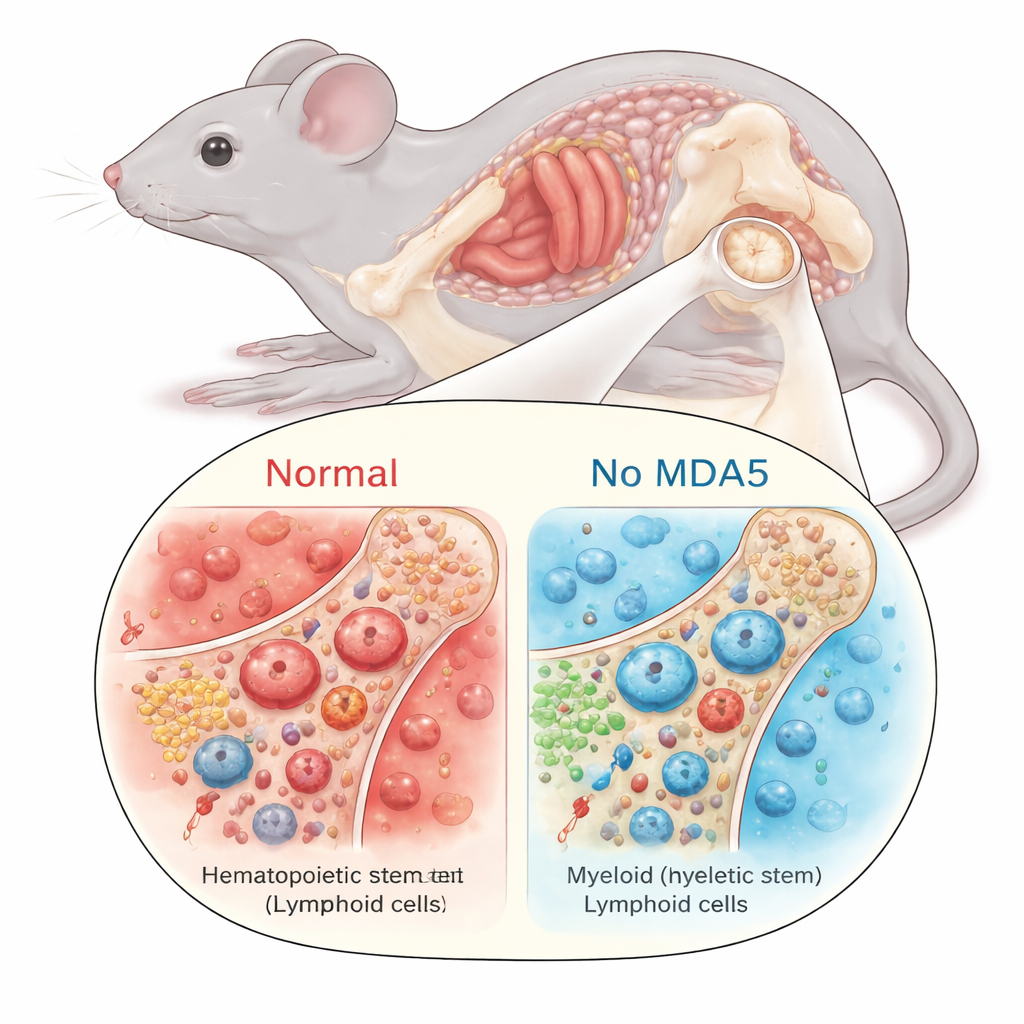
Un comportement plus jeune des cellules souches sanguines vieillissantes
Avec moins d’inflammation dans la moelle, les cellules souches hématopoïétiques se comportaient différemment. Dans le vieillissement normal, ces cellules ont tendance à s’accumuler en nombre mais à perdre en qualité : elles se divisent davantage, perdent leur capacité régénérative à long terme et développent un biais vers la production de cellules myéloïdes (comme certains globules blancs) au détriment des cellules lymphoïdes qui soutiennent l’immunité adaptative. Chez les souris âgées dépourvues de MDA5, ce schéma habituel était atténué. Leurs CSCs (cellules souches hématopoïétiques) s’étendaient moins, présentaient un biais myéloïde réduit et restaient plus quiescentes : elles passaient plus de temps à l’état de repos plutôt qu’à se diviser. Lorsque les chercheurs ont transplanté des nombres égaux de cellules souches dans des souris receveuses irradiées, les CSCs âgées déficientes en MDA5 ont mieux reconstruit le système sanguin en situations non compétitives, ce qui indique des réserves fonctionnelles supérieures par rapport aux CSCs normales du même âge.
Le métabolisme et la qualité protéique restent plus jeunes
Au-delà des dénombrements et du comportement cellulaire, les chercheurs ont examiné le fonctionnement interne de ces cellules souches. À l’aide d’une combinaison d’analyse de l’expression génique, d’accessibilité de la chromatine, de profilage métabolique et d’analyses unicellulaires, ils ont constaté que la perte de MDA5 préservait un profil métabolique et de maintien des protéines plus jeune. Les CSCs âgées déficientes en MDA5 présentaient des marqueurs redox plus sains, comme des niveaux moindres de glutathion oxydé et des niveaux plus élevés de NAD et NADP, des molécules associées à la résilience cellulaire. À l’intérieur de ces cellules, les protéines mal repliées et non repliées — un marqueur du vieillissement et du stress — étaient réduites, tandis que les marqueurs d’autophagie, le processus par lequel les cellules recyclent les composants endommagés, étaient augmentés. La synthèse protéique était réduite et les acides aminés s’accumulaient, en accord avec un passage vers un contrôle de la qualité des protéines plus attentif plutôt que vers une production rapide et sujette aux erreurs.
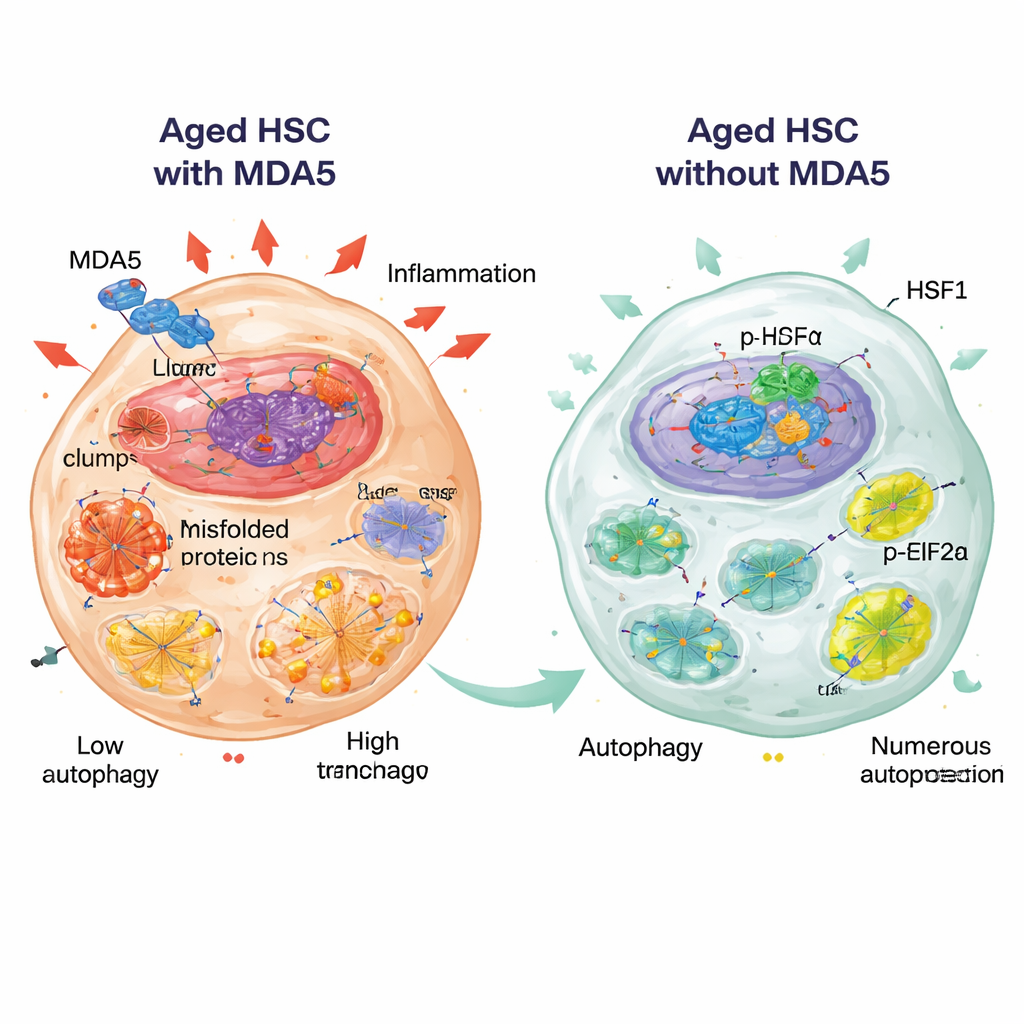
HSF1 et eIF2α : gardiens de la protéostasie
Deux régulateurs moléculaires sont apparus centraux pour cet état protecteur : HSF1, un facteur de transcription majeur qui stimule la production de chaperonnes et d’autres facteurs de protection des protéines, et eIF2α, un facteur de traduction dont la forme phosphorylée (p-eIF2α) ralentit la synthèse protéique en situation de stress. Dans les CSCs âgées déficientes en MDA5, les niveaux de protéine HSF1 et sa localisation nucléaire étaient accrus, et le p-eIF2α était augmenté, cohérents avec un programme actif de protection contre le stress. Les auteurs ont montré que MDA5 peut se rapprocher de HSF1 et, lorsqu’il est surexprimé, peut retenir HSF1 dans le cytoplasme, ce qui suggère qu’un MDA5 actif pourrait limiter les fonctions nucléaires bénéfiques de HSF1. De manière importante, lorsqu’ils ont activé pharmacologiquement HSF1 dans des CSCs âgées normales à l’aide d’une petite molécule, ces cellules sont devenues plus quiescentes et ont mieux conservé leur capacité à former des colonies au fil des passages en culture, mimant partiellement les caractéristiques de jeunesse observées en l’absence de MDA5.
Ce que cela signifie pour un vieillissement sain du sang
Dans l’ensemble, ces résultats dessinent un scénario dans lequel l’activation chronique d’un senseur antiviral, MDA5, pousse progressivement les cellules souches hématopoïétiques vers l’inflammation, le stress métabolique et les dommages protéiques. Supprimer MDA5 chez la souris interrompt ce cycle : les signaux inflammatoires dans la moelle sont atténués, les CSCs restent plus au repos et moins biaisées, et leurs systèmes internes de contrôle de la qualité des protéines restent robustes. Bien que désactiver directement MDA5 chez l’humain serait risqué en raison de son rôle dans la défense contre les infections, ce travail souligne le principe général selon lequel cibler l’inflammation liée à l’âge et renforcer la protéostasie pourrait aider à préserver la fonction des cellules souches sanguines en fin de vie. À plus long terme, des moyens plus sûrs de moduler les voies reliées à MDA5 ou d’amplifier les réponses de protection pilotées par HSF1 et eIF2α pourraient offrir des stratégies pour prolonger la durée de vie en bonne santé de notre sang et de notre système immunitaire.
Citation: Bergo, V., Bousounis, P., To Vu, G. et al. Lack of MDA5 delays hematopoietic aging by modulating inflammaging and proteostasis in mice. Nat Commun 17, 1645 (2026). https://doi.org/10.1038/s41467-026-69424-x
Mots-clés: cellules souches hématopoïétiques, inflammaging, MDA5, protéostasie, sang vieillissant