Clear Sky Science · fr
Base structurale et moléculaire de la régulation allostérique et du couplage catalytique de la phosphoribosylformylglycinamidine synthase humaine
Pourquoi cette enzyme compte pour la santé
Toutes les cellules de votre corps dépendent des purines, de petites molécules qui alimentent des réactions, stockent de l’énergie et portent l’information génétique. Les cellules cancéreuses, qui se divisent rapidement, ont un besoin particulièrement important en purines et réorganisent souvent leur mode de production. Cette étude se concentre sur une enzyme humaine appelée FGAMS, un acteur clé de la synthèse des purines de novo. En révélant la structure tridimensionnelle de FGAMS et la manière dont ses parties bougent et communiquent, les auteurs mettent au jour comment l’enzyme est activée ou inhibée et comment elle pourrait être ciblée pour ralentir la croissance tumorale.
Les éléments de la vie sous contrôle
Les cellules fabriquent les purines via une chaîne de montage exigeante appelée voie de novo, qui consomme de l’énergie et plusieurs enzymes pour assembler un anneau complexe. FGAMS réalise la quatrième étape de cette séquence et se trouve au cœur d’un ensemble enzymatique plus large nommé purinosome, qui facilite la canalisation efficace des substrats. Parce que les cellules cancéreuses à croissance rapide stimulent souvent cette voie, des enzymes comme FGAMS représentent des cibles médicamenteuses attractives : les bloquer peut priver les tumeurs des nucléotides dont elles ont besoin, tandis que les cellules saines se rabattent sur des voies de recyclage.
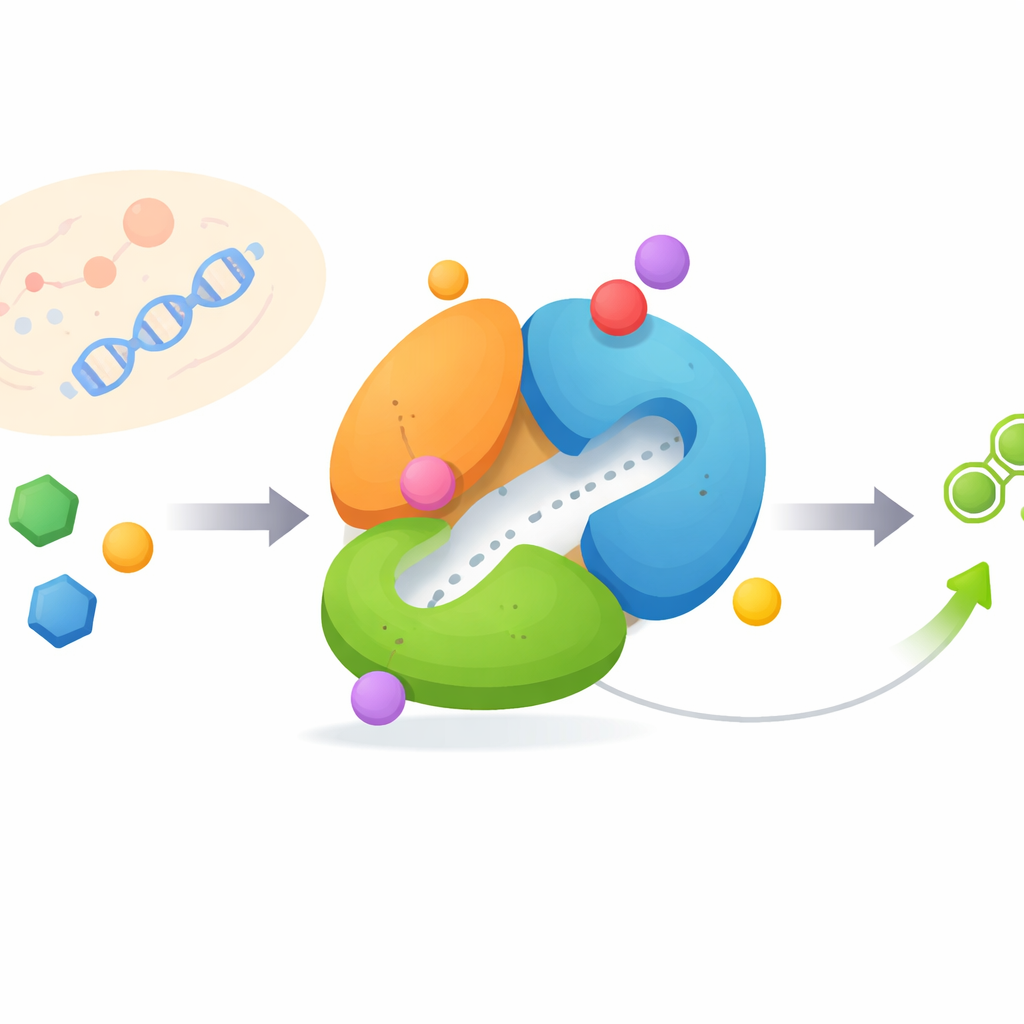
Une machine moléculaire changeante
FGAMS est construite de trois parties reliées, ou domaines, qui accomplissent chacune une fonction différente et doivent coopérer dans un ordre précis. Un domaine libère l’ammoniac de l’acide aminé glutamine, un autre utilise cet ammoniac pour modifier une petite molécule à base de sucre, et un troisième domaine joue le rôle de centre régulateur. Grâce à la cryo‑microscopie électronique à haute résolution, les chercheurs ont saisi FGAMS dans trois états de fonctionnement distincts : lié à une molécule porteuse d’énergie, avec un intermédiaire réactionnel de courte durée piégé, et avec plusieurs substrats et intermédiaires présents simultanément. La comparaison de ces états a révélé que des boucles flexibles et un « bras » N‑terminal se déplacent de manière spectaculaire, reconfigurant l’enzyme au fur et à mesure de l’avancement de la réaction.
Un tunnel caché et des portes moléculaires
Un énigme centrale était de comprendre comment l’ammoniac libéré dans un domaine voyage en toute sécurité jusqu’au site distant où il est utilisé, sans se diffuser et causer des dommages. Les nouvelles structures dévoilent un tunnel interne jusqu’alors invisible qui relie les deux sites, ainsi qu’une série de « portes » formées par des acides aminés spécifiques. Lorsque les bons substrats se lient et que l’intermédiaire se forme, une boucle centrale se verrouille en position ordonnée, tirant sur le domaine N‑terminal et réarrangeant les boucles proches dans le domaine catalytique. Cette chorégraphie ouvre deux portes d’entrée pour que la glutamine soit traitée et reconfigure brièvement une région qui stabilise l’intermédiaire à haute énergie nécessaire à la rupture de liaison.
Coupler la chimie par le mouvement
Au fur et à mesure de la réaction, l’enzyme n’attend pas passivement ; elle utilise chaque étape chimique comme signal. Une fois qu’un intermédiaire thioester covalent se forme dans le domaine générateur d’ammoniac, les mouvements antérieurs sont partiellement inversés. Cela relâche la boucle centrale et repositionne les portes pour bloquer les voies d’échappement, tandis que deux portes supplémentaires aux extrémités du tunnel s’ouvrent. Des déplacements subtils d’une poignée de résidus « goulot d’étranglement » élargissent le passage intérieur, permettant à une molécule d’ammoniac de traverser le tunnel directement vers le deuxième site actif, où elle réagit avec l’intermédiaire piégé pour produire le produit final. La mutation des résidus formant les portes provoque des fuites d’ammoniac ou le découplage des deux moitiés de la réaction, confirmant que ce système de portes et de canal est essentiel à une catalyse efficace.
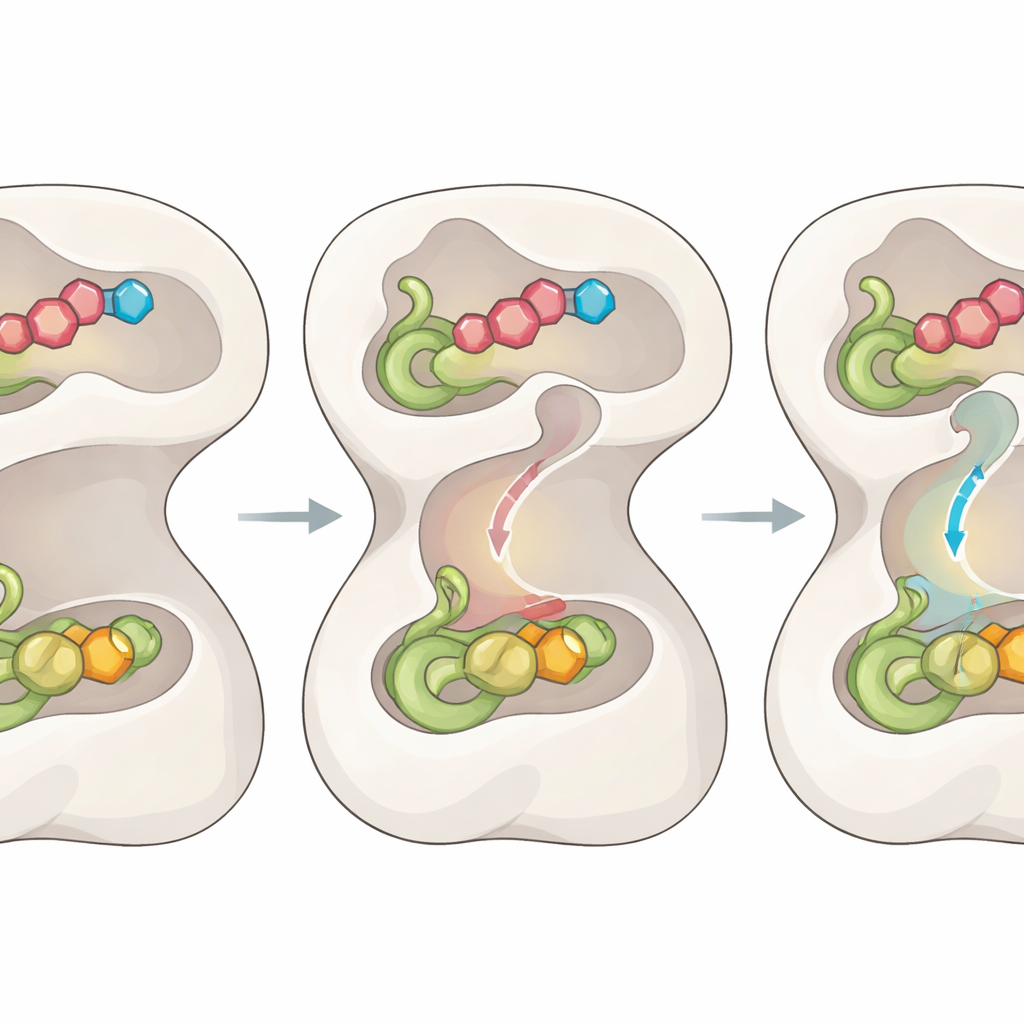
Des aperçus structuraux aux pistes thérapeutiques
En suivant FGAMS tout au long de son cycle catalytique, l’étude dresse un tableau détaillé de la façon dont les mouvements des domaines, les boucles flexibles, les portes internes et un tunnel transitoire sont tous interconnectés pour coordonner la chimie. Pour un public non spécialisé, l’idée essentielle est que l’enzyme fonctionne comme une petite usine programmable : elle n’ouvre ses portes et sa « chaîne interne » que lorsque toutes les pièces adéquates sont en place, garantissant vitesse et sécurité. Parce que FGAMS soutient la production de purines dans les cellules cancéreuses et est associée à un mauvais pronostic dans les tumeurs hépatiques, les plans structuraux et les points de contrôle nouvellement identifiés offrent plusieurs cibles potentielles pour concevoir des médicaments qui obstruent le tunnel, figent les portes ou piègent des intermédiaires clés, ouvrant la voie à une nouvelle classe de thérapies anticancéreuses ciblées.
Citation: Sharma, N., Zhou, W. & French, J.B. Structural and molecular basis for allosteric regulation and catalytic coupling of human phosphoribosylformylglycinamidine synthase. Nat Commun 17, 2732 (2026). https://doi.org/10.1038/s41467-026-69423-y
Mots-clés: biosynthèse des purines, régulation allostérique, canalisation de l’ammoniac, métabolisme du cancer, structure cryo-EM