Clear Sky Science · fr
Régulation par rétrocontrôle négatif de la signalisation STING via la golgiphagie dirigée par TAX1BP1
Comment les cellules évitent une réaction immunitaire excessive
Notre système immunitaire doit faire preuve d’un équilibre délicat : il doit reconnaître rapidement les virus envahisseurs et l’ADN endommagé, mais il doit aussi éteindre cette alarme avant que l’inflammation incontrôlée n’endommage les tissus sains. Cette étude révèle comment une aide cellulaire peu connue, TAX1BP1, agit comme un frein intégré sur une voie d’alerte puissante appelée cGAS–STING. En expliquant comment les cellules démantèlent cette alarme une fois qu’elle a fait son travail, le travail éclaire l’auto-immunité, la défense antivirale et des pistes potentielles pour des thérapies anticancéreuses.
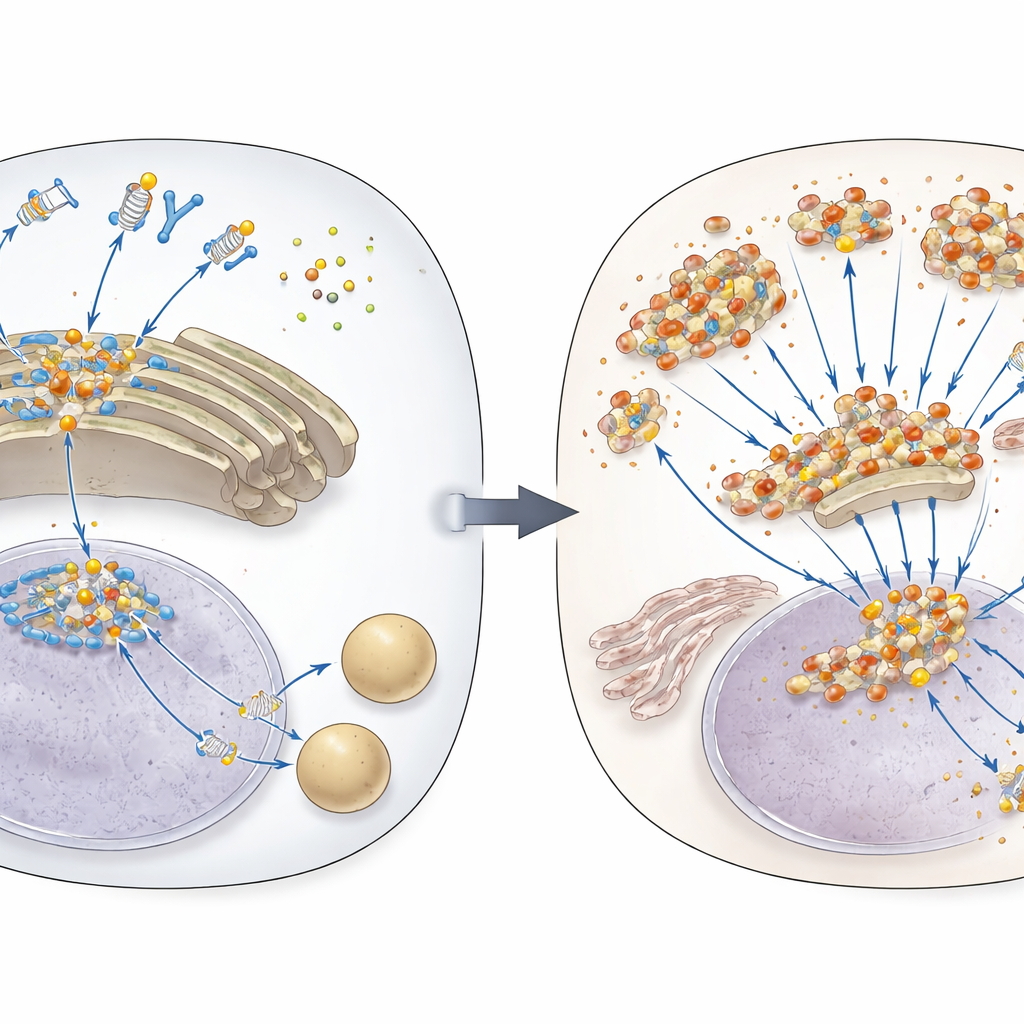
Le système d’alerte à l’ADN de la cellule
Quand de l’ADN étranger ou déplacé apparaît dans le liquide intracellulaire, une protéine détectrice nommée cGAS le repère et produit une petite molécule messagère. Ce messager active STING, une protéine de type interrupteur présente sur des membranes internes. STING migre ensuite vers un centre d’expédition cellulaire appelé Golgi, où il s’agrège et déclenche la production de molécules antivirales connues sous le nom d’interférons de type I, ainsi que d’autres signaux inflammatoires. Parce que cette réponse est très puissante, les cellules dégradent normalement STING après une brève période d’activité, le dirigeant vers les centres de recyclage cellulaires appelés lysosomes. Jusqu’à présent, la manière dont STING était ciblé pour cette phase d’arrêt n’était que partiellement comprise.
Un frein cellulaire aux multiples fonctions
TAX1BP1 était auparavant connu comme un multitâche aidant le système d’élimination cellulaire, l’autophagie, à reconnaître le matériel indésirable. Il peut se lier à la fois aux cargaisons marquées pour élimination et aux sacs en formation qui vont engloutir ces cargaisons. Les auteurs ont investigué si TAX1BP1 pouvait aussi contribuer à freiner l’alarme cGAS–STING. En utilisant des cellules humaines de type immunitaire et des macrophages de souris dépourvus de TAX1BP1, ils ont constaté que l’activation de cGAS ou STING produisait beaucoup plus d’interféron et de cytokines inflammatoires que dans les cellules normales. Ces cellules déficientes en TAX1BP1 étaient aussi plus résistantes à l’infection par le virus de l’herpès simplex, cohérent avec une signalisation antivirale hyperactivée.
Éliminer STING et un Golgi stressé
En approfondissant, les chercheurs ont montré que sans TAX1BP1, STING restait actif plus longtemps et était dégradé plus lentement. La microscopie et des tests biochimiques ont révélé que STING actif forme de grands agrégats et que ces amas s’accumulent en l’absence de TAX1BP1. Parallèlement, la structure du Golgi gonfle et se fragmente en morceaux. L’équipe a découvert que TAX1BP1, de concert avec un autre acteur du recyclage appelé p62, cible ces fragments de Golgi endommagés et les amas de STING qui s’y trouvent pour destruction dans les lysosomes — une forme spécialisée de nettoyage que les auteurs désignent par « golgiphagie ». Ce processus se distingue de l’autophagie générale et utilise plutôt des voies plus sélectives pour saisir les portions de Golgi surchargées.
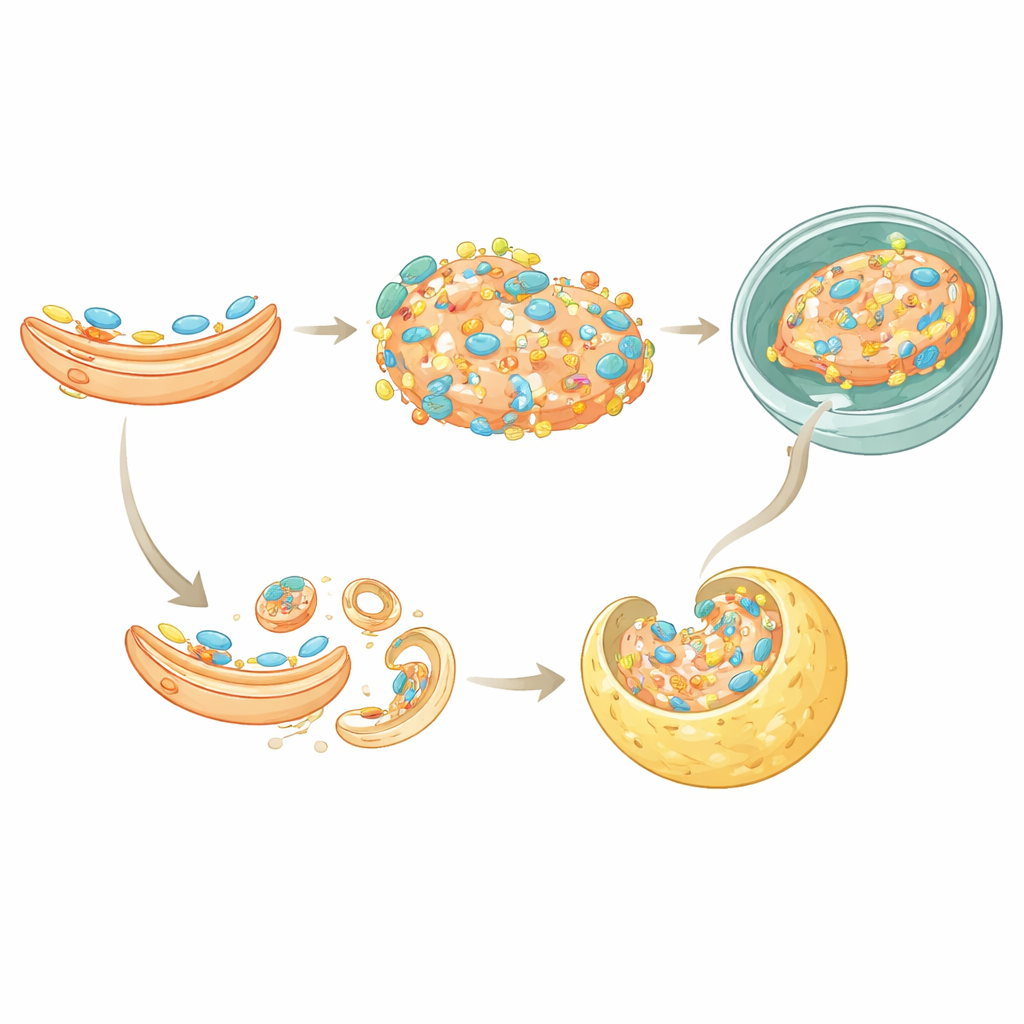
Deux voies pour éteindre l’alarme
L’étude a également mis en lumière une seconde manière dont TAX1BP1 aide à silencier STING. Normalement, une fois que STING a signalé au Golgi, il est emballé dans de petites vésicules qui bourgeonnent et sont reconnues par un système de tri des protéines appelé ESCRT, qui livre ensuite STING aux lysosomes. TAX1BP1 se lie directement à STING et facilite son interaction avec un composant clé d’ESCRT, HGS. Lorsque TAX1BP1 a été retiré, le transfert de STING vers cette machinerie de tri était moins efficace, et sa dégradation a ralenti. Cependant, une partie de la dégradation persiste, indiquant que TAX1BP1 travaille aux côtés de p62 dans cette voie de microautophagie, offrant aux cellules des moyens partiellement redondants pour s’assurer que STING ne persiste pas trop longtemps.
Pourquoi c’est important pour la santé et la maladie
Pour tester l’importance de ce frein chez l’animal vivant, les chercheurs ont génétiquement modifié des souris pour qu’elles manquent de TAX1BP1 spécifiquement dans certains cellules immunitaires. Lorsqu’on les a stimulées avec un médicament activant STING, ces souris présentaient des taux d’interféron et de cytokines inflammatoires dans le sang plus élevés que les souris normales. Lors d’une infection par un poxvirus, elles portaient moins de virus, montrant une résistance accrue. Ensemble, ces résultats suggèrent que TAX1BP1 couple le moment d’activation de STING au Golgi à un arrêt programmé par destruction ciblée à la fois de STING et des membranes de Golgi endommagées. Pour un non-spécialiste, l’idée principale est que les cellules non seulement déclenchent une alarme lorsqu’elles détectent de l’ADN dangereux, mais qu’elles démantèlent aussi activement des parties de leur propre câblage interne pour s’assurer que l’alarme se coupe. Comprendre et potentiellement ajuster ce frein interne pourrait aider à concevoir des traitements pour des maladies inflammatoires chroniques, améliorer les défenses antivirales ou moduler les réponses immunitaires en cancérologie.
Citation: Suklabaidya, S., Mohanty, S., Reider, I.E. et al. Negative feedback regulation of STING signaling by TAX1BP1-directed Golgiphagy. Nat Commun 17, 2762 (2026). https://doi.org/10.1038/s41467-026-69422-z
Mots-clés: immunité innée, voie STING, autophagie, appareil de Golgi, réponse antivirale