Clear Sky Science · fr
Mécanisme d’action moléculaire de la petite molécule SMT-738 sur le transporteur de lipoprotéines bactérien LolCDE
Pourquoi ce nouvel antibiotique est important
Alors que de plus en plus d’infections nosocomiales résistent à nos meilleurs antibiotiques, les médecins ont un besoin urgent de médicaments capables d’éliminer les bactéries dangereuses sans détruire les microbes utiles que nous hébergeons. Cette étude décrit comment un composé expérimental prometteur, nommé SMT-738, bloque une machine de transport cruciale dans la couche externe de certaines bactéries difficiles à traiter. En révélant précisément où et comment ce médicament bloque la machinerie, le travail ouvre la voie à des antibiotiques plus intelligents qui visent les super‑bactéries tout en épargnant une grande partie du microbiote intestinal.
L’armure externe des bactéries pathogènes
Beaucoup des agents pathogènes les plus préoccupants en milieu hospitalier appartiennent à un groupe appelé bactéries Gram‑négatives. Elles sont difficiles à éradiquer parce qu’elles s’enveloppent d’une armure externe à double couche. Cette couche externe est construite et maintenue par plusieurs machines moléculaires qui déplacent des éléments de construction depuis la membrane interne, où ils sont synthétisés, vers la surface. Un type important de cargaison est constitué par les lipoprotéines, qui contribuent à l’intégrité de l’enveloppe externe et soutiennent des processus tels que l’absorption de nutriments et la résistance aux antibiotiques. Un système de transport appelé voie Lol, et en particulier une pompe nommée LolCDE, extrait les lipoprotéines de la membrane interne et les remet à des chaperons qui les acheminent vers la surface externe. Parce que ces étapes sont essentielles, elles constituent des cibles attractives pour de nouveaux antibiotiques.
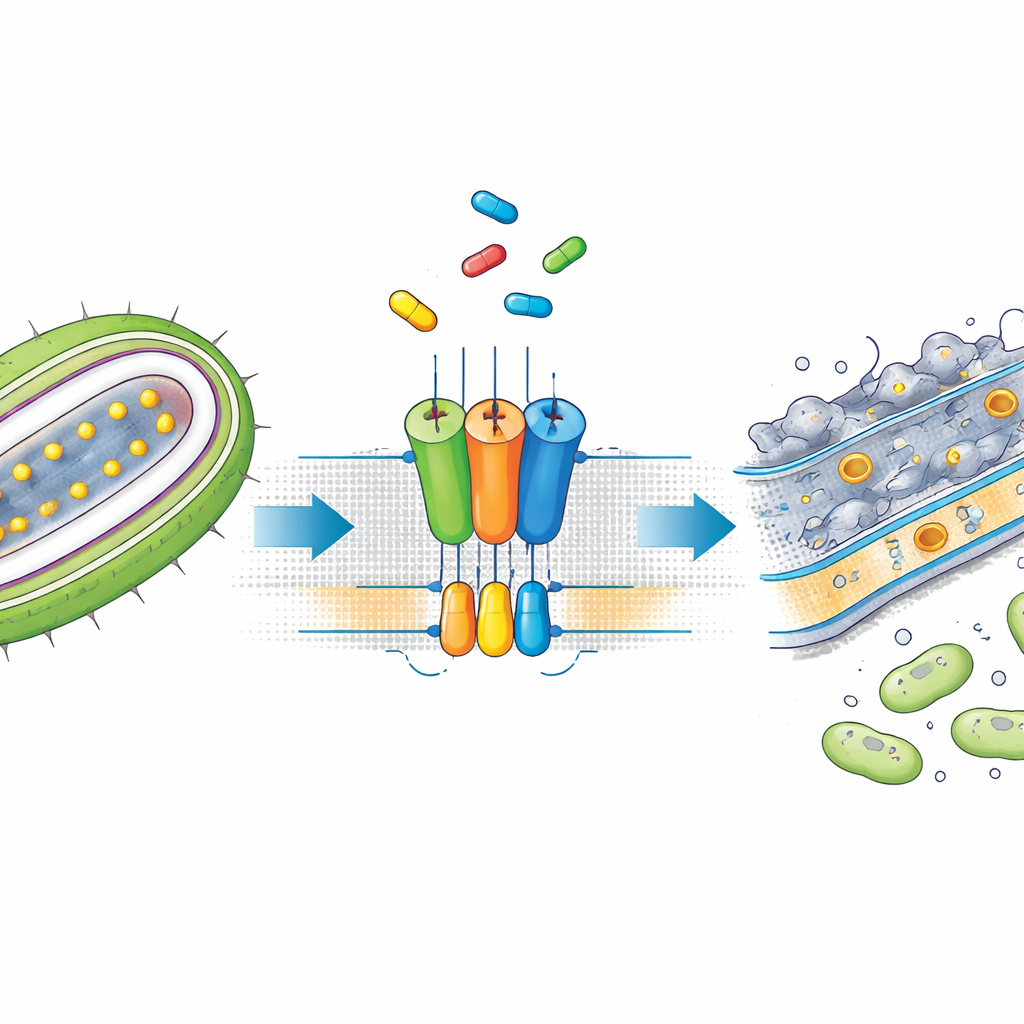
Une petite molécule qui bloque le tapis roulant
SMT-738 est apparu lors de criblages antérieurs comme un bloqueur puissant des pathogènes Gram‑négatifs de la famille des Enterobacteriaceae, y compris des souches multirésistantes d’Escherichia coli et de Klebsiella pneumoniae. Pourtant, son mode d’action précis restait flou. Les auteurs ont d’abord montré que SMT-738 empêche une lipoprotéine test d’être libérée par LolCDE dans des bactéries modifiées, confirmant que le composé bloque réellement l’étape de transport. Fait important, lorsque les bactéries portaient certaines mutations dans les gènes codant pour le complexe LolCDE, elles devenaient résistantes à SMT-738, ce qui suggère que le médicament agit en se liant directement à cette pompe. Ces observations ont préparé le terrain pour une plongée structurale afin de comprendre comment le composé interagit avec le transporteur.
Bloquer la pompe de l’intérieur
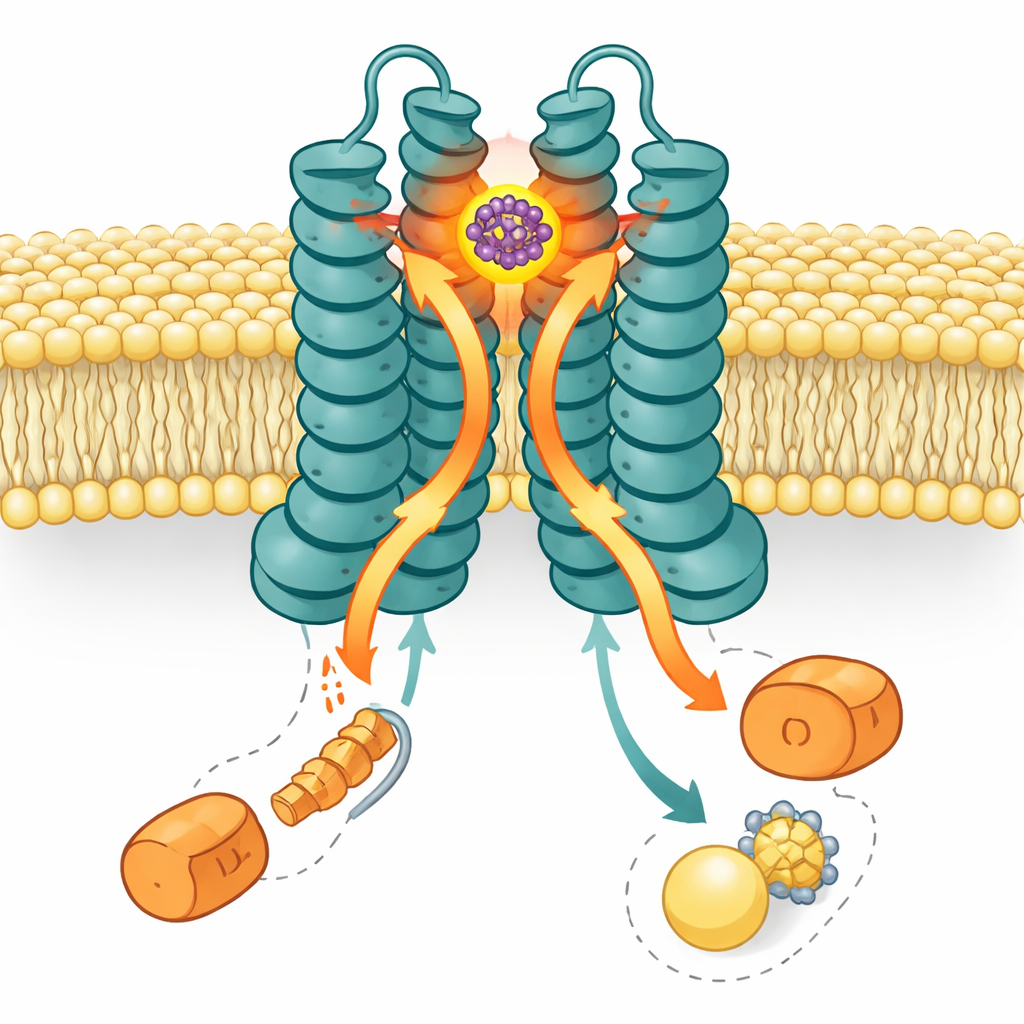
Grâce à la microscopie cryo‑électronique à haute résolution, les chercheurs ont obtenu une image tridimensionnelle de LolCDE avec SMT-738 verrouillé en place. La structure montre le médicament calé dans une poche à l’extrémité périplasmique — du côté faisant face à l’espace entre les membranes interne et externe — entre deux sous‑unités centrales, LolC et LolE. Ce site recouvre la zone d’ancrage normale du cargo lipoprotéique. Quand SMT-738 occupe cette poche, les acides aminés environnants de LolC et LolE se déplacent d’environ un nanomètre. Ces mouvements créent des encombrements stériques avec l’emplacement où la lipoprotéine et ses queues lipidiques seraient normalement situées, empêchant effectivement l’entrée du cargo dans la pompe. La mutation de nombreuses résidues bordant la poche a soit affaibli la liaison du médicament, soit rendu les bactéries résistantes, en accord net avec l’image structurale.
Provoquer une rupture unilatérale
L’histoire ne s’arrête pas au site de liaison. LolCDE est alimenté par deux copies d’une sous‑unité motrice nommée LolD, qui se situent du côté cytoplasmique et hydrolysent l’ATP pour fournir l’énergie du transport. De façon frappante, dans la structure liée à SMT-738, une seule LolD reste attachée ; la partenaire LolD s’est dissociée. Des gels biochimiques et des tests d’activité ATPasique ont confirmé que la liaison de SMT-738 provoque la perte d’une LolD et réduit fortement l’activité énergétique de la pompe. Des simulations informatiques du transporteur dans une membrane ont confirmé cette vue : à mesure que SMT-738 se logeait dans sa poche, des changements conformationnels se propageaient vers le bas, poussant les hélices de couplage qui relient LolC et LolE à LolD. Ces déplacements ont placé la LolD liée à LolC dans un conflit défavorable, la forçant à se détacher, tandis que la LolD liée à LolE restait en place. Le résultat est une machine asymétrique « bloquée » qui ne peut plus déplacer les lipoprotéines.
Pourquoi certaines bactéries sont touchées et d’autres épargnées
SMT-738 présente un avantage souhaitable : il attaque fortement les Enterobacteriaceae résistantes aux médicaments tout en laissant de nombreuses autres espèces Gram‑négatives du microbiote intestinal largement intactes. Pour comprendre cette sélectivité, l’équipe a comparé les séquences de LolE entre bactéries sensibles et résistantes et s’est concentrée sur les positions en contact avec SMT-738. Deux résidus de LolE, en particulier une position correspondant à D264 chez E. coli, se sont distingués. Chez les pathogènes sensibles, ces positions correspondaient à la version contact‑médicament d’E. coli, alors que chez de nombreux commensaux intestinaux résistants elles étaient remplacées par d’autres acides aminés. Lorsque les chercheurs ont modifié génétiquement E. coli pour porter de telles substitutions, les bactéries sont devenues fortement résistantes à SMT-738 tout en continuant d’exprimer LolCDE. Les simulations suggéraient que ces changements modifient la flexibilité locale autour de la poche, réduisant la capacité de SMT-738 à se lier. Fait intéressant, un autre inhibiteur de LolCDE, la lolamicine, s’appuie sur des points de contact seulement partiellement chevauchants et montrait un profil de résistance différent, suggérant des manières distinctes de cibler la même pompe.
De nouveaux plans pour les antibiotiques du futur
En combinant imagerie structurale, scans mutationnels, tests biochimiques et simulations informatiques, ce travail montre que SMT-738 n’est pas qu’un simple bouchon dans un canal. Il se fixe plutôt sur le côté périplasmique de la pompe LolCDE, bloque le site d’entrée des lipoprotéines, puis déclenche des déplacements à longue portée qui éjectent l’une des deux unités motrices, immobilisant le transporteur dans un état non fonctionnel. Ce mécanisme d’« enclenchement allostérique » représente une nouvelle façon de neutraliser une machine bactérienne et aide à expliquer pourquoi SMT-738 peut cibler précisément des agents pathogènes dangereux tout en épargnant une grande partie du microbiome. La carte détaillée de la poche de liaison et le résidu clé de sélectivité dans LolE offrent désormais une feuille de route rationnelle pour concevoir des antibiotiques de nouvelle génération exploitant la même vulnérabilité avec encore plus de puissance et de précision.
Citation: Li, H., Zhu, X., Zhang, D. et al. Molecular mechanism of action of small molecule SMT-738 on bacterial lipoprotein transporter LolCDE. Nat Commun 17, 2540 (2026). https://doi.org/10.1038/s41467-026-69411-2
Mots-clés: résistance aux antibiotiques, bactéries Gram-négatives, transport de lipoprotéines, inhibiteur de LolCDE, structure cryo-EM