Clear Sky Science · fr
Le lactate dérivé des macrophages entraîne le remodelage phénotypique des fibroblastes dermiques via la lactylation de l’histone H3 lysine 23 primée par MCT1 dans la cicatrice hypertrophique
Pourquoi certaines cicatrices deviennent épaisses et surélevées
La plupart des coupures et des brûlures finissent par s’atténuer en cicatrices fines et plates. Mais certaines plaies guérissent en formant des bandes de tissu épaisses et surélevées appelées cicatrices hypertrophiques, qui peuvent démanger, faire mal et limiter les mouvements. Cette étude révèle un moteur inattendu de ces cicatrices tenaces : un sous-produit métabolique courant, le lactate, produit par des cellules immunitaires dans une peau cicatrisante rigide, qui reprogramme les cellules réparatrices voisines pour adopter un comportement plus agressif et pro-cicatrice.
De la réparation normale à la cicatrice problématique
Dans la cicatrisation saine, les cellules cutanées coopèrent pour fermer la blessure et reconstruire le tissu. Les fibroblastes, principales cellules réparatrices du derme, basculent brièvement vers un état plus actif produisant du collagène, l’armature protéique de la peau. Une fois la plaie refermée, ces cellules se calment. Dans les cicatrices hypertrophiques, cependant, les fibroblastes restent coincés dans cet état hyperactif, déposant trop de collagène en faisceaux épais et désorganisés. Les auteurs ont commencé par comparer la peau normale au tissu de cicatrice hypertrophique et ont observé un basculement métabolique net : l’environnement de la cicatrice favorisait une chimie glycolytique rapide générant de grandes quantités de lactate, ainsi que des niveaux élevés d’une protéine de transport appelée MCT1 qui fait entrer le lactate dans les cellules. 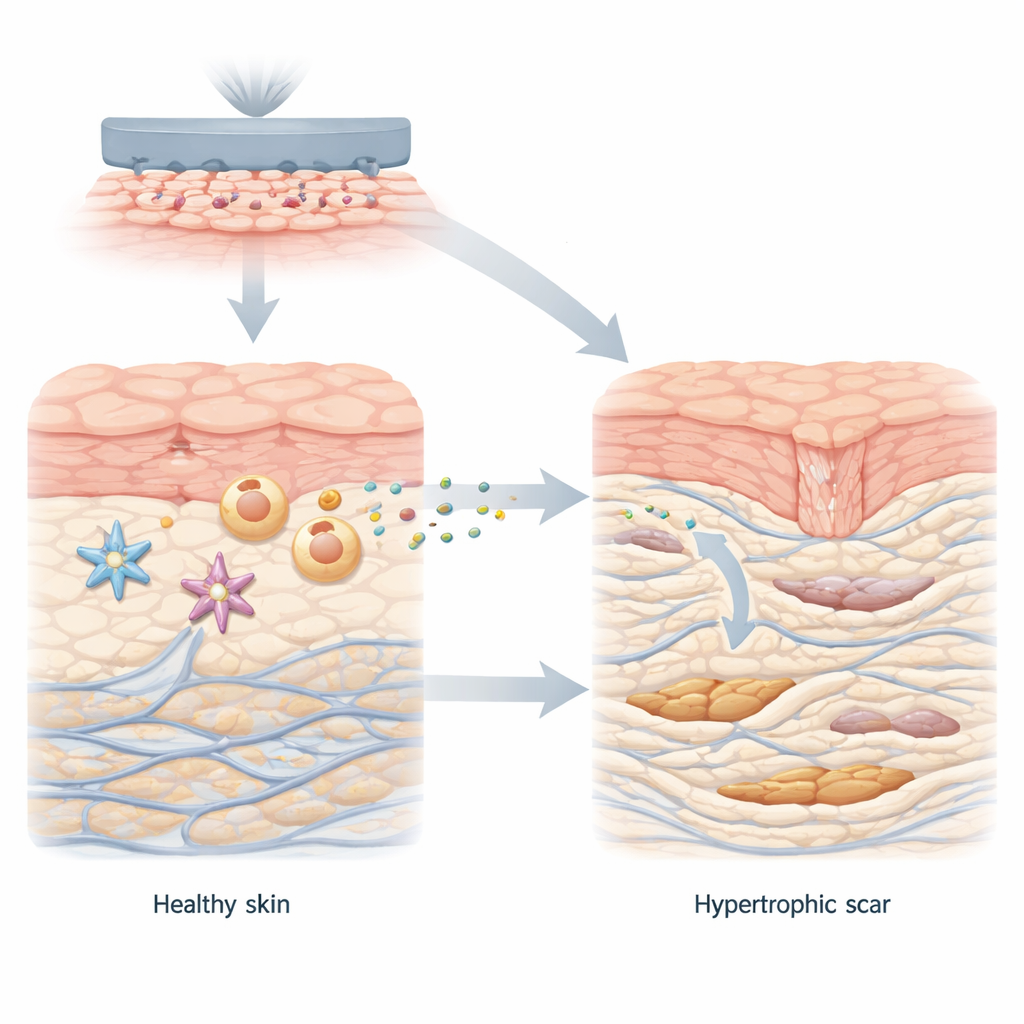
Les cellules immunitaires, usines inattendues de lactate
Pour identifier l’origine de ce lactate, l’équipe a examiné différents types cellulaires de peau humaine et de modèles murins : les macrophages (cellules immunitaires qui éliminent les débris et coordonnent la réparation), les cellules des vaisseaux sanguins et les fibroblastes. Elles ont cultivé ces cellules sur des substrats mous ou rigides reproduisant la peau normale et cicatrisée. Sur des surfaces rigides, seuls les macrophages ont basculé vers un mode hautement glycolytique, vorace en glucose, et ont sécrété de grandes quantités de lactate, tant en culture qu’au sein de tissus cicatriciels réels. Lorsque les macrophages ont été retirés de plaies murines en cours de guérison, les niveaux de lactate tissulaire ont chuté et la formation de cicatrice a diminué. Ces résultats désignent les macrophages, en particulier ceux qui détectent un environnement rigide, comme les principales usines à lactate qui façonnent le microenvironnement cicatriciel.
Le lactate comme signal qui reprogramme les fibroblastes
Les chercheurs ont ensuite interrogé l’effet de cet excès de lactate sur les fibroblastes. Lorsqu’ils ont exposé des fibroblastes à un milieu riche en lactate provenant de macrophages cultivés sur support rigide, ces fibroblastes ont proliféré plus vite, migré davantage et produit plus de collagène, autant de caractéristiques de l’état agressif de myofibroblaste. Bloquer le transporteur MCT1 sur les fibroblastes, ou réduire la production de lactate par les macrophages, a nettement atténué ces changements. À l’intérieur des fibroblastes, le lactate entrant faisait plus que fournir de l’énergie : il déclenchait une marque chimique spécifique sur les protéines histones qui emballent l’ADN dans le noyau cellulaire. Cette marque, appelée lactylation de H3K23, était beaucoup plus élevée dans les fibroblastes formant des cicatrices que dans les fibroblastes normaux et agissait comme un interrupteur activant deux gènes clés, HEY2 et COL11A1, qui amplifient conjointement les signaux de cicatrisation.
Une boucle d’amplification auto-entretenue
Les protéines induites par cette modification des histones constituent une boucle de rétroaction puissante. HEY2 augmente l’activité d’une voie impliquant YAP1 et SMAD2, connue pour pousser les fibroblastes vers un état plus contractile et producteur de collagène. COL11A1, une protéine structurelle liée au collagène, interagit physiquement avec le transporteur MCT1 sur les fibroblastes, contribuant à le stabiliser et à rendre l’entrée du lactate plus efficace. En d’autres termes, le lactate qui pénètre dans la cellule modifie la régulation génique d’une manière qui renforce encore l’entrée de lactate et la production de collagène, enfermant les fibroblastes dans une identité pro-cicatrice. 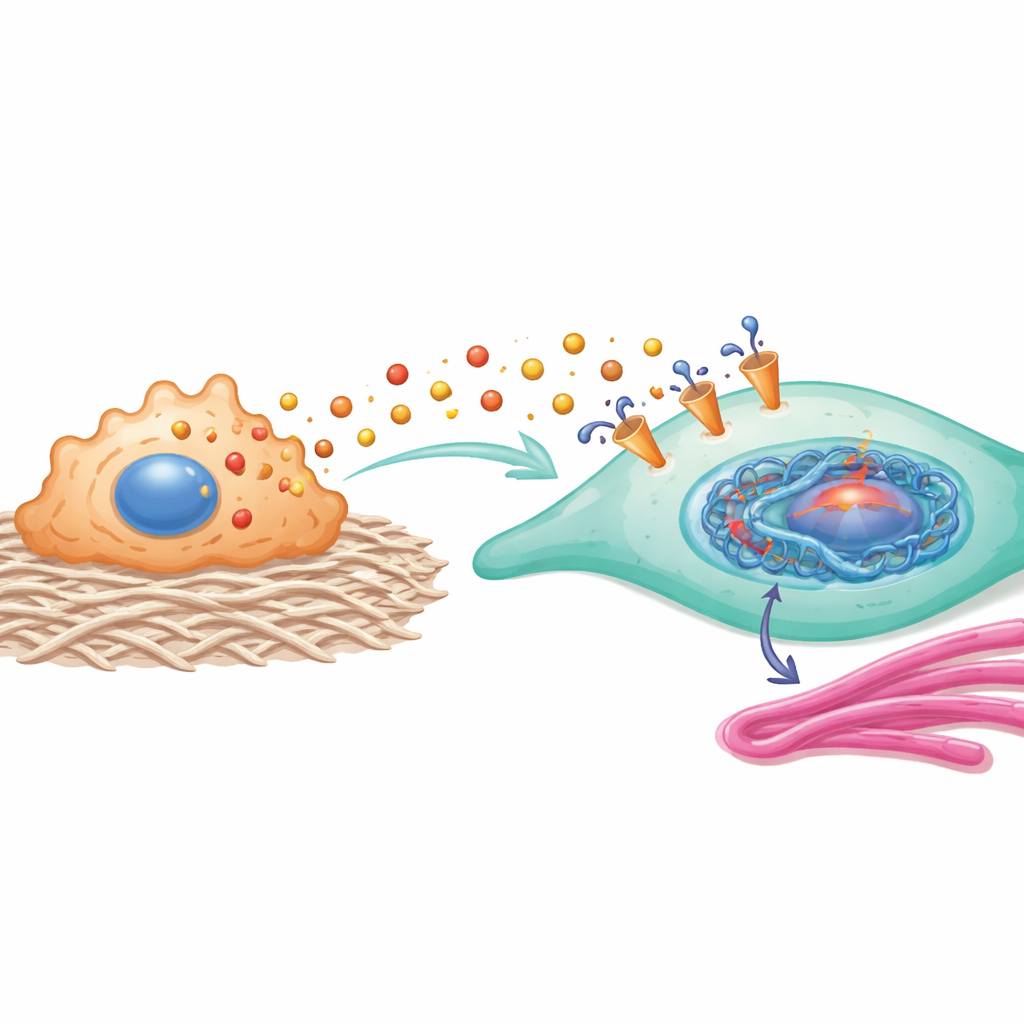
Réduire la boucle pour améliorer la guérison
Pour tester si interrompre cette boucle peut améliorer la guérison, l’équipe a utilisé des souris chez lesquelles MCT1 pouvait être supprimé sélectivement dans les fibroblastes, ainsi qu’un médicament bloquant MCT1. Dans les deux cas, les plaies se refermaient plus rapidement, la peau nouvellement formée paraissait mieux organisée et les fibres de collagène étaient plus fines et mieux alignées, avec moins de caractéristiques de cicatrice hypertrophique. La marque histone spécifique et ses gènes en aval ont également diminué. L’élimination des macrophages, principale source de lactate, ou la réduction chimique du lactate ont produit des effets anti-cicatrice similaires. Ces expériences montrent que la chaîne plaie rigide–macrophage–lactate–fibroblaste n’est pas qu’une corrélation mais bien un moteur clé de la cicatrisation pathologique.
Ce que cela signifie pour les traitements futurs des cicatrices
Ce travail requalifie le lactate, non plus simple déchet métabolique, mais messager puissant reliant mécanique, métabolisme et contrôle génétique dans la cicatrisation. En montrant comment le lactate d’origine macrophagique, transporté via MCT1, modifie les histones et déclenche un programme de cicatrisation auto-entretenu dans les fibroblastes, l’étude met en lumière plusieurs cibles thérapeutiques prometteuses. Des médicaments modulant la production de lactate, bloquant MCT1 ou interférant avec la modification histone spécifique pourraient un jour aider les plaies à guérir plus rapidement et à laisser des cicatrices plus plates et moins visibles.
Citation: Yuan, Y., Xiao, Y., Zou, J. et al. Lactate derived from macrophages drives skin dermal fibroblasts phenotypic remodeling via MCT1-primed histone H3 lysine 23 lactylation in hypertrophic scar. Nat Commun 17, 2694 (2026). https://doi.org/10.1038/s41467-026-69388-y
Mots-clés: cicatrice hypertrophique, signalisation du lactate, communication macrophage–fibroblaste, lactylation des histones, thérapie de cicatrisation