Clear Sky Science · fr
La myoferline est un composant des vésicules de trafic vRNP en phase finale pour les virus à ARN enveloppés
Pourquoi cela compte pour la santé quotidienne
La grippe saisonnière et d’autres infections respiratoires peuvent sembler routinières, mais elles tuent ensemble des millions de personnes chaque année dans le monde. Beaucoup de ces virus, y compris le virus de la grippe A et le virus respiratoire syncytial (VRS), échappent déjà aux vaccins et aux antiviraux en mutant rapidement. Cette étude examine plutôt quelque chose que les virus ne peuvent pas facilement modifier : la machinerie cellulaire humaine qu’ils détournent pour s’échapper des cellules infectées. En découvrant une vulnérabilité partagée dans cette machinerie, ce travail ouvre la voie à des médicaments futurs susceptibles d’atténuer en une fois une large gamme de virus respiratoires.
Une voie de livraison cellulaire exploitée par les virus
Nos cellules des voies aériennes réutilisent en permanence des portions de leur membrane externe par un processus appelé recyclage. De petites bulles membranaires, ou vésicules, transportent des cargos de l’intérieur de la cellule vers la surface, guidées par une famille de protéines connues collectivement sous le nom de Rab11. Le virus de la grippe A, le VRS et un virus apparenté appelé virus de Sendai exploitent tous cette voie en fin d’infection. Ils chargent leur matériel génétique, empaqueté sous forme de complexes ribonucléoprotéiques, sur des vésicules contenant Rab11 qui les conduisent vers la face apicale (orientée vers les voies aériennes) de la cellule, où de nouveaux particules virales bourgeonnent et se propagent. Jusqu’à présent, Rab11 était le seul facteur de l’hôte clairement partagé par ces vésicules de trafic, laissant un vide important dans notre compréhension de leur formation et de leur fonctionnement.
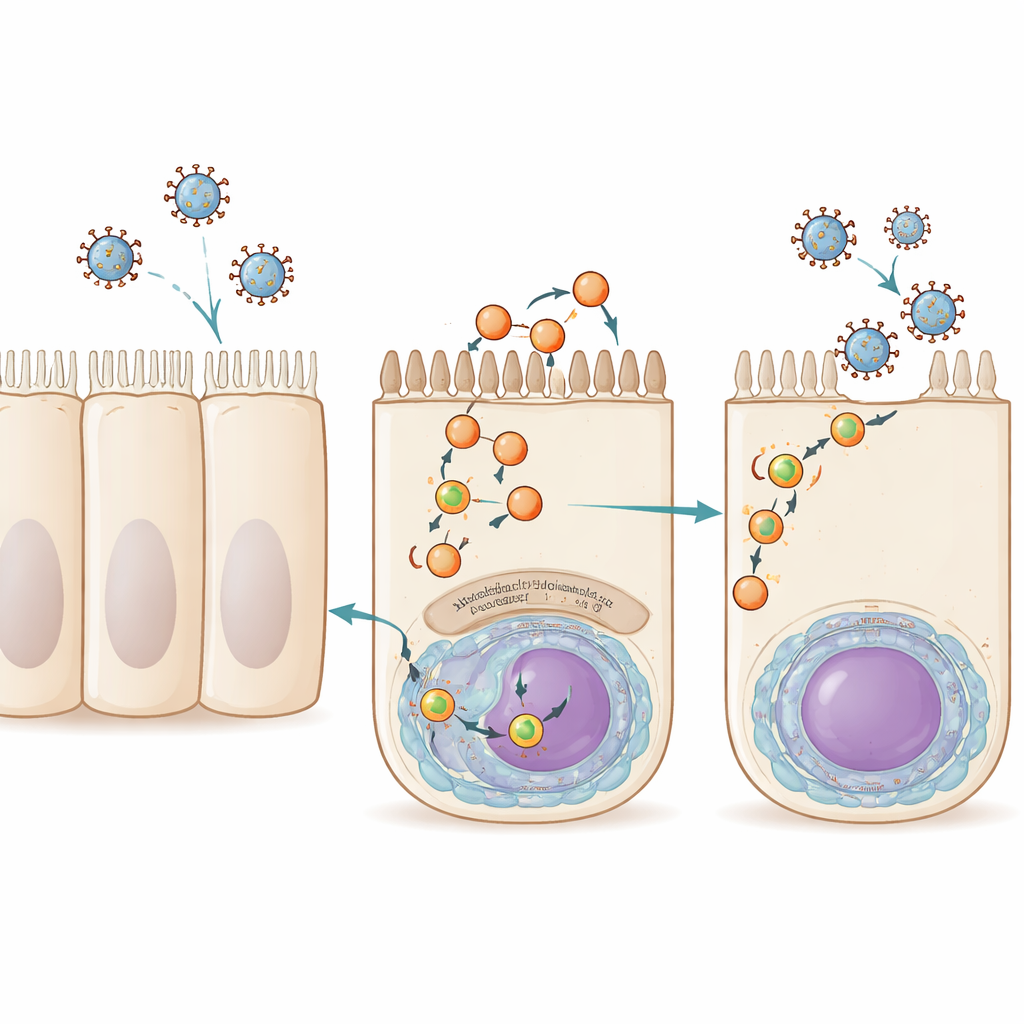
Découverte d’un nouvel acteur : la myoferline
Les chercheurs ont commencé par se demander quelles protéines humaines s’associent physiquement au dispositif d’empaquetage du génome de la grippe à différents moments de l’infection. Ils ont ingénieré un virus de la grippe A dont la polymérase portait une étiquette moléculaire, puis ont utilisé la spectrométrie de masse pour inventorier les protéines humaines liées à ce complexe en début et en fin d’infection. Parmi des centaines de candidats, une protéine s’est distinguée aux stades tardifs : la myoferline, une grande protéine associée aux membranes précédemment liée au développement musculaire, à l’endocytose et à la réparation membranaire. Lorsque l’équipe a réduit les niveaux de myoferline dans des cellules dérivées du poumon en utilisant des petits ARN interférents ou l’a bloquée avec un inhibiteur de petite molécule, les cellules produisaient toujours normalement ARN viral et protéines virales, mais libéraient beaucoup moins de particules infectieuses de la grippe. Cela indiquait que la myoferline n’est pas nécessaire à la copie du génome viral, mais qu’elle est cruciale pour les stades tardifs où les nouveaux virus sont assemblés et quittent la cellule.
La myoferline voyage avec le cargo viral
Une imagerie à haute résolution a révélé où se trouve la myoferline pendant l’infection. Dans les cellules non infectées, la myoferline coïncide largement avec les vésicules de recyclage positives pour Rab11, à la fois près du noyau et vers le bord cellulaire, et la perte de l’une ou l’autre protéine perturbe la distribution normale de l’autre. Lors de l’infection par la grippe, le réseau Rab11 est remodelé de façon spectaculaire en vésicules agrandies et irrégulières qui transportent les ribonucléoprotéines virales. La myoferline reste présente dans ces vésicules remodélisées et montre une forte colocalisation avec le génome viral et Rab11. Lorsque l’équipe a utilisé un médicament qui force les complexes du génome viral et leurs vésicules porteuses à s’agréger, la myoferline a été entraînée dans les mêmes agrégats, confirmant qu’elle est un composant intégré de ces structures de trafic en phase finale et non un simple voisin par hasard.
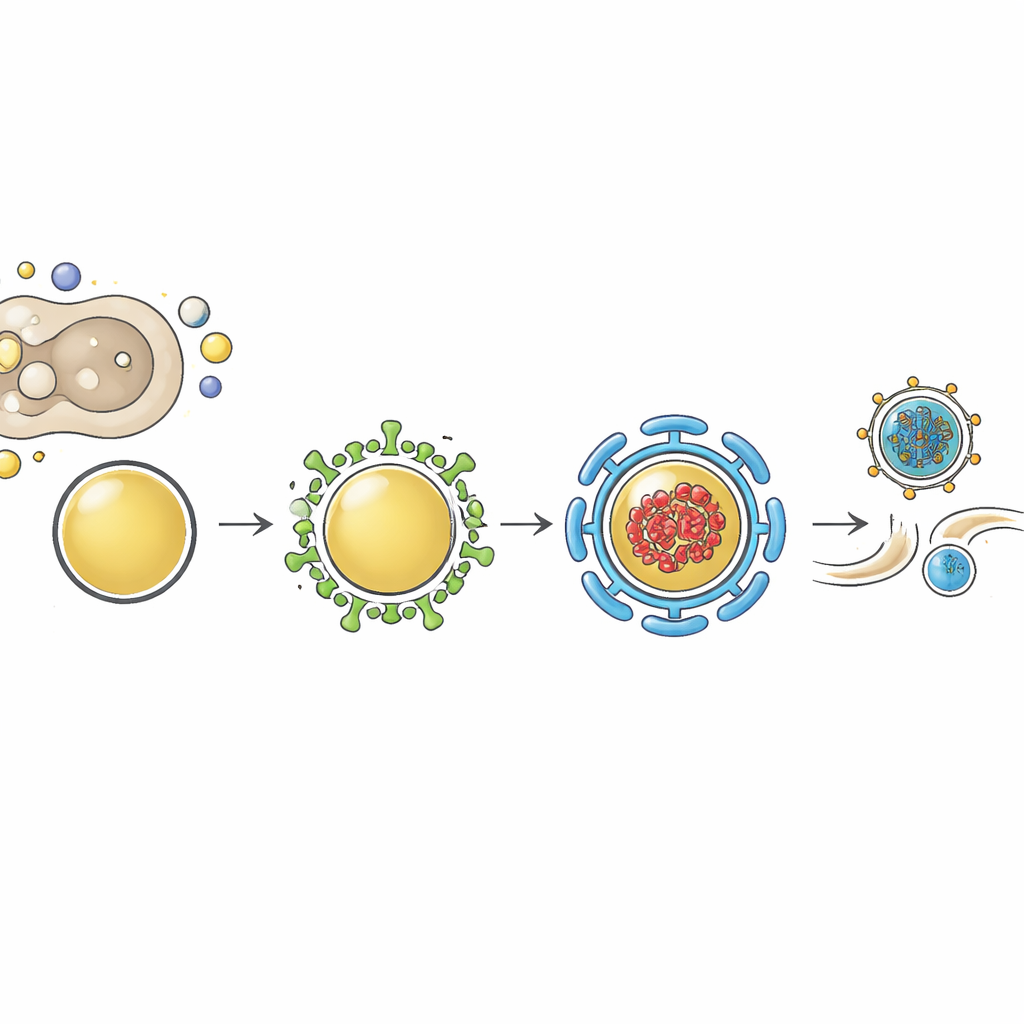
Un carrefour commun à plusieurs virus respiratoires
L’étude a ensuite examiné si cette dépendance à la myoferline est spécifique à la grippe ou partagée de façon plus générale. La réduction de la myoferline dans des cellules pulmonaires infectées par le VRS ou le virus de Sendai a de nouveau provoqué une forte baisse de virus infectieux libérés, sans diminuer les niveaux d’ARN viral. L’imagerie monomoléculaire a montré que les génomes des deux virus se regroupent avec la myoferline et Rab11 dans des points cytoplasmiques qui représentent probablement des carrefours de transport plutôt que des usines de réplication. Ce schéma soutient une image unificatrice : différents virus respiratoires à ARN enveloppés, malgré leurs styles de vie variés, convergent vers le même système de vésicules Rab11–myoferline lorsqu’il s’agit de déplacer leurs génomes complétés vers la surface cellulaire pour l’empaquetage et la sortie.
Comment la myoferline façonne les vésicules transportant les virus
La myoferline est composée de plusieurs domaines « C2 » capables de lier les membranes et des protéines partenaires. Des travaux antérieurs ont montré que l’un de ces domaines interagit avec une famille de protéines remodelant les membranes appelées EHD. Dans cette étude, des EHD1 et EHD2 marqués par fluorescence ont été trouvés au sein des mêmes vésicules remodélisées qui transportent les génomes de la grippe et Rab11, en particulier lorsque ces vésicules étaient expérimentalement agrégées. La réduction des niveaux d’EHD2, comme la réduction de la myoferline, diminuait les rendements de la grippe sans affecter la réplication du génome. De plus, l’élimination de la myoferline entraînait une baisse des niveaux de protéine EHD2, suggérant que la myoferline aide à stabiliser ou à positionner correctement EHD2 sur les membranes. Les auteurs proposent que la myoferline se place sur les vésicules positives pour Rab11 et recrute les protéines EHD pour sculpter leurs membranes, complétant ainsi la formation de « vésicules irrégulièrement recouvertes » spécialisées et optimisées pour transporter le cargo viral vers les sites de bourgeonnement.
Ce que cela signifie pour les stratégies antivirales futures
Dans l’ensemble, ces résultats placent la myoferline comme un organisateur central d’une voie de recyclage de l’hôte dont dépendent de nombreux virus respiratoires enveloppés à une étape critique tardive. Parce que cibler uniquement les protéines virales conduit souvent à une résistance rapide, les facteurs de l’hôte réutilisés par plusieurs virus constituent des cibles médicamenteuses attrayantes. Interférer avec la fonction de la myoferline, ou avec son partenariat avec Rab11 et les protéines EHD, pourrait en principe ralentir ou bloquer la propagation de pathogènes divers, de la grippe et du VRS à d’autres virus dépendants de Rab11, comme certains coronavirus. Il reste beaucoup de travail pour traduire ce concept en thérapies sûres, mais l’étude fournit une carte détaillée d’une voie d’évasion virale partagée — et met en lumière la myoferline comme un point d’étranglement prometteur sur ce chemin.
Citation: Bonazza, S., Turkington, H.L., Sukumar, S. et al. Myoferlin is a component of late-stage vRNP trafficking vesicles for enveloped RNA viruses. Nat Commun 17, 2507 (2026). https://doi.org/10.1038/s41467-026-69386-0
Mots-clés: grippe, virus respiratoires, trafic vésiculaire, facteurs hôtes, myoferline