Clear Sky Science · fr
Nanovésicules exosomales conçues pour délivrer des anticorps afin de traiter la maladie inflammatoire de l’intestin
Un nouvel espoir pour une maladie intestinale tenace
La maladie inflammatoire de l’intestin (MII) peut transformer la vie quotidienne en une lutte permanente contre la douleur, la diarrhée et la fatigue, et augmente aussi le risque à long terme de cancer du côlon. De nombreux médicaments actuels calment les poussées mais ne rétablissent pas véritablement les réactions immunitaires défaillantes à l’origine de la maladie, si bien que les symptômes réapparaissent souvent. Cette étude présente une nanoparticule « intelligente » ingénieusement conçue qui circule dans le sang, identifie les zones enflammées de l’intestin et délivre un traitement en deux volets visant à la fois à réduire l’inflammation nocive et à reconstruire un équilibre immunitaire durable.
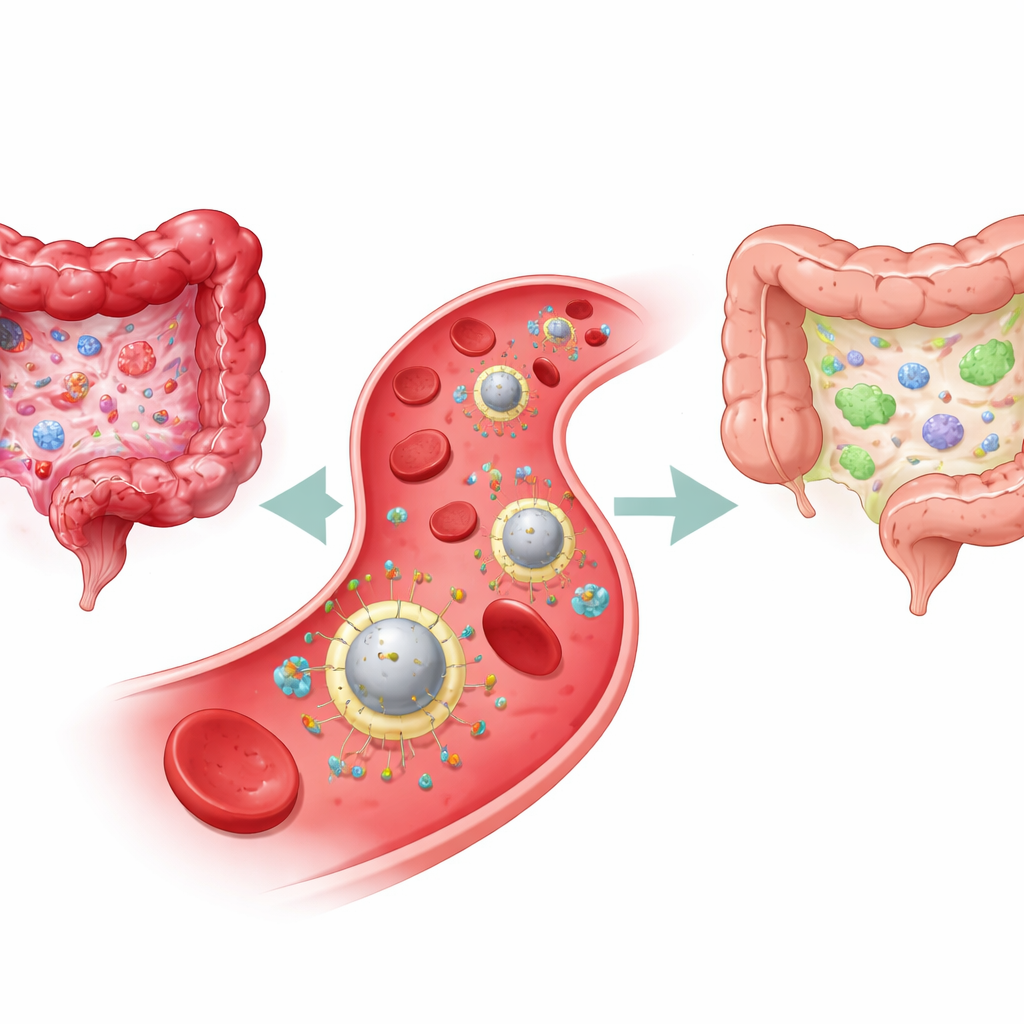
Pourquoi les traitements actuels sont insuffisants
La MII, qui comprend la maladie de Crohn et la rectocolite hémorragique, provient d’un bras de fer chronique au sein du système immunitaire intestinal. D’un côté se trouvent des cellules immunitaires agressives et des molécules inflammatoires qui endommagent la muqueuse intestinale ; de l’autre se trouvent des cellules régulatrices qui maintiennent normalement cette réponse sous contrôle. Les thérapies standards — comme les corticoïdes, les immunosuppresseurs et les médicaments biologiques — cherchent principalement à atténuer l’inflammation de façon systémique. Elles peuvent soulager les symptômes, mais elles restituent rarement l’équilibre immunitaire sous‑jacent, et une immunosuppression étendue peut augmenter le risque d’infections. Même les anticorps plus récents qui bloquent un signal inflammatoire clé, l’interleukine‑23 (IL‑23), ne bénéficient qu’à une partie des patients et circulent toujours largement, pas seulement là où ils sont nécessaires.
Concevoir un médicament ciblé et modulable
Les chercheurs ont voulu concevoir un traitement qui se comporte davantage comme une cellule vivante que comme un simple médicament. Ils sont partis de minuscules vésicules libérées naturellement par les cellules T régulatrices — des cellules immunitaires qui favorisent la tolérance et le maintien de la paix. Ces vésicules, appelées exosomes, transportent des protéines et du matériel génétique susceptibles d’inciter d’autres cellules immunitaires à adopter un mode apaisé. L’équipe a fusionné ces exosomes avec des fragments de membrane plaquettaire, empruntant aux plaquettes leur capacité à adhérer aux vaisseaux sanguins endommagés dans les tissus enflammés. Sur la surface de cette coque hybride, ils ont fixé des anticorps bloquant l’IL‑23 au moyen d’une « ficelle » moléculaire pouvant être coupée par des enzymes (métalloprotéinases matricielles) abondantes uniquement dans le tissu intestinal enflammé. Le résultat, nommé PrEXO‑a23, est une nanovésicule qui circule dans le sang, se fixe aux vaisseaux intestinaux lésés, puis libère son chargement d’anticorps uniquement là où la maladie est active.
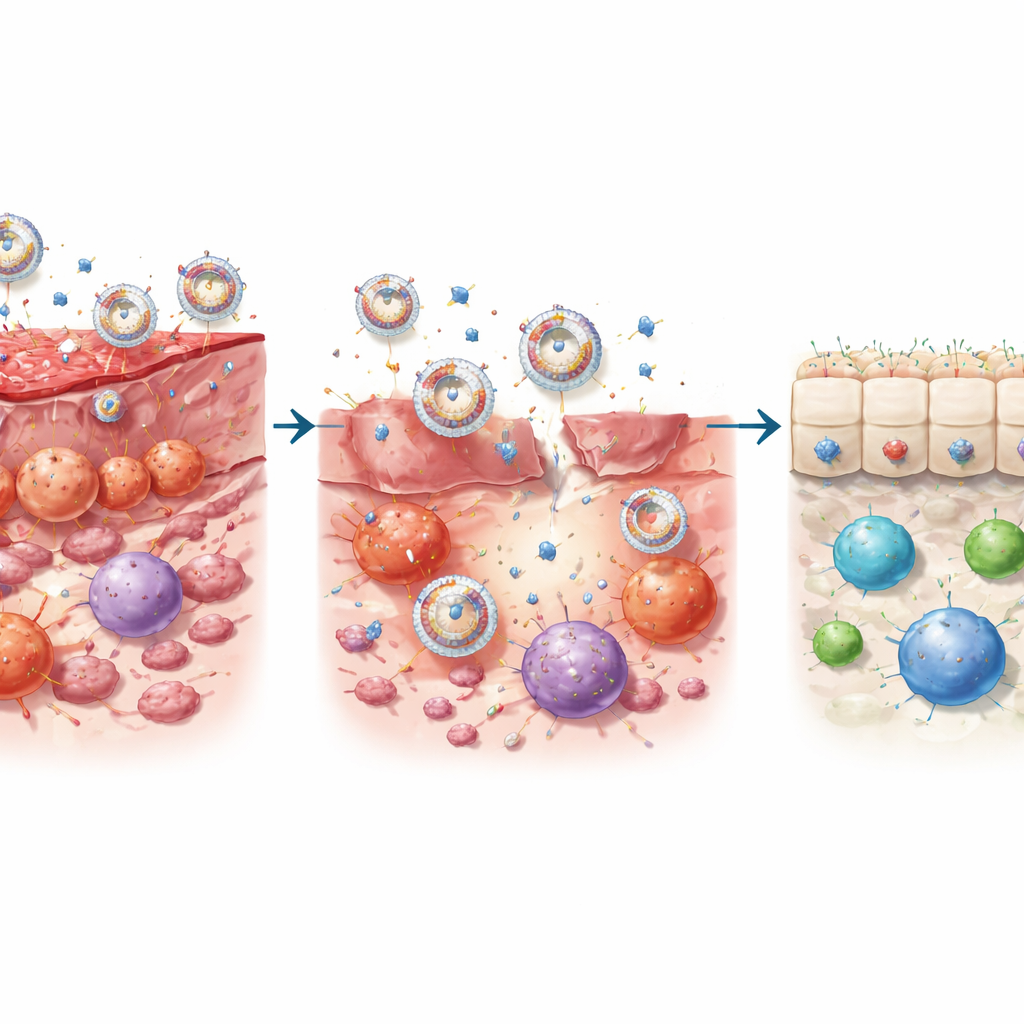
Rééduquer le voisinage immunitaire intestinal
Dans des études cellulaires, PrEXO‑a23 a surpassé soit l’anticorps seul soit les exosomes seuls. Il a fortement réduit la formation de cellules T auxiliaires 17 inflammatoires (Th17) et la libération de cytokines dommageables qui agressent la muqueuse intestinale, tout en protégeant les cellules épithéliales intestinales humaines de la mort. Parallèlement, il a poussé les cellules dendritiques — gardiennes qui instruisent les cellules T — à passer d’un état hostile et activateur à un état « tolérant » favorisant la croissance des cellules T régulatrices. Chez des souris modèles de colite, les nanovésicules se sont dirigées efficacement vers le tissu colique enflammé, ont été internalisées par plusieurs types de cellules immunitaires et ont libéré les anticorps en réponse à l’activité enzymatique locale. Cette double action — bloquer l’inflammation pilotée par l’IL‑23 et renforcer les signaux favorisant la tolérance — a ramené les marqueurs inflammatoires proches de la normale et a restauré un mélange de types de cellules T plus sain.
Réparer les tissus et prévenir les dommages à long terme
Les souris atteintes de colite induite chimiquement qui ont reçu PrEXO‑a23 ont moins perdu de poids, avaient des côlons plus longs et plus sains et présentaient moins d’augmentation de la taille de la rate, signe d’une inflammation systémique. L’examen microscopique a révélé une architecture intestinale préservée et des jonctions serrées entre les cellules épithéliales, indiquant une barrière réparée. Le traitement a également contribué à rééquilibrer le microbiote intestinal, augmentant des familles associées à la santé intestinale et réduisant celles liées à la maladie. Dans un modèle plus sévère qui imite la progression de la colite chronique vers le cancer du côlon, PrEXO‑a23 n’a pas seulement atténué l’inflammation en cours, il a complètement empêché le développement de tumeurs et limité l’épaississement et la cicatrisation de la paroi intestinale caractéristiques de la fibrose. Des analyses moléculaires ont pointé vers la restauration de la signalisation protectrice de p53 — un gardien central contre le cancer — qui s’est avérée importante pour l’effet anticancéreux.
Vers une prise en charge de la MII plus intelligente et plus durable
Pour un non‑spécialiste, le message clé est que ce travail va au‑delà de la simple « atténuation » de l’inflammation. En combinant une délivrance ciblée, une libération d’anticorps sur site et un contenu apaisant d’exosomes dans un seul minuscule système, PrEXO‑a23 calme la maladie active tout en aidant à réentraîner le système immunitaire vers une tolérance durable. Chez la souris, cela a conduit non seulement à un soulagement des symptômes mais aussi à une protection contre la cicatrisation et le cancer du côlon, deux des complications les plus redoutées d’une MII de longue date. Si de nombreux tests restent nécessaires avant qu’un tel traitement puisse atteindre les patients, l’étude illustre comment des nanomédicaments s’inspirant de la biologie pourraient un jour offrir un contrôle plus précis et durable de troubles immunitaires complexes comme la MII.
Citation: Cao, J., Luo, R., Miao, R. et al. Engineered exosome nanovesicles for delivery of antibodies to treat inflammatory bowel disease. Nat Commun 17, 2737 (2026). https://doi.org/10.1038/s41467-026-69382-4
Mots-clés: maladie inflammatoire de l’intestin, nanomédecine, tolérance immunitaire, exosomes, prévention du cancer colorectal