Clear Sky Science · fr
Les défauts structurels des fibrilles d’amyloïde-β stimulent la nucléation secondaire
Pourquoi de petites imperfections dans les protéines cérébrales comptent
Dans la maladie d’Alzheimer et les affections cérébrales apparentées, certaines protéines s’agglomèrent en longues structures filamenteuses appelées fibrilles amyloïdes. Ces fibrilles ne se contentent pas de marquer la maladie : elles favorisent aussi la génération de nouvelles particules protéiques hautement toxiques capables d’endommager les cellules nerveuses. Cette étude pose une question simple mais puissante : de rares « défauts » structurels à l’intérieur des fibrilles agissent-ils comme les principaux points chauds déclenchant une nouvelle croissance nuisible ? La réponse pourrait indiquer de nouvelles façons de ralentir ou d’arrêter ces troubles en ciblant seulement quelques sites critiques plutôt que toute la surface protéique. 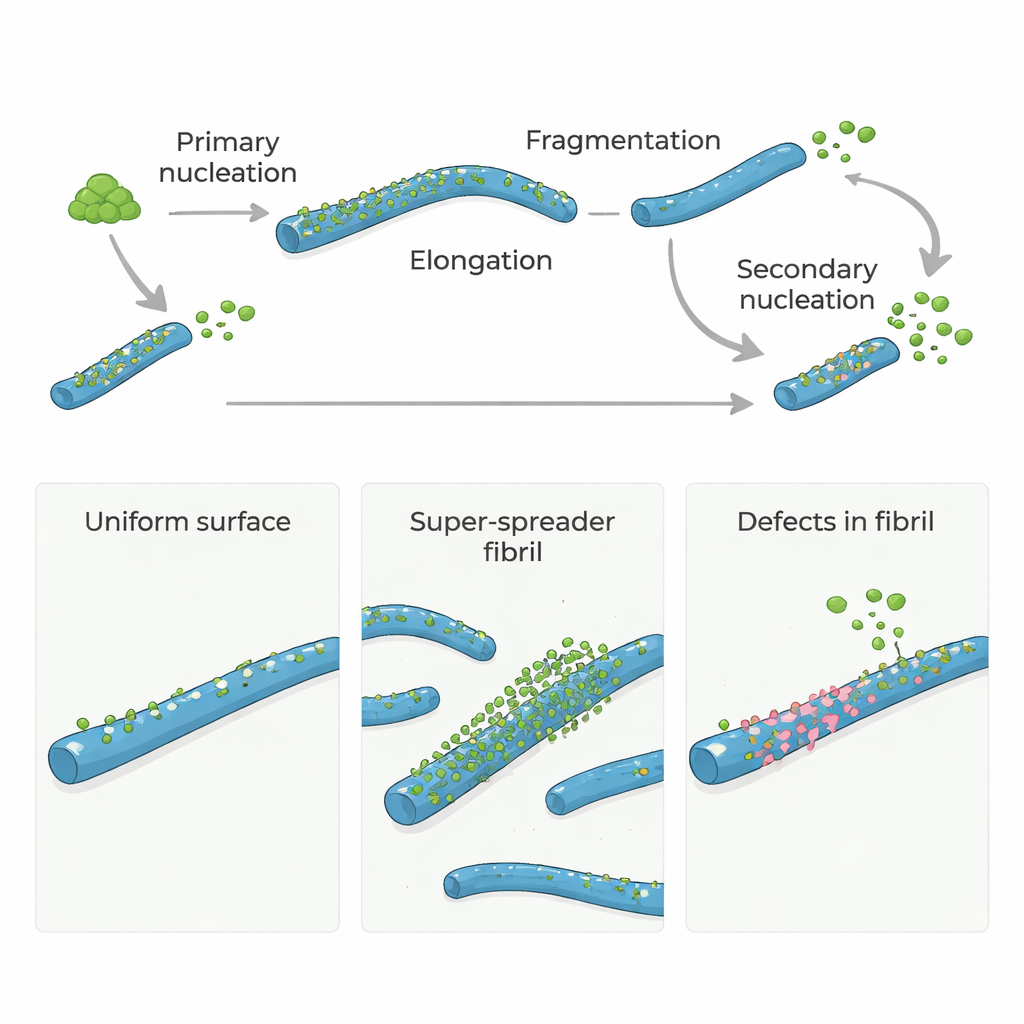
De la protéine inerte à la réaction en chaîne incontrôlée
Les protéines amyloïde-β (Aβ), centrales dans la maladie d’Alzheimer, ne forment pas rapidement des amas de façon autonome. Pour démarrer, quelques monomères doivent lentement s’assembler en les premières fibrilles minuscules, étape appelée nucléation primaire. Une fois ces fibrilles initiales présentes, elles croissent rapidement à mesure que d’autres monomères s’ajoutent à leurs extrémités. Et plus important encore, les fibrilles existantes peuvent induire l’apparition de nouvelles fibrilles sur leurs surfaces via un processus nommé nucléation secondaire. Cette étape pilotée par la surface peut inonder le système de nouvelles fibrilles et de petits oligomères toxiques, transformant un filet lent en une réaction en chaîne incontrôlée.
Toutes les surfaces de fibrilles sont-elles également dangereuses ?
De nombreux modèles supposaient que l’ensemble de la surface d’une fibrille amyloïde catalysait de la même façon la nucléation secondaire. Cependant, des expériences récentes laissaient entendre que seule une petite fraction de la surface est réellement active. Pour explorer cela, les auteurs ont utilisé un « chaperon » moléculaire naturel appelé Brichos, connu pour bloquer la nucléation secondaire de Aβ40 et Aβ42 (deux formes clés d’amyloïde-β). En mesurant avec précision la quantité de Brichos marqué par fluorescence qui se fixe aux fibrilles, ils ont observé qu’il se lie fermement mais en très faible nombre : environ une molécule de Brichos pour 100–150 molécules d’Aβ dans une fibrille. Pourtant, cette couverture parcimonieuse suffisait à supprimer plus de 90 % de la nucléation secondaire, ce qui signifie que seuls des sites rares et localisés — plutôt que la surface entière — dominent la production de nouveaux assemblages toxiques.
Examiner le rôle des défauts cachés
Ces résultats suggéraient que les sites de nucléation cruciaux pourraient être des défauts structurels : de petites irrégularités formées lors de la croissance des fibrilles, comme des couches mal alignées ou des noyaux internes partiellement exposés. Pour tester directement cette idée, les chercheurs ont fait croître des fibrilles d’Aβ40 dans deux conditions différentes. Un lot, les fibrilles « contrôle », a été formé en conditions fortement surgonflées favorisant une croissance rapide et le piégeage cinétique de défauts. L’autre lot a été créé à l’aide d’un protocole de recuit lent et contrôlé en température : les fibrilles ont été cultivées à une force motrice effective très faible, proche de leur limite de solubilité, où les structures incorrectes peuvent se dissoudre ou se réparer avant de se figer. La cryo-microscopie électronique à haute résolution a montré que les deux ensembles de fibrilles étaient essentiellement identiques en forme globale et en torsion, indiquant que le recuit n’a pas modifié la morphologie de base. 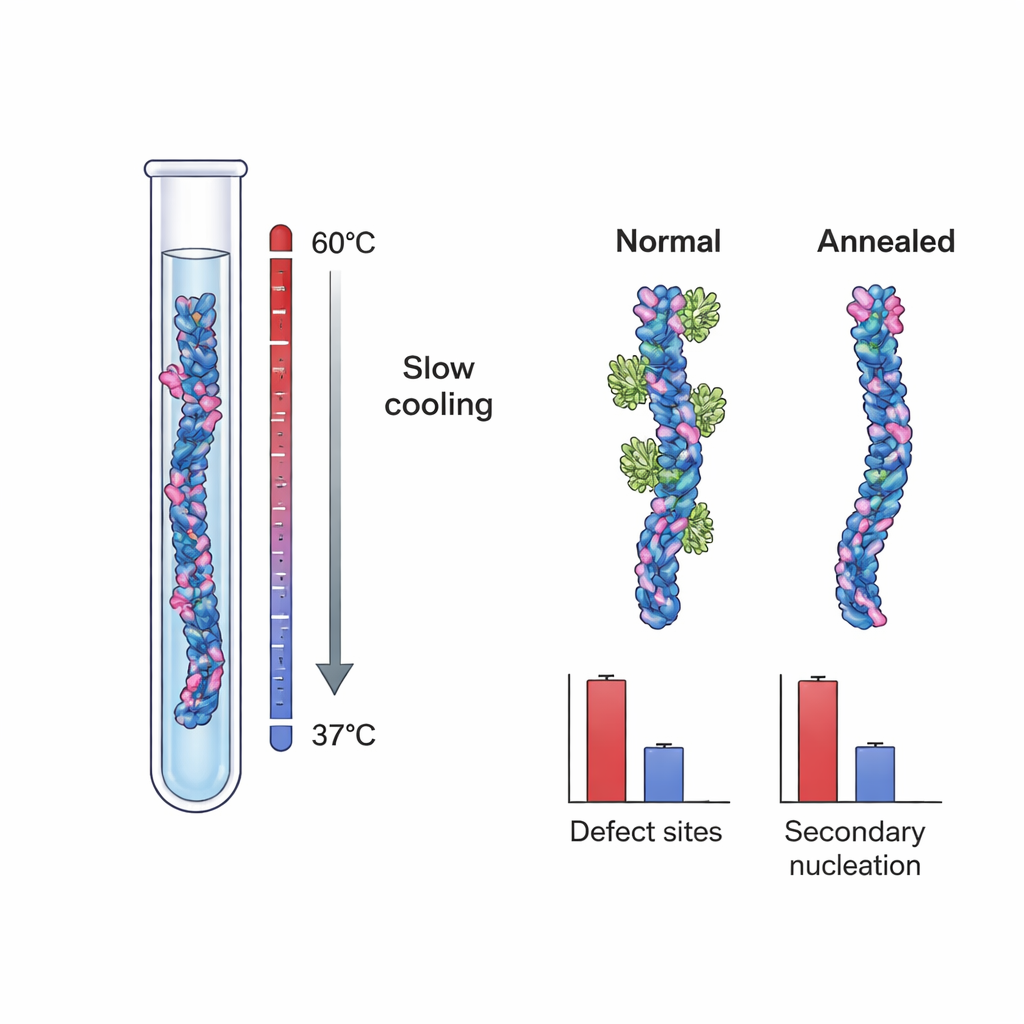
Moins de défauts, moins de sites de croissance dangereux
Lorsque l’équipe a mesuré la liaison du Brichos à ces deux types de fibrilles, elle a découvert une différence frappante. Les fibrilles Aβ40 contrôle présentaient environ un site de liaison pour le Brichos tous les ~100 monomères, indiquant à nouveau des sites rares mais importants. Les fibrilles recuites, en revanche, n’avaient qu’environ un site pour ~800 monomères — une réduction de fréquence des sites d’environ 90 %. Dans des expériences séparées où ces fibrilles étaient ajoutées comme « graines » à des solutions fraîches d’Aβ40, les fibrilles recuites étaient beaucoup moins efficaces pour déclencher une nouvelle agrégation, même lorsque leur masse totale était appariée à celle des fibrilles contrôle. Une modélisation cinétique détaillée a montré que cette baisse de pouvoir d’ensemencement ne pouvait pas s’expliquer simplement par des différences de longueur des fibrilles. Au contraire, elle concordait quantitativement avec le nombre réduit de sites de liaison au Brichos, soutenant fortement l’idée que les défauts de croissance agissent comme les principaux moteurs de la nucléation secondaire.
Un principe général porteur d’espoir thérapeutique
En combinant des arguments thermodynamiques, une réanalyse de travaux antérieurs et des comparaisons entre plusieurs protéines formant des amyloïdes, les auteurs soutiennent que de rares défauts de croissance sont vraisemblablement centraux dans la nucléation secondaire de nombreux systèmes, pas seulement de l’Aβ lié à Alzheimer. Ces défauts exposent partiellement le noyau interne étroitement empaqueté de la fibrille, offrant un échafaudage prêt à l’emploi où de nouveaux oligomères et fibrilles peuvent se former bien plus facilement que sur une surface lisse. Identifier ces défauts comme les coupables principaux ouvre de nouvelles voies pour la conception de médicaments. Plutôt que d’essayer de bloquer toutes les interactions possibles sur une surface de fibrille, les thérapies pourraient viser à protéger ou réparer uniquement ces rares sites défectueux, ou à réduire les conditions qui les génèrent. Concrètement, cela pourrait signifier diminuer la concentration effective des protéines formant des amyloïdes dans le cerveau ou concevoir des molécules, inspirées par Brichos, capables de reconnaître et neutraliser les points chauds de nucléation pilotés par des défauts. Si ces stratégies réussissent, elles pourraient couper la principale source d’oligomères toxiques et ralentir la progression des maladies liées aux amyloïdes.
Citation: Hu, J., Scheidt, T., Thacker, D. et al. Structural defects in amyloid-β fibrils drive secondary nucleation. Nat Commun 17, 1933 (2026). https://doi.org/10.1038/s41467-026-69377-1
Mots-clés: fibrilles amyloïdes, maladie d’Alzheimer, nucléation secondaire, agrégation protéique, chaperon Brichos