Clear Sky Science · fr
Mécanisme de « roaming » ultra‑rapide modulé par le solvant dans le bromoforme révélé par la diffusion X en solution en femtosecondes
Pourquoi de petites molécules dans l’eau et l’air comptent
Le bromoforme est une petite molécule produite naturellement qui a un impact environnemental important. Lorsque la lumière solaire atteint cette molécule dans l’atmosphère ou les embruns marins, elle peut libérer des atomes de brome qui contribuent à détruire l’ozone, la barrière qui nous protège des rayons ultraviolets nocifs du Soleil. Cette étude pose une question apparemment simple mais aux conséquences étendues : l’environnement liquide autour du bromoforme modifie‑t‑il ce qui se passe dans les premiers billionièmes de seconde après l’impact de la lumière, et donc change‑t‑il la quantité finale de brome destructeur d’ozone qui apparaît ?
La lumière qui rompt une molécule
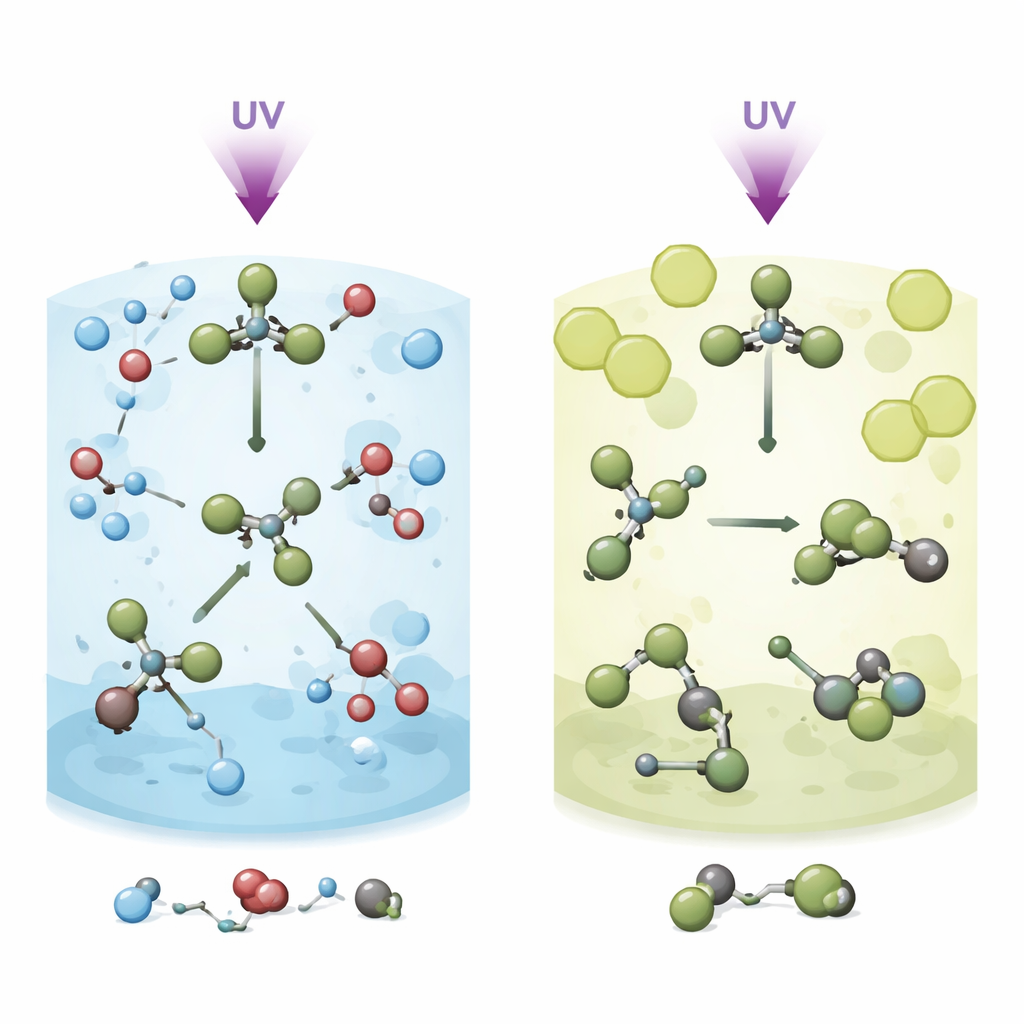
Les chercheurs commencent par éclairer le bromoforme dissous dans deux liquides différents par des impulsions ultracourtes d’ultraviolet : le méthanol, qui est polaire et chimiquement réactif, et le méthylcyclohexane, non polaire et relativement inerte. La lumière affaiblit rapidement l’une des liaisons carbone–brome du bromoforme, provoquant le début de la désintégration de la molécule. Mais au lieu de se séparer immédiatement, un atome de brome s’attarde et « roame » autour du fragment restant, CHBr₂. Ce mouvement de roaming crée une structure éphémère et réarrangée appelée isomère. L’énigme centrale est de savoir ce qu’il advient de cet intermédiaire en roaming dans différents solvants, et comment cette évolution contrôle si le bromoforme libère des atomes de brome libres ou est détourné vers d’autres produits.
Faire des films moléculaires avec des rayons X
Pour observer ces événements, l’équipe utilise la diffusion X en solution résolue en temps par femtosecondes au Laser à électron libre européen. Essentiellement, ils enregistrent un film stroboscopique montrant les variations des distances interatomiques en temps réel, avec une résolution en picosecondes et sous‑picosecondes. En comparant les motifs de diffusion mesurés avec des motifs générés par ordinateur pour de nombreuses structures possibles, ils reconstruisent l’évolution des longueurs de liaison et des angles au sein du bromoforme après excitation. Des techniques d’analyse avancées et des simulations accélérées par apprentissage automatique les aident à séparer des voies réactionnelles qui se recouvrent et à attribuer des durées de vie précises aux espèces à vie courte.
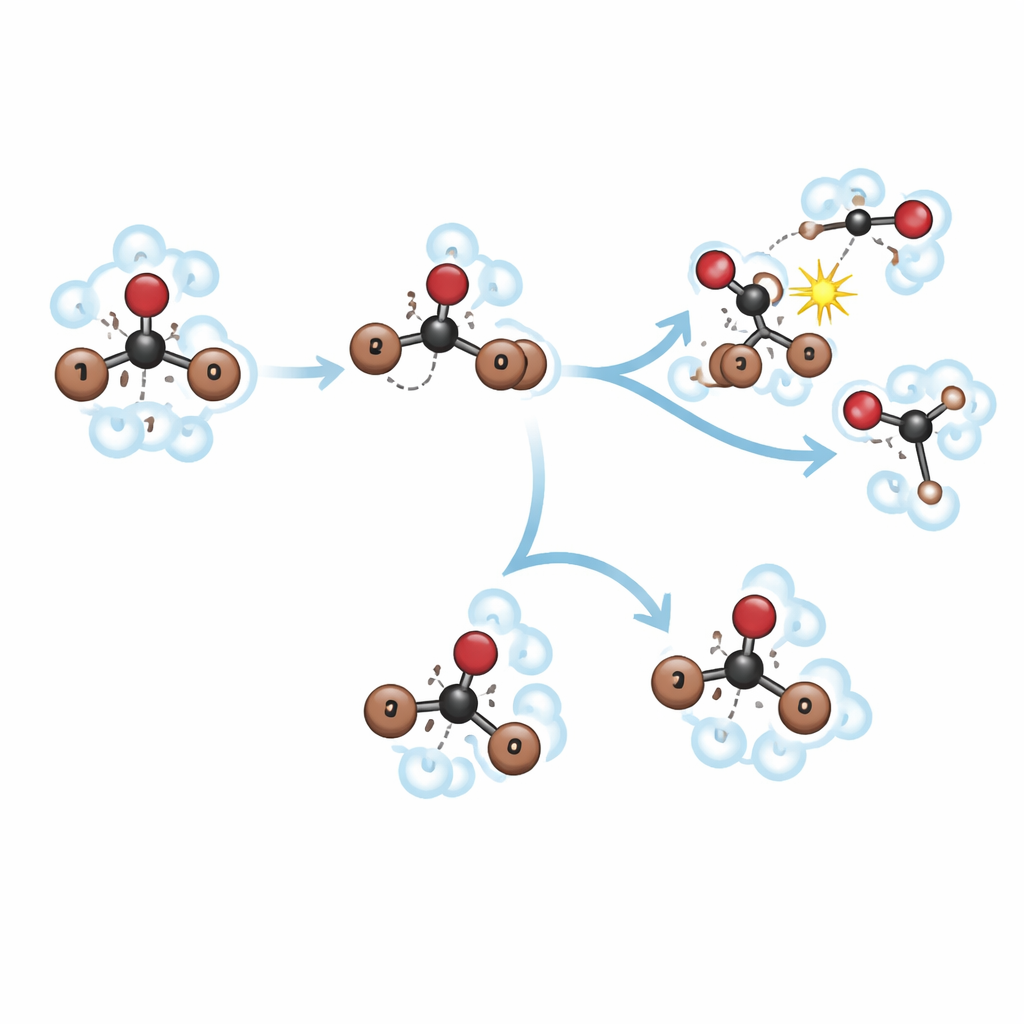
Deux solvants, deux destins très différents
Dans le méthanol, l’intermédiaire en roaming est présent mais de courte durée. Environ 150 femtosecondes après l’excitation, la liaison carbone–brome initiale se rompt, formant CHBr₂ et un brome en roaming. Au cours des ~400 femtosecondes suivantes, cet isomère chaud et vibrant s’étire et se plie à plusieurs reprises, ce qui met les fragments en contacts fréquents avec les molécules de méthanol environnantes. Au lieu de se relaxer en une forme réarrangée stable, la structure en roaming est rapidement interceptée par le méthanol dans une réaction de « méthanolyse ». Cela produit de nouvelles molécules, CH₃OCHBr₂ et HBr, tandis que des fragments libres CHBr₂ et Br issus d’une voie de dissociation plus directe continuent de réagir plus lentement sur plusieurs picosecondes. La « cage » moléculaire serrée du solvant et ses groupes hydroxyle réactifs agissent de concert pour orienter le bromoforme vers cette voie de réaction chimique plutôt que vers un isomère de longue durée de vie.
Quand le solvant recule et laisse le roaming durer
Dans le méthylcyclohexane, l’histoire change radicalement. Le même coup d’ultraviolet crée à nouveau un mouvement de roaming en ~150 femtosecondes, mais le liquide non polaire entoure le bromoforme de façon plus lâche et ne réagit pas facilement avec lui. Ici, le brome en roaming et le fragment CHBr₂ ont la liberté de se réorienter et de se stabiliser en une structure isomérique au lieu d’interagir immédiatement avec les molécules du solvant. La dissociation directe en fragments séparés CHBr₂ et Br se produit toujours et concurrence la formation d’isomères, mais désormais l’isomère réarrangé survit beaucoup plus longtemps. Les simulations montrent que la « cage » du solvant plus grande et plus souple dans le méthylcyclohexane favorise ce comportement de roaming analogue au gaz, tandis que la cage confinée et fortement interactive du méthanol canalise le même intermédiaire directement vers la réaction chimique.
Ce que cela implique pour l’ozone et au‑delà
Ensemble, ces expériences et calculs révèlent que le roaming est une étape précoce universelle lorsque le bromoforme absorbe de l’ultraviolet en milieu liquide, mais que le solvant environnant décide de la suite. Dans des milieux de type méthanol, le roaming sert principalement à déclencher des réactions très rapides avec le liquide, limitant la formation d’isomères de longue durée et déterminant l’apparition et le moment des produits porteurs de brome. Dans des environnements de type méthylcyclohexane, le roaming alimente plutôt une forme réarrangée de longue durée qui peut ensuite libérer du brome sur des échelles de temps différentes. En filmant directement ces mouvements ultrarapides, ce travail montre que le caractère microscopique des gouttelettes, aérosols et autres phases condensées peut contrôler fortement les voies chimiques des molécules d’intérêt pour l’ozone, aidant les scientifiques à construire des modèles plus précis de la photochimie atmosphérique et en solution.
Citation: Su, P., Zhang, J., Wang, H. et al. Ultrafast solvent-modulated roaming mechanism in bromoform revealed by femtosecond X-ray solution scattering. Nat Commun 17, 2514 (2026). https://doi.org/10.1038/s41467-026-69374-4
Mots-clés: bromoforme, mécanisme de roaming, photochimie ultrarapide, effets du solvant, appauvrissement de la couche d’ozone