Clear Sky Science · fr
Des ordres de liaisons hydrogène concurrents expliquent l’anomalie de la tension superficielle de l’eau
Pourquoi la surface de l’eau est plus étrange qu’elle n’en a l’air
La surface de l’eau permet aux insectes de marcher sur les étangs, façonne les gouttes de pluie et commande la formation et l’éclatement des bulles. Pourtant, quand les chercheurs mesurent combien cette surface est « serrée » — la tension superficielle — ils observent que l’eau se comporte de manière étonnamment étrange en se refroidissant, surtout lorsqu’elle est refroidie au-dessous de son point de congélation habituel. Cet article utilise des simulations numériques avancées pour révéler comment l’organisation cachée des molécules d’eau à la surface explique ce mystère ancien.
Deux types cachés d’eau liquide
Bien que nous percevions l’eau comme un liquide simple et homogène, ses molécules peuvent localement s’organiser de deux manières contrastées. Une organisation est plus compacte et désordonnée ; les auteurs l’appellent l’état ρ. L’autre est plus ouverte et symétrique, chaque molécule étant entourée selon une géométrie approximativement tétraédrique à quatre branches ; c’est l’état S. Des travaux antérieurs suggéraient que l’équilibre entre ces deux motifs locaux aide à expliquer nombre des propriétés étranges de l’eau en volume. Ici, les auteurs s’interrogent sur la façon dont cette image à deux états se manifeste à l’interface air–eau, où naît la tension superficielle.
Comment la surface aligne les molécules
À la frontière entre l’air et l’eau, les molécules ne subissent plus des forces égales en toutes directions. Cette brisure de symétrie favorise les molécules de l’état ρ dont les atomes d’hydrogène et les dipôles moléculaires peuvent facilement s’orienter dans une direction préférentielle. Les simulations montrent qu’autour de la température ambiante et en dessous, la toute première couche de surface devient encombrée par ces molécules ρ alignées, tandis que les molécules S sont plus fréquentes juste sous la surface et dans le volume. Parce que les molécules ρ s’alignent fortement, elles créent un déséquilibre des forces — une anisotropie des contraintes — qui génère une tension superficielle relativement élevée par rapport à des liquides ordinaires comme le benzène.
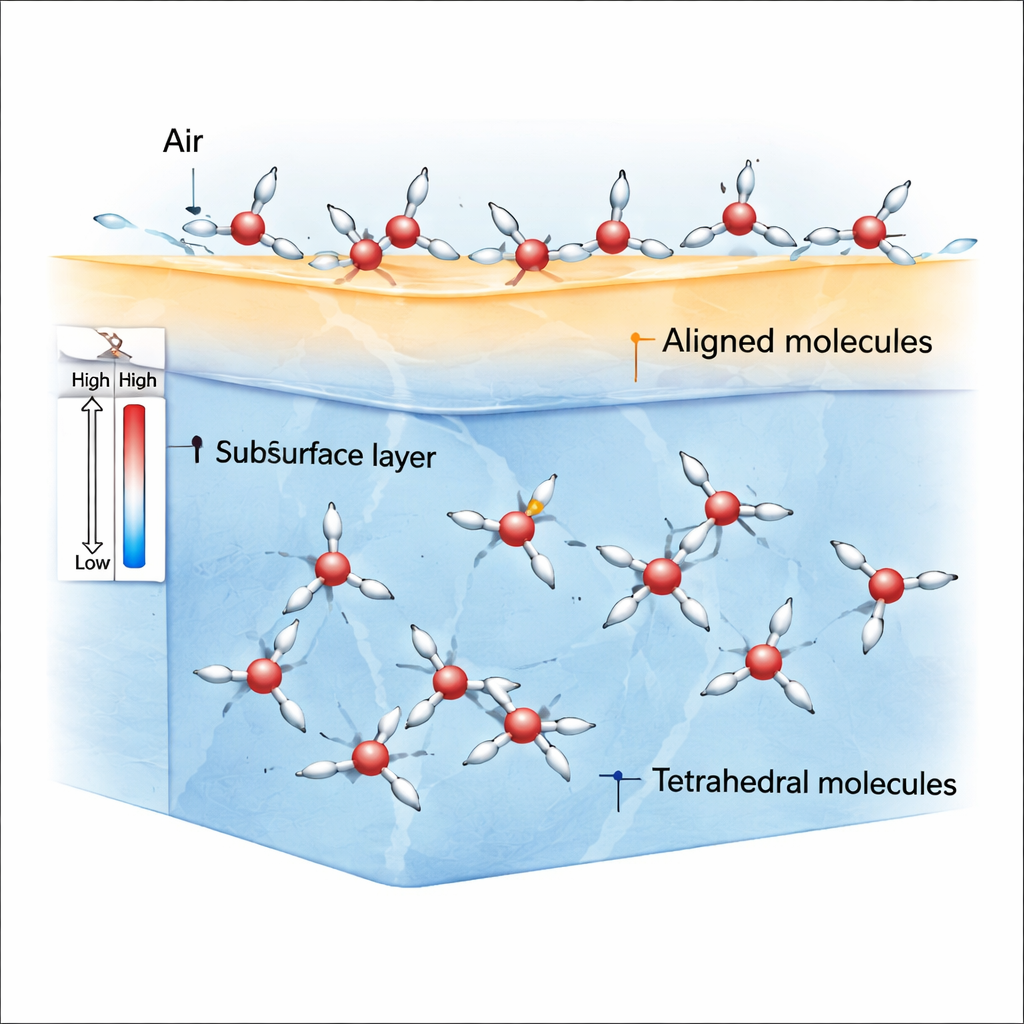
Pourquoi le refroidissement ralentit d’abord, puis accélère le renforcement de la surface
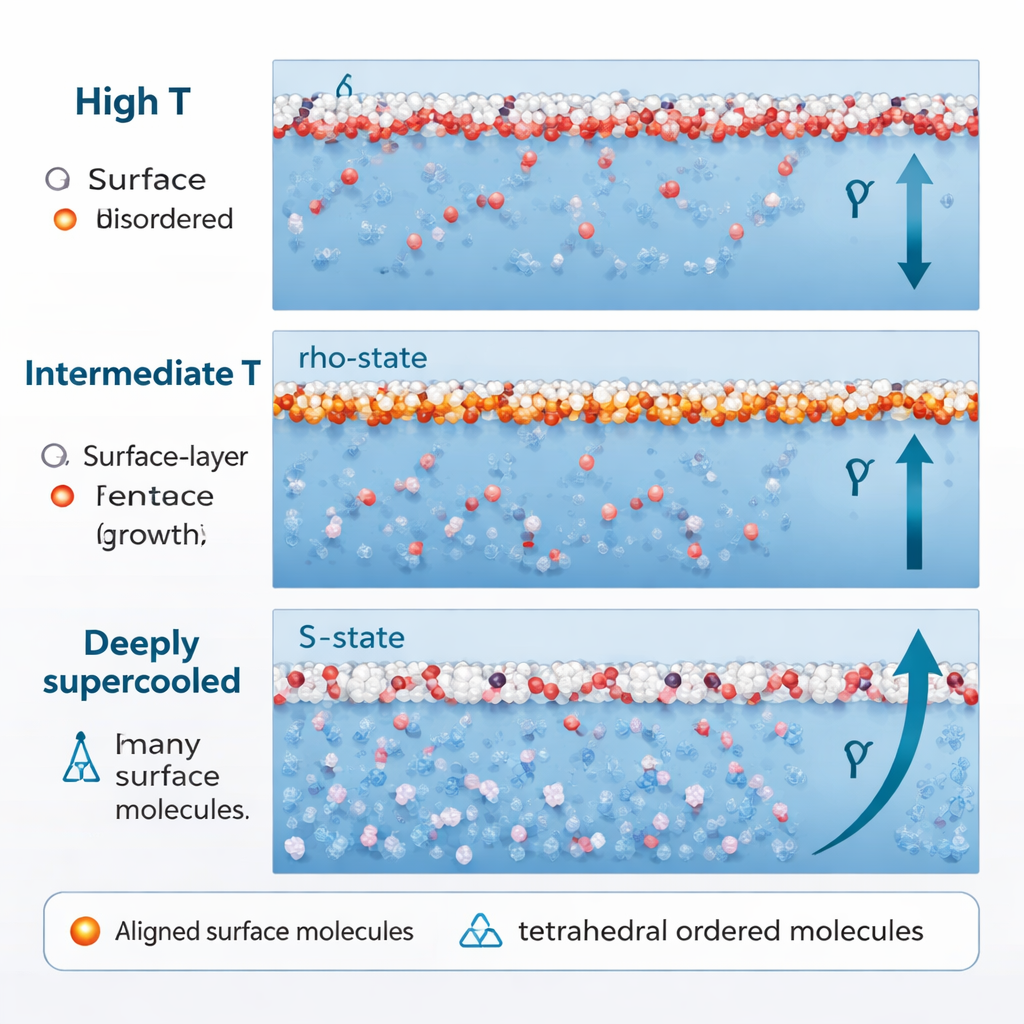
Dans la plupart des liquides simples, le refroidissement resserre régulièrement la surface, faisant augmenter la tension superficielle de façon presque linéaire. L’eau ne le fait que à des températures plus élevées. En se refroidissant vers environ −0,15 °C (275 K), la montée de la tension superficielle commence à ralentir. Les simulations montrent que ce ralentissement survient parce que les molécules ρ à la surface se sont déjà alignées au maximum ; un refroidissement supplémentaire modifie à peine leur contribution. Parallèlement, les molécules S sous la surface restent majoritairement orientées au hasard, de sorte qu’elles contribuent peu à l’augmentation des contraintes de surface. Le résultat net est une sorte de palier : la température continue de baisser, mais la tension superficielle croît uniquement de manière languissante.
Une surfroidissement profond déclenche un second renforcement
Lorsque l’eau est refroidie beaucoup plus loin, bien en dessous de son point de congélation normal, dans le régime profondément surfroidu (environ 250 K et moins), son comportement change à nouveau. La fraction de structures tétraédriques de l’état S augmente fortement, y compris près de la surface. Surtout, ces molécules S ne pointent plus dans des directions aléatoires. Leurs dipôles commencent à s’aligner le long de la direction perpendiculaire à la surface, entraînés par les interactions entre dipôles voisins et par une région de pression négative juste sous la surface. Une fois que cela se produit, l’eau en état S, qui auparavant avait tendance à assouplir la tension superficielle, commence à la renforcer. Cette contribution ordonnée supplémentaire produit une reprise plus rapide — l’augmentation « réentrante » — de la tension superficielle à basses températures.
Des énigmes de surface à la glace et au‑delà
Les mêmes amas tétraédriques de l’état S qui rigidifient la surface à basse température ressemblent aussi aux premiers éléments constitutifs de certaines formes de glace, et les simulations montrent qu’ils sont enrichis près de l’interface. Cela signifie que la frontière air–eau peut servir de berceau pour la formation de la glace, contribuant à expliquer pourquoi la congélation commence souvent aux surfaces. Plus largement, ce travail établit un lien concret, au niveau moléculaire, entre la façon dont les molécules d’eau s’organisent et s’orientent et la force avec laquelle la surface s’attire vers l’intérieur. Ce tableau structurel–mécanique résout non seulement la courbe de température étrange de la tension superficielle de l’eau, mais offre aussi une feuille de route pour comprendre et contrôler les phénomènes interfaciaux dans d’autres liquides formant des réseaux, de l’eau surfondue dans les nuages aux matériaux employés en technologie et en biologie.
Citation: Yuan, J., Qiu, K., Sun, G. et al. Competing hydrogen-bond orders drive water’s anomalous surface tension. Nat Commun 17, 1498 (2026). https://doi.org/10.1038/s41467-026-69356-6
Mots-clés: tension superficielle de l’eau, liaison hydrogène, eau surfondue, structure du liquide, nucléation de la glace