Clear Sky Science · fr
STING synergie avec TOX pour supprimer l’expression de HO-1 et déclencher la ferroptose dans les cellules T CD8+ infiltrant la tumeur et la résistance à l’immunothérapie
Pourquoi cette recherche est importante pour le traitement du cancer
Les immunothérapies anticancéreuses modernes fonctionnent en libérant les cellules T cytotoxiques de l’organisme, mais de nombreuses tumeurs trouvent encore des moyens de neutraliser ces cellules. Cette étude met au jour un interrupteur d’autodestruction caché à l’intérieur des cellules T CD8+ « tueuses » que les tumeurs exploitent, et montre comment désactiver cet interrupteur peut rendre l’immunothérapie beaucoup plus efficace.
Une voie de mort cachée à l’intérieur des cellules T anti-tumorales
Dans une tumeur, les cellules T CD8+ sont censées traquer et détruire les cellules cancéreuses. Pourtant, elles deviennent souvent rares, lentes et de courte durée de vie. Les auteurs se sont concentrés sur deux molécules présentes dans les cellules T — STING, un détecteur de dommages à l’ADN, et TOX, une protéine liée à l’épuisement des cellules T. Ils ont conçu des souris dont les cellules T CD8+ étaient dépourvues de STING, de TOX, ou des deux, puis ont implanté plusieurs types de tumeurs. De manière surprenante, les souris dont les cellules T étaient déficientes en STING ou en TOX ont éliminé les tumeurs bien mieux. Leurs tumeurs croissaient plus lentement, contenaient beaucoup plus de cellules T CD8+, et ces cellules produisaient davantage de molécules cytotoxiques comme l’interféron-gamma et la granzyme B. Cela a mis en évidence un programme interne qui sabote silencieusement les cellules T à l’intérieur des tumeurs.
Comment la mort cellulaire induite par le fer affaiblit l’immunité
En examinant l’activité génique des cellules T infiltrant les tumeurs, les chercheurs ont constaté que les cellules T normales à l’intérieur des tumeurs étaient préparées à une forme particulière de mort cellulaire appelée ferroptose. Contrairement à l’apoptose, la ferroptose est déclenchée par une surcharge en fer et l’accumulation de lipides oxydés dans les membranes cellulaires. Dans les cellules T CD8+ ordinaires exposées aux cellules tumorales, les gènes favorisant l’accumulation de fer et les dommages lipidiques étaient activés, tandis que les gènes protecteurs étaient réprimés. En revanche, les cellules T déficientes en STING ou TOX montraient le schéma inverse : elles exprimaient davantage d’enzymes protectrices HO-1 et GPX4, présentaient des niveaux de fer plus faibles, moins de peroxydation lipidique, des mitochondries en meilleure santé et résistaient à la mort par ferroptose. Des tests en laboratoire ont confirmé que bloquer chimiquement la ferroptose maintenait en vie les cellules T normales, tandis que la suppression de STING ou TOX les rendait naturellement résistantes.
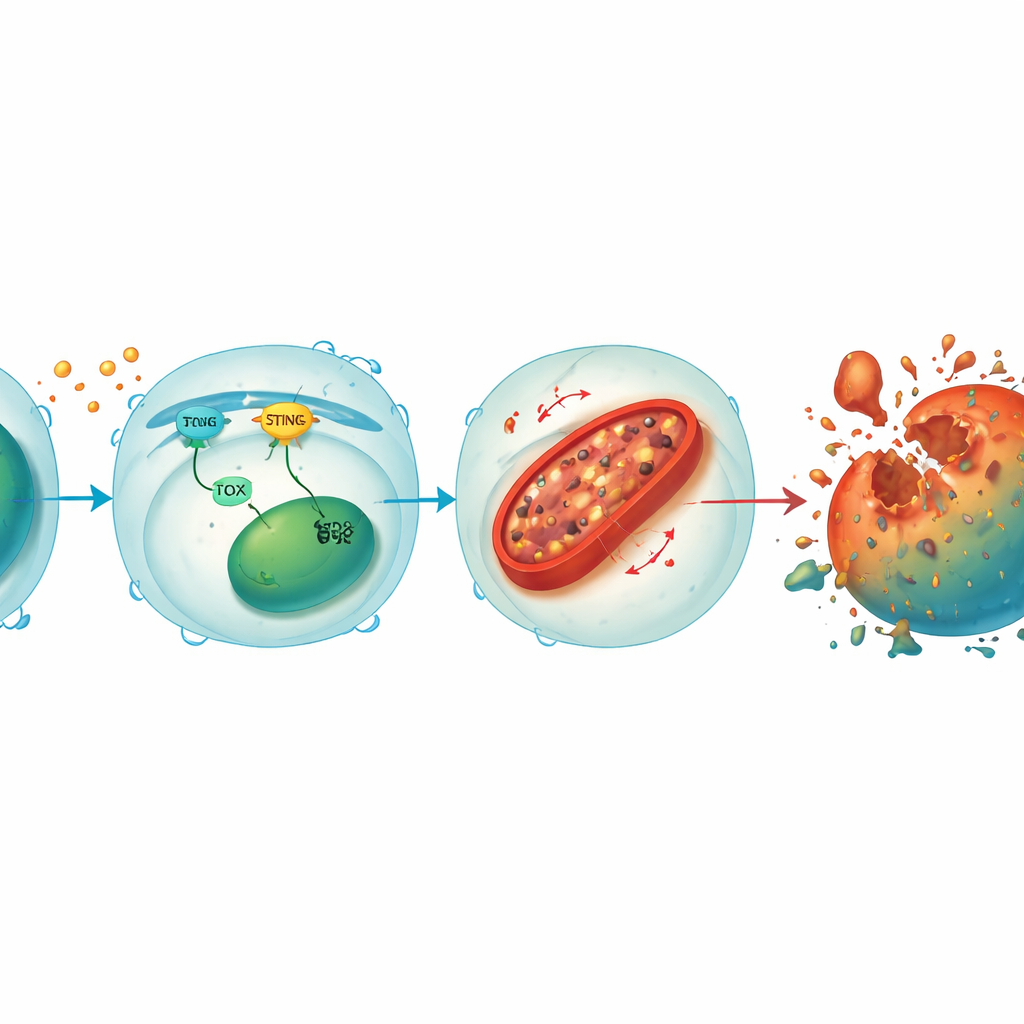
Une boucle liant signaux de stress et dommages mitochondriaux
En approfondissant, l’équipe a découvert que STING et TOX forment une boucle d’amplification au sein des cellules T CD8+. Lorsque des signaux tumoraux ou viraux activent STING, cela déclenche des facteurs en aval qui renforcent TOX, et TOX à son tour contribue à maintenir l’activité de STING. Ensemble, ils suppriment HO-1, une enzyme qui aide normalement à réguler le fer cellulaire. Avec HO-1 réprimé, le fer s’accumule dans les mitochondries — les centrales énergétiques de la cellule — conduisant à des niveaux élevés de molécules réactives et à l’oxydation des lipides membranaires. Ces dommages mitochondriaux épuisent la production d’énergie et poussent finalement la cellule T vers la ferroptose. La restauration de STING ou TOX dans des cellules T knock-out rétablit la surcharge en fer et la mort cellulaire, tandis qu’une nouvelle diminution de HO-1 rendait même les cellules T protégées vulnérables, soulignant le rôle central de HO-1 comme frein sur cette voie destructrice.
Comment le lactate tumoral appuie sur la gâchette
Le microenvironnement tumoral est riche en lactate, un sous-produit du métabolisme altéré du cancer. L’étude montre que ce lactate n’est pas simplement un déchet métabolique — il aide activement à basculer l’interrupteur de la ferroptose dans les cellules T. Comparées à d’autres cellules, les cellules T CD8+ étaient particulièrement sensibles au lactate. Lorsque le lactate entrait dans les cellules via des transporteurs spécifiques, il provoquait une accumulation de fer, le rétrécissement des mitochondries, une perte d’ADN mitochondrial et davantage de dommages oxydatifs. En parallèle, le lactate augmentait l’activité de STING et TOX et supprimait encore HO-1. Les cellules T dépourvues de STING ou TOX étaient beaucoup plus résistantes aux lésions induites par le lactate. Bloquer un transporteur clé du lactate avec un médicament (AZD3965) protégeait les cellules T CD8+ de la ferroptose chez la souris, augmentait leur présence dans les tumeurs et ralentissait la croissance tumorale, reproduisant l’effet bénéfique de la suppression génétique de STING dans les cellules T.
Transformer une vulnérabilité en avantage thérapeutique
Ces éclairages mécanistiques ont des implications pratiques. Lorsque les chercheurs ont utilisé la thérapie cellulaire adoptive — en injectant des souris avec des cellules T activées en laboratoire — ils ont constaté que des cellules T conçues pour être dépourvues de STING ou TOX contrôlaient la tumeur bien mieux que des cellules T normales. De plus, combiner ces cellules T « résistantes à la ferroptose » avec des traitements existants tels que les inhibiteurs de points de contrôle PD-1 ou TIM-3, la chimiothérapie au cisplatine, ou un activateur de STING donnait une régression tumorale nettement supérieure à celle obtenue par chaque thérapie seule. Enfin, dans des prélèvements tumoraux de patientes atteintes d’un cancer du col de l’utérus, des niveaux plus élevés de TOX et plus faibles de HO-1 dans les lymphocytes infiltrant la tumeur étaient associés à une survie plus mauvaise, ce qui suggère que cette voie influence aussi les résultats cliniques chez l’humain.
Ce que cela signifie pour les soins contre le cancer à venir
En termes simples, l’étude révèle que les tumeurs peuvent forcer nos meilleures cellules T anti-cancer à « rouiller » de l’intérieur en déclenchant une forme de mort cellulaire alimentée par le fer. Un circuit lactate–STING–TOX réduit la protection assurée par HO-1, endommage les mitochondries et conduit à la ferroptose, amenuisant les rangs des cellules T CD8+ efficaces. Perturber ce circuit — en concevant des cellules T dépourvues de STING ou TOX, en renforçant HO-1, ou en bloquant l’entrée du lactate — maintient les cellules T en vie, énergétiques et prêtes à attaquer. Ce travail ouvre la voie à des immunothérapies de nouvelle génération qui combinent un réglage métabolique et génétique des cellules T avec des médicaments existants pour surmonter la résistance et obtenir un contrôle tumoral plus durable.
Citation: Zhu, Q., Zhang, Jb., Nie, Cp. et al. STING synergizes with TOX suppressing HO-1 expression to trigger ferroptosis in tumor-infiltrating CD8+ T cell and immunotherapy resistance. Nat Commun 17, 2543 (2026). https://doi.org/10.1038/s41467-026-69350-y
Mots-clés: immunothérapie anticancéreuse, cellules T CD8, ferroptose, microenvironnement tumoral, voie STING TOX HO-1