Clear Sky Science · fr
Seq-Scope-eXpanded : omique spatiale au‑delà de la résolution optique
Voir les cellules avec plus de précision
Nos corps sont constitués d'innombrables petites cellules, chacune animée d'activités que l'on ne peut généralement pas voir, même avec des microscopes puissants. Cet article présente Seq-Scope-X, une technologie qui permet aux chercheurs de zoomer sur le fonctionnement interne des tissus avec une clarté sans précédent, en cartographiant quels gènes et quelles protéines sont actifs à des emplacements précis à l'intérieur et entre les cellules. Ce niveau de détail pourrait transformer la façon dont nous étudions le développement, le système immunitaire et des maladies comme le cancer ou les lésions hépatiques.
Pourquoi cartographier les molécules in situ ?
Les cellules ne fonctionnent pas isolément : elles vivent en voisinages, forment des couches et se spécialisent selon leur position. Les méthodes traditionnelles de séquençage brisent les tissus, faisant perdre ce contexte spatial. Les outils plus récents d'« omique spatiale » conservent les molécules en place, mais il y a eu un compromis. Les méthodes basées sur l'imagerie voient des détails très fins mais suivent généralement un nombre limité de gènes. Les méthodes fondées sur le séquençage peuvent lire presque tous les gènes à la fois, mais elles estompent les caractéristiques fines, brouillant souvent les signaux sur plusieurs micromètres — plus grand que de nombreuses structures subcellulaires. Les auteurs se sont donnés pour objectif de combler cet écart : conserver la richesse et l'absence de biais du séquençage, tout en atteignant ou dépassant la netteté des microscopes modernes.
Étendre le tissu pour dépasser les limites optiques
L'idée centrale de Seq-Scope-X est d'une simplicité trompeuse : agrandir délicatement le tissu lui‑même afin que chaque nanomètre d'origine devienne plus facile à résoudre. L'équipe ancre d'abord les molécules d'ARN — ou des tags ADN spéciaux liés à des anticorps — dans un hydrogel souple construit autour de la coupe de tissu. Ils digèrent ensuite le tissu d'origine et gonflent le gel dans une solution salée, étirant physiquement l'ensemble d'environ trois fois tout en conservant presque intactes les positions relatives. Ce gel expansé est ensuite déposé sur une puce de séquençage ultra‑dense recouverte de sondes de capture. En chauffant soigneusement l'assemblage, les molécules ancrées se détachent du gel et se réattachent à la puce, qui peut alors être séquencée pour révéler quels gènes ou protéines étaient présents à chaque coordonnée minuscule. 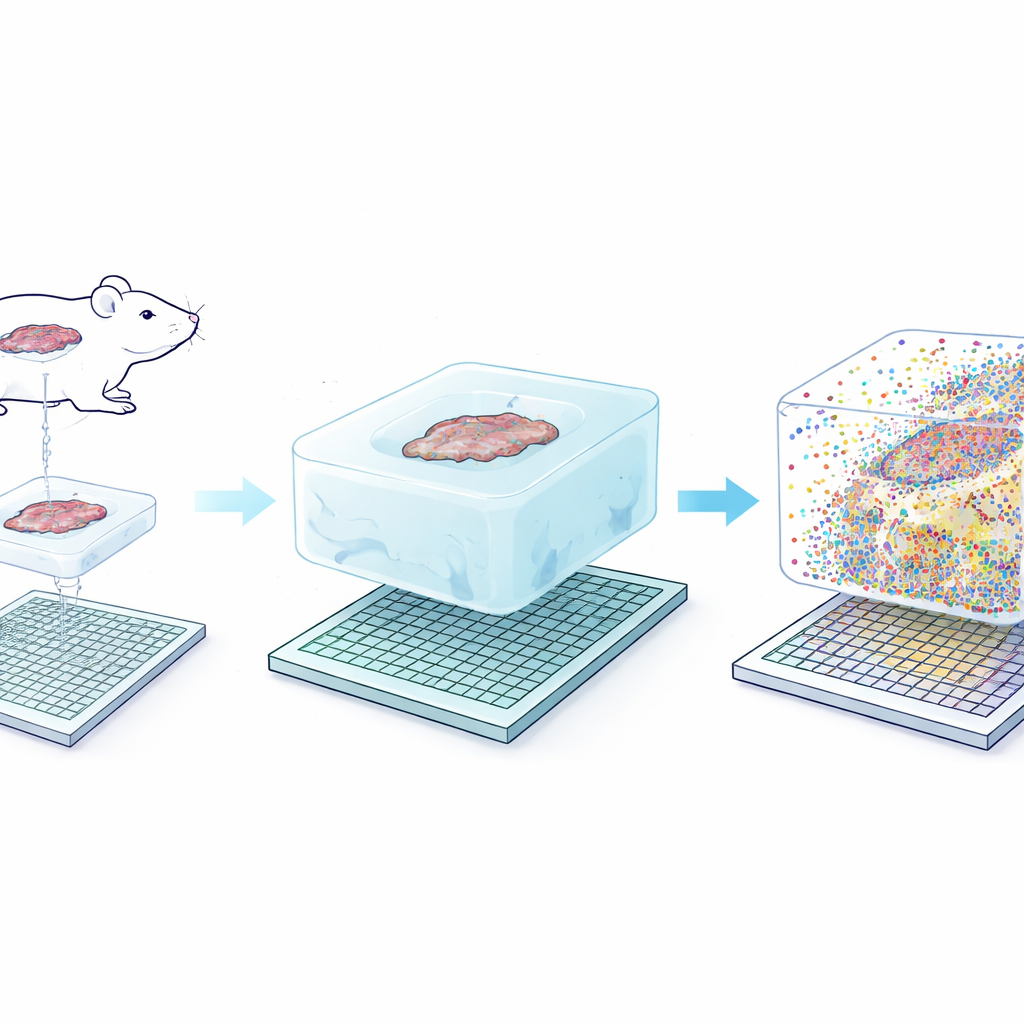
De cellules floues à des cartes subcellulaires
Lorsque les chercheurs ont appliqué Seq-Scope-X au foie de souris, ils ont constaté que la méthode affinait la résolution spatiale d'environ 0,6 micromètre à environ 0,2 micromètre et augmentait le nombre de positions mesurables par millimètre carré de près de dix fois. En termes pratiques, ce qui ressemblait auparavant à des taches floues de signal est devenu des contours nets de cellules individuelles. Plus frappant encore, des amas d'ARN non encore entièrement traités (non épissés) se sont alignés précisément avec les centres des noyaux, tandis que l'ARN mature (épissé) retraçait le cytoplasme environnant. Cela a permis aux auteurs de délimiter les frontières cellulaires en utilisant uniquement l'ARN et de séparer les lectures géniques nucléaires et cytoplasmiques pour presque chaque hépatocyte du tissu, ce que les méthodes de séquençage précédentes ne faisaient que suggérer.
Cellules aux personnalités partagées
Avec cette nouvelle clarté, l'équipe a découvert une forme inattendue de « double vie » moléculaire à l'intérieur des cellules hépatiques. Le long du gradient bien connu allant des vaisseaux sanguins du côté portal de l'acinus hépatique à ceux du côté central, les hépatocytes se spécialisent dans différentes tâches métaboliques. Seq-Scope-X a montré que, dans de nombreuses cellules, le profil génique du noyau ne correspondait pas au profil du cytoplasme environnant. Environ un tiers des hépatocytes semblaient présenter un profil nucléaire aligné sur une zone et un profil cytoplasmique aligné sur une zone voisine. Des méthodes d'imagerie indépendantes, incluant MERFISH et des essais de fluorescence pour ARN monomoléculaire, ont confirmé que des transcrits individuels peuvent se concentrer soit dans le noyau soit dans le cytoplasme. Ensemble, ces observations suggèrent que les hépatocytes peuvent modifier dynamiquement leurs rôles métaboliques au fil du temps, le noyau préparant un état futur tandis que le cytoplasme reflète l'état actuel. 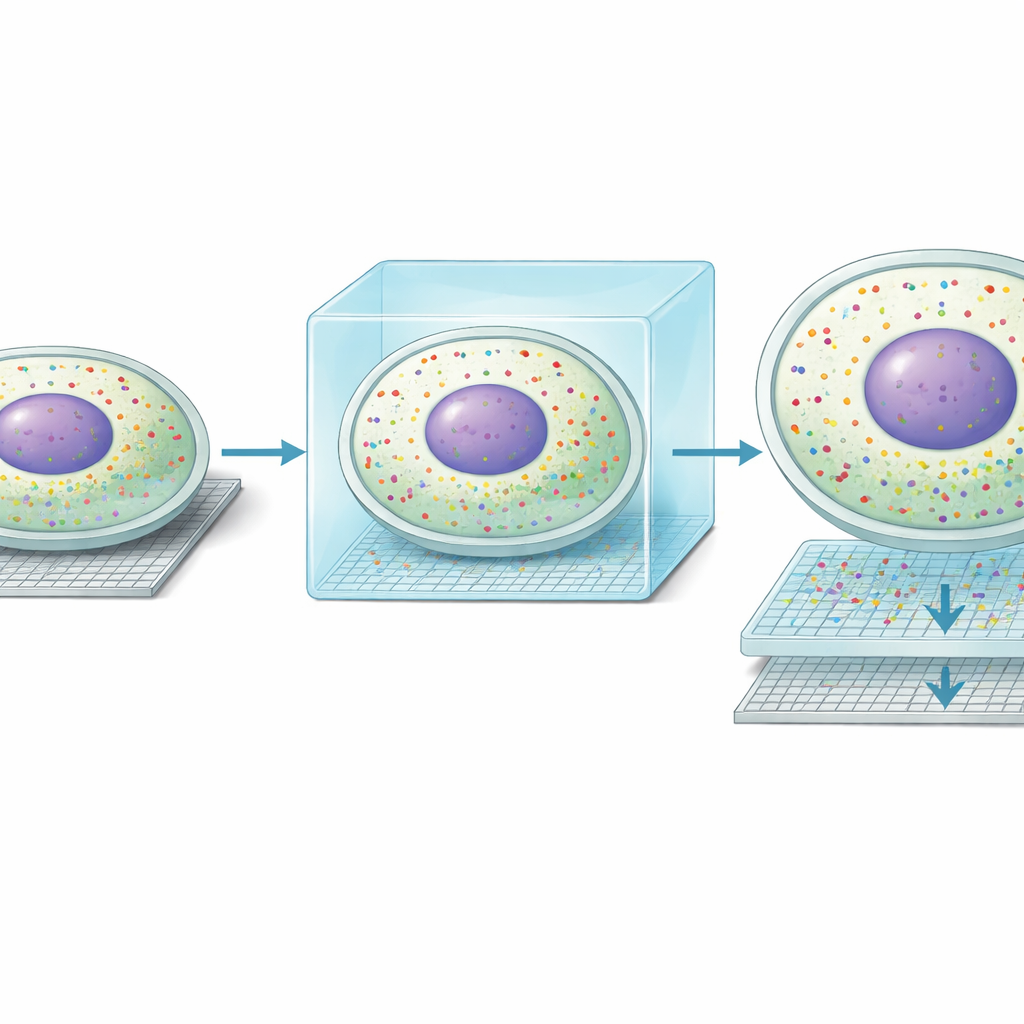
Au‑delà du foie : cerveau, intestin et tissus immunitaires
Les auteurs ont ensuite testé si Seq-Scope-X fonctionnait dans d'autres organes. Dans le cerveau, il a séparé clairement différents types de neurones et cellules de soutien et révélé des motifs subcellulaires d'ARN autour des noyaux. Dans le côlon, il a distingué des sous‑types de cellules caliciformes et des couches de colonocytes le long de l'axe cryptes‑surface, capturant à nouveau des signatures nucléaires. Peut‑être de façon plus spectaculaire, l'équipe a adapté la méthode aux protéines en utilisant des anticorps codés par ADN dans la rate de souris et les amygdales humaines. Seq-Scope-X a pu cartographier simultanément plus d'une centaine de marqueurs de surface cellulaire à résolution unicellulaire, distinguant des sous‑ensembles de cellules T et B très proches et des cellules myéloïdes. En passant à une chimie de gel plus extensible, ils ont poussé la résolution effective vers le véritable nanoscopique, tout en préservant suffisamment l'architecture tissulaire pour des cartographies détaillées.
Ce que cela implique pour l'avenir
Seq-Scope-X montre que l'élargissement physique des tissus avant le séquençage peut surmonter des limites de résolution anciennes, offrant un détail presque équivalent à celui du microscope tout en lisant simultanément des milliers de gènes ou d'étiquettes protéiques. Pour un observateur profane, cela signifie que les scientifiques peuvent désormais construire des « atlas moléculaires » qui non seulement indiquent où se trouvent les cellules, mais révèlent aussi ce qui se passe à l'intérieur de différentes parties de chaque cellule. De telles cartes pourraient aider à expliquer comment les tissus réagissent aux blessures, comment les cellules immunitaires s'organisent dans les organes lymphoïdes et les tumeurs, ou comment des changements subtils à l'intérieur des cellules annoncent une maladie. Bien que des améliorations restent nécessaires pour étendre la couverture et optimiser certains panels de marquage, Seq-Scope-X ouvre une nouvelle fenêtre puissante sur les paysages microscopiques qui sous‑tendent la santé et la maladie.
Citation: Anacleto, A., Cheng, W., Feng, Q. et al. Seq-Scope-eXpanded: spatial omics beyond optical resolution. Nat Commun 17, 2564 (2026). https://doi.org/10.1038/s41467-026-69346-8
Mots-clés: transcriptomique spatiale, expansion tissulaire, omique unicellulaire, protéomique spatiale, zonation hépatique