Clear Sky Science · fr
La photosensibilisation « sur eau » permet l’acylation et l’alkylation redox‑neutres des quinones
L’eau au service de la chimie verte
Les chimistes admirent depuis longtemps la manière dont la nature utilise l’eau comme un milieu de réaction sûr et efficace à l’intérieur des cellules vivantes. Cette étude s’inspire de cette idée et montre comment l’eau ordinaire, associée à la lumière visible d’LED simples, peut piloter des réactions utiles de formation de liaisons carbone–carbone. Le travail révèle que la surface où se rencontrent l’huile et l’eau n’est pas seulement une frontière : elle peut agir comme un minuscule réacteur auto‑assemblé qui rend des transformations difficiles plus propres, plus douces et plus polyvalentes.
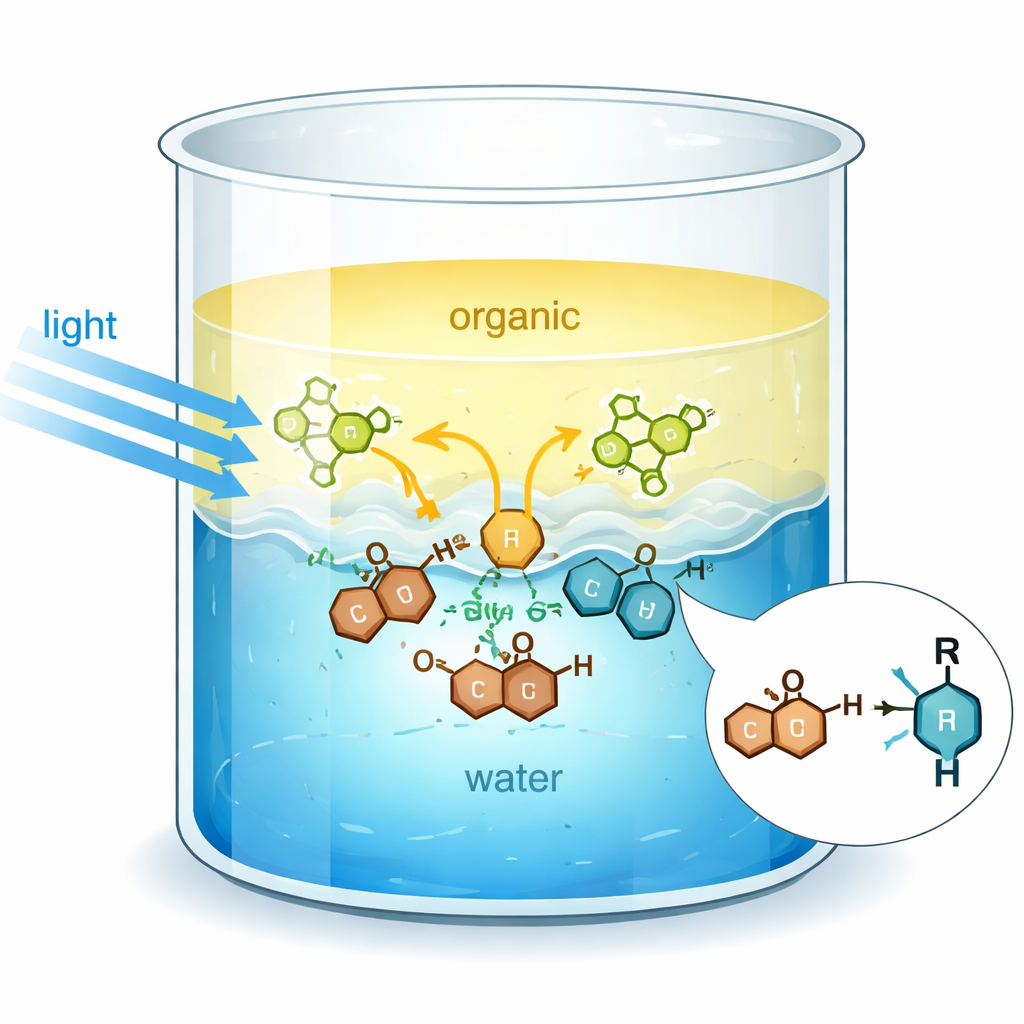
Une frontière animée entre l’huile et l’eau
Quand on agite de l’huile et de l’eau, elles se séparent en deux couches, mais la surface qu’elles partagent devient un environnement fortement organisé. Les molécules d’eau y forment un réseau dense de liaisons hydrogène, créant une interface structurée et robuste. Les auteurs montrent que cette interface peut aider les réactions organiques de plusieurs façons : elle rassemble des molécules autrement mal mélangées, augmente leur concentration locale et modifie subtilement leurs propriétés électroniques. En particulier, des réactifs clés appelés quinones — des molécules en anneau apparentées à de nombreux produits naturels et médicaments — interagissent avec l’eau à la surface de sorte que leurs états excités électroniques sont stabilisés et déplacés vers des énergies plus faibles.
Transformer la lumière en travail chimique
Pour capter efficacement la lumière visible, l’équipe utilise une teinture commune, l’Eosin Y, comme photosensibilisateur. Dans des conditions normales, les quinones absorbent principalement les ultraviolets, qui sont plus agressifs et peuvent dégrader les produits. À l’interface eau‑organique, cependant, les niveaux d’énergie de la quinone et de l’Eosin Y se déplacent de manière opposée mais complémentaire. Des mesures optiques détaillées montrent que l’eau déplace la bande d’absorption de la quinone vers des longueurs d’onde plus longues tout en poussant la bande de l’Eosin Y vers des longueurs plus courtes. Cela rend le transfert d’énergie depuis l’Eosin Y excité vers la quinone très favorable sous lumière LED bleue ou verte, activant la quinone sans recourir à des sources UV intenses ni à un équipement élaboré.
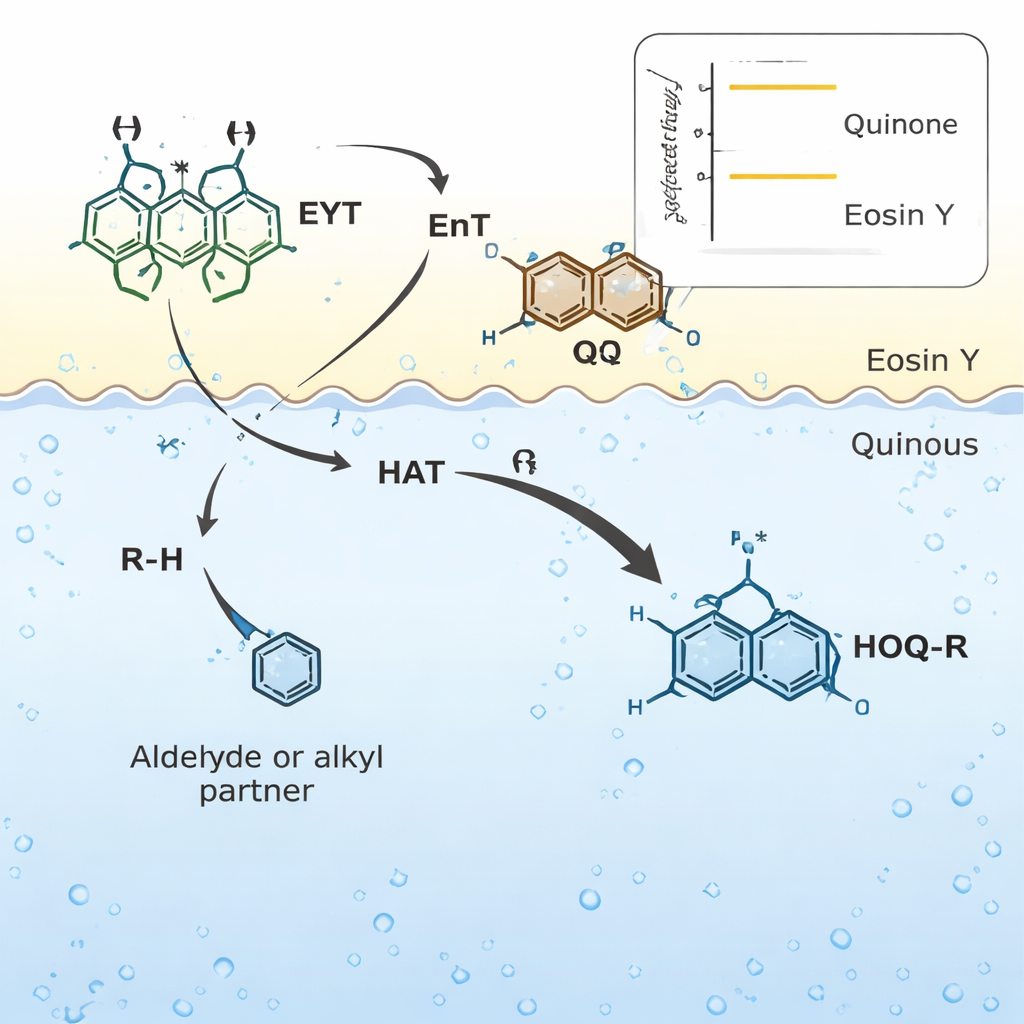
Construire des molécules complexes en douceur
Une fois activée par la lumière à l’interface, la quinone peut arracher un atome d’hydrogène à une large gamme de molécules partenaires — telles que des aldéhydes aromatiques et aliphatiques, des éthers, des thioéthers, des alcanes, des silanes et des amines — formant des radicaux de courte durée des deux côtés. Ces radicaux se recombinent rapidement pour forger de nouvelles liaisons carbone–carbone, produisant en une étape des quinols 2‑fonctionnalisés. Comme il n’y a pas d’oxydo‑réduction nette, le processus global est redox‑neutre, évitant réactifs supplémentaires et déchets. Les auteurs démontrent plus d’une centaine d’exemples, y compris de nombreux composants de parfumerie et des blocs de construction dérivés de médicaments commercialisés, et montrent que la méthode s’étend de la gamme milligramme à gramme tout en conservant de bons rendements.
Des intermédiaires réactifs à des produits utiles
Les nouveaux produits quinol ne sont pas de simples curiosités : ce sont des plateformes polyvalentes pour la chimie en aval. Certains se réoxydent facilement en quinones, se réduisent en structures plus saturées ou se plient en systèmes cycliques plus élaborés rappelant des antibiotiques naturels et des agents anticancéreux. L’équipe applique également la méthode à une variété de cœurs de type quinone, y compris des benzoquinones simples, des systèmes polyaromatiques plus larges et des maléimides, montrant que le concept sous‑jacent — transfert d’atome d’hydrogène entraîné par la lumière d’une molécule partenaire vers une quinone excitée stabilisée par l’eau — est largement applicable. Des expériences de contrôle soignées avec des pièges à radicaux, un marquage isotopique et des catalyseurs absorbeurs de lumière alternatifs étayent ce modèle mécanistique.
Pourquoi c’est important pour la chimie de tous les jours
Pour un non‑spécialiste, l’impact de ce travail tient à la combinaison de trois caractéristiques attractives : l’eau comme milieu bénin, la lumière visible comme source d’énergie douce, et des molécules organiques largement disponibles comme partenaires. En exploitant l’organisation naturelle à la frontière huile‑eau, la méthode évite les réactifs agressifs, minimise les déchets et ouvre de nouvelles voies vers des composés bioactifs et des produits fins. En substance, les auteurs montrent que la modeste surface de l’eau peut être conçue en une plate‑forme verte et puissante pour construire des molécules complexes utiles en médecine, matériaux et produits du quotidien.
Citation: Mandal, T., Sharma, R., Mendez-Vega, E. et al. “On-water” photosensitization enables redox neutral acylation and alkylation of quinones. Nat Commun 17, 1813 (2026). https://doi.org/10.1038/s41467-026-69343-x
Mots-clés: photochimie, chimie verte, quinones, transfert d’atome d’hydrogène, réactions « on‑water »