Clear Sky Science · fr
L’IPA d’origine microbienne protège contre la colite en régulant la cétogenèse intestinale médiée par HMGCS2 pour faciliter la cicatrisation muqueuse
Pourquoi les bactéries intestinales comptent pour un intestin blessé
Lorsque la muqueuse intestinale est endommagée, comme dans les maladies inflammatoires de l’intestin (MII) ou après des traitements médicaux agressifs, l’organisme doit réparer rapidement cette « peau » interne pour empêcher que des contenus nocifs ne passent dans la circulation sanguine. Cette étude révèle comment une seule molécule produite par des bactéries intestinales bénéfiques peut aider l’intestin à se réparer, ouvrant la voie à de nouvelles approches pour traiter les troubles chroniques de l’intestin sans supprimer largement le système immunitaire.
Un signal utile émis par des microbes bienveillants
Les chercheurs ont commencé par comparer les empreintes chimiques des échantillons de selles de personnes atteintes de MII et de volontaires sains, ainsi que dans plusieurs modèles murins de colite. Parmi des centaines de molécules, une a retenu l’attention : l’acide indole-3-propionique (IPA), un produit de dégradation du tryptophane alimentaire produit par certaines bactéries intestinales. Les niveaux d’IPA étaient systématiquement plus faibles chez les personnes atteintes de la maladie de Crohn et chez les souris atteintes de colite que chez les sujets sains. Cela suggère que la perte d’IPA pourrait faire partie du dysfonctionnement lorsque la muqueuse devient inflammée et n’arrive pas à se réparer.
Renforcer la paroi protectrice de l’intestin
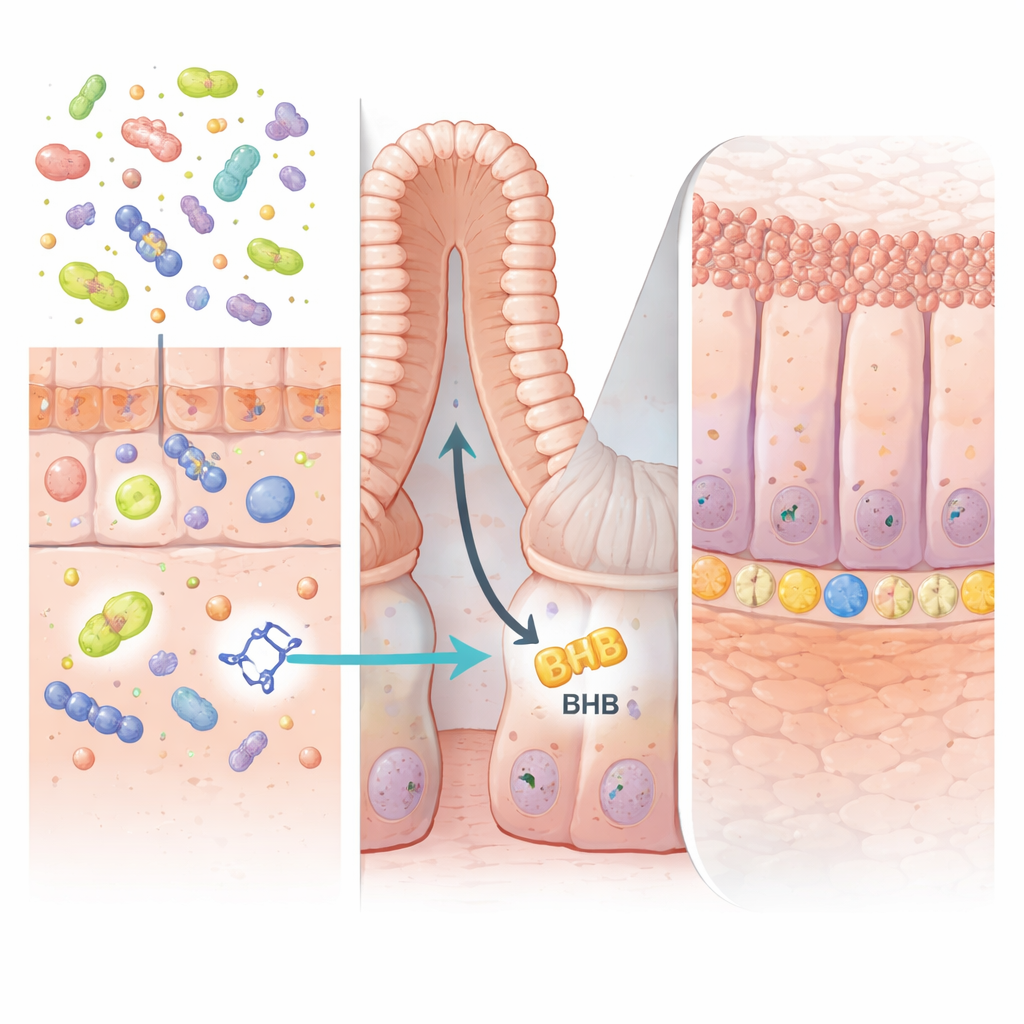
Pour déterminer si l’IPA était seulement un marqueur de la maladie ou si elle protégeait réellement, l’équipe a administré de l’IPA à des souris avant d’induire plusieurs types de lésions intestinales, notamment la colite chimique et les dommages par radiation. Les souris recevant des doses adéquates d’IPA avaient un côlon plus long et en meilleure santé, moins d’altérations inflammatoires au microscope et une couche de mucus plus épaisse avec des jonctions cellulaires plus étanches. Elles présentaient moins de fuites de marqueurs inflammatoires et un plus grand nombre de cellules caliciformes, qui produisent le mucus protecteur. Fait important, ces bénéfices ont été observés même chez des souris exemptes de germes, dépourvues de microbiote résident, montrant qu’une fois présente, l’IPA peut agir directement sur la muqueuse intestinale sans nécessiter d’autres microbes.
Approvisionner les cellules souches avec un type d’énergie particulier
La clé de l’action de l’IPA se trouvait au fond des « cryptes » intestinales, ces petites poches où siège un vivier de cellules souches qui renouvellent en permanence la muqueuse. Les auteurs montrent que l’IPA active une protéine appelée PPARα dans les cellules épithéliales intestinales. Cela stimule à son tour la production d’une enzyme nommée HMGCS2, qui pilote la cétogenèse — le processus de fabrication de la molécule énergétique β‑hydroxybutyrate (BHB). L’augmentation du BHB dans la paroi intestinale a stimulé l’expansion des cellules souches LGR5‑positives et accéléré la régénération des tissus endommagés. Lorsque l’enzyme HMGCS2 ou PPARα a été supprimée sélectivement dans les cellules intestinales chez la souris, l’IPA n’a plus pu renforcer l’activité des cellules souches ni protéger contre la colite, confirmant que cette voie de production de corps cétoniques est essentielle.
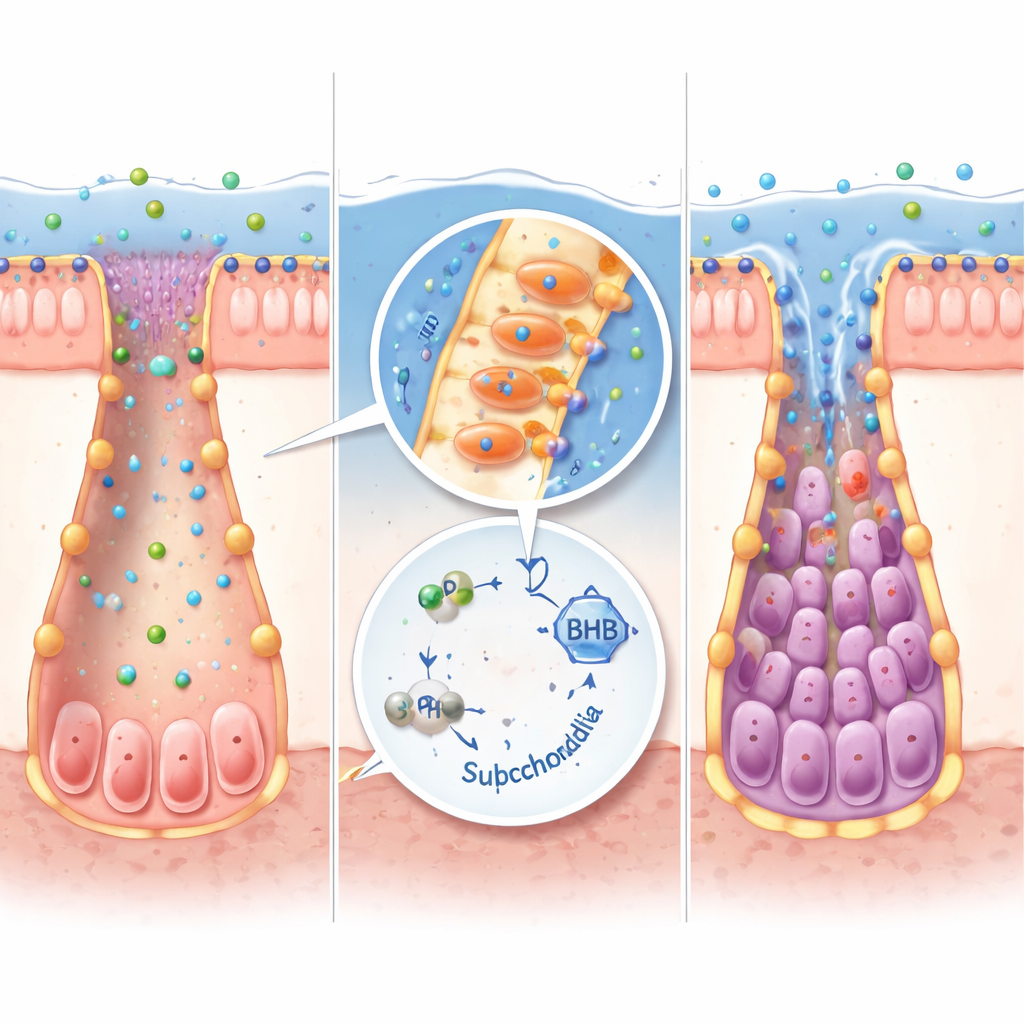
Des usines bactériennes aux tissus humains
Toutes les bactéries intestinales ne peuvent pas produire de l’IPA. En réanalysant de larges jeux de données du microbiome, les chercheurs ont identifié Peptostreptococcus russellii comme un producteur clé d’IPA, appauvri dans plusieurs cohortes de MII. En culture, cette bactérie convertissait efficacement le tryptophane en IPA. Lorsque des souris exemptes de germes ont été colonisées par P. russellii, leurs niveaux d’IPA ont augmenté, les gènes de la production de cétone se sont allumés, les marqueurs des cellules souches ont augmenté et la sévérité de la colite a diminué par rapport aux souris recevant une transplantation microbienne générique. La même voie IPA–cétone fonctionnait dans des organoïdes intestinaux miniatures issus de tissus murins et humains, où l’ajout d’IPA ou de BHB aidait les cellules souches à se rétablir après des dommages inflammatoires tout en atténuant les signaux pro-inflammatoires.
Ce que cela pourrait signifier pour les traitements futurs
Ensemble, ces travaux décrivent une chaîne d’événements simple mais puissante : certaines bactéries intestinales transforment le tryptophane alimentaire en IPA ; l’IPA active un interrupteur métabolique dans les cellules intestinales ; cet interrupteur augmente la production de BHB ; et le BHB, à son tour, revitalise les cellules souches qui reconstruisent la muqueuse. Pour les personnes atteintes de MII ou d’autres affections qui endommagent la barrière intestinale, des thérapies visant à restaurer l’IPA ou à imiter ses effets en toute sécurité — par l’alimentation, des probiotiques ciblés ou des médicaments concepteurs — pourraient favoriser une véritable cicatrisation muqueuse sans suppression immunitaire généralisée. Bien que des études supplémentaires chez l’humain soient nécessaires, cet axe microbe–métabolite–cellule souche offre un angle prometteur pour réparer l’intestin de l’intérieur.
Citation: Zhang, Y., Tu, S., Shao, X. et al. Microbiota-derived IPA protects against colitis by regulating intestinal HMGCS2-mediated ketogenesis to facilitate mucosal healing. Nat Commun 17, 2437 (2026). https://doi.org/10.1038/s41467-026-69341-z
Mots-clés: microbiome intestinal, cellules souches intestinales, maladie inflammatoire de l’intestin, métabolites microbiens, cicatrisation muqueuse