Clear Sky Science · fr
CD38 dégrade MAVS via la mitophagie pour inhiber la sécrétion d’interférons de type I dans les cellules du carcinome du nasopharynx et compromet l’immunité antitumorale médiée par les cellules T CD8+
Pourquoi cela compte pour le traitement du cancer
Le carcinome du nasopharynx est un cancer qui se développe derrière le nez et est particulièrement fréquent en Asie de l’Est et du Sud-Est. Les médicaments immunothérapeutiques qui libèrent les cellules T du patient ont modifié le pronostic de certains malades, mais la majorité n’en bénéficie pas. Cette étude met au jour un frein caché au sein même des cellules tumorales : une molécule appelée CD38 qui désactive silencieusement un système d’alarme interne et affaiblit l’attaque des cellules T CD8 tueuses de cancer. Comprendre et neutraliser ce frein pourrait permettre à de nombreuses personnes de mieux répondre aux immunothérapies existantes.
Un interrupteur caché sur les cellules tumorales
Les chercheurs se sont concentrés sur CD38, une protéine présente sur de nombreuses cellules immunitaires mais aussi exprimée par les cellules du carcinome du nasopharynx. Des travaux antérieurs avaient relié CD38 à la résistance aux médicaments de point de contrôle ciblant PD-1 et PD-L1. Ici, l’équipe a demandé si CD38 à l’intérieur des cellules tumorales modifie directement la capacité des cellules T CD8 à reconnaître et détruire ces cellules. En cultivant des cellules tumorales humaines avec ou sans CD38 aux côtés de cellules T CD8 humaines activées, ils ont observé que la suppression de CD38 dans les cellules cancéreuses rendait les lymphocytes T beaucoup plus efficaces : ils sécrétaient des niveaux plus élevés de molécules d’attaque clés, survivaient mieux et tuaient davantage de cellules tumorales. Lorsque CD38 était réintroduit, la fonction des T a diminué, ce qui désigne CD38 comme un suppresseur intrinsèque à la tumeur de l’attaque immunitaire.
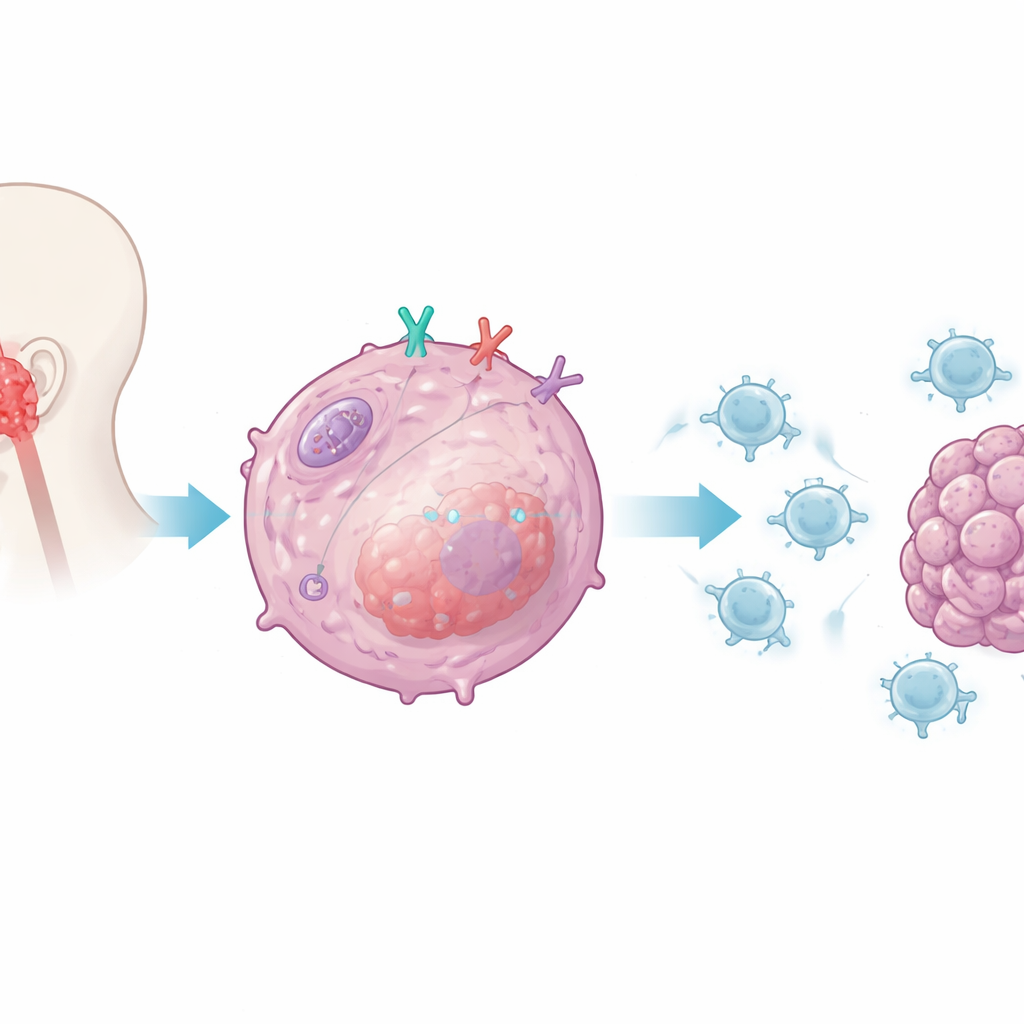
Atténuer l’alarme interne de la cellule
L’équipe a ensuite cherché comment CD38 transmet ce signal suppressif. Ils se sont focalisés sur le système d’alarme inné de la cellule tumorale, qui détecte normalement du matériel génétique de type viral et déclenche les interférons de type I — des messagers puissants stimulant l’immunité. Dans les cellules tumorales dépourvues de CD38, les chercheurs ont observé une forte augmentation de l’interféron-bêta et des chimiokines qui attirent les cellules T CD8 dans les tumeurs. Ils ont montré que CD38 atténue sélectivement la voie contrôlée par le détecteur interne RIG-I et sa protéine adaptatrice MAVS, située sur les mitochondries, les centrales énergétiques de la cellule. Lorsque CD38 était présent, l’activation de cette voie et de ses molécules de signalisation en aval était réduite ; quand CD38 était supprimé, la signalisation et la production d’interféron augmentaient fortement, renforçant la visibilité de la tumeur pour le système immunitaire.
Comment CD38 détruit un hub de signalisation clé
En approfondissant, les scientifiques ont trouvé que CD38 s’associe physiquement à MAVS sur les mitochondries et perturbe le partenariat de MAVS avec RIG-I, affaiblissant la transmission du signal. Plus frappant encore, des niveaux plus élevés de CD38 entraînaient une réduction de la protéine MAVS sans altération de son gabarit génétique, ce qui suggère une destruction active. Des tests avec différents inhibiteurs ont montré que cette perte dépendait du système de recyclage cellulaire appelé autophagie, et plus précisément d’une forme ciblant les mitochondries. CD38 augmentait les marqueurs de la « autophagie mitochondriale », réduisait plusieurs protéines mitochondriales et favorisait l’incorporation de MAVS dans des structures autophagiques ensuite dégradées. Bloquer la mitophagie préservait MAVS et restaurait la signalisation par les interférons, indiquant que CD38 désactive l’alarme en entraînant MAVS vers la voie d’élimination de la cellule.
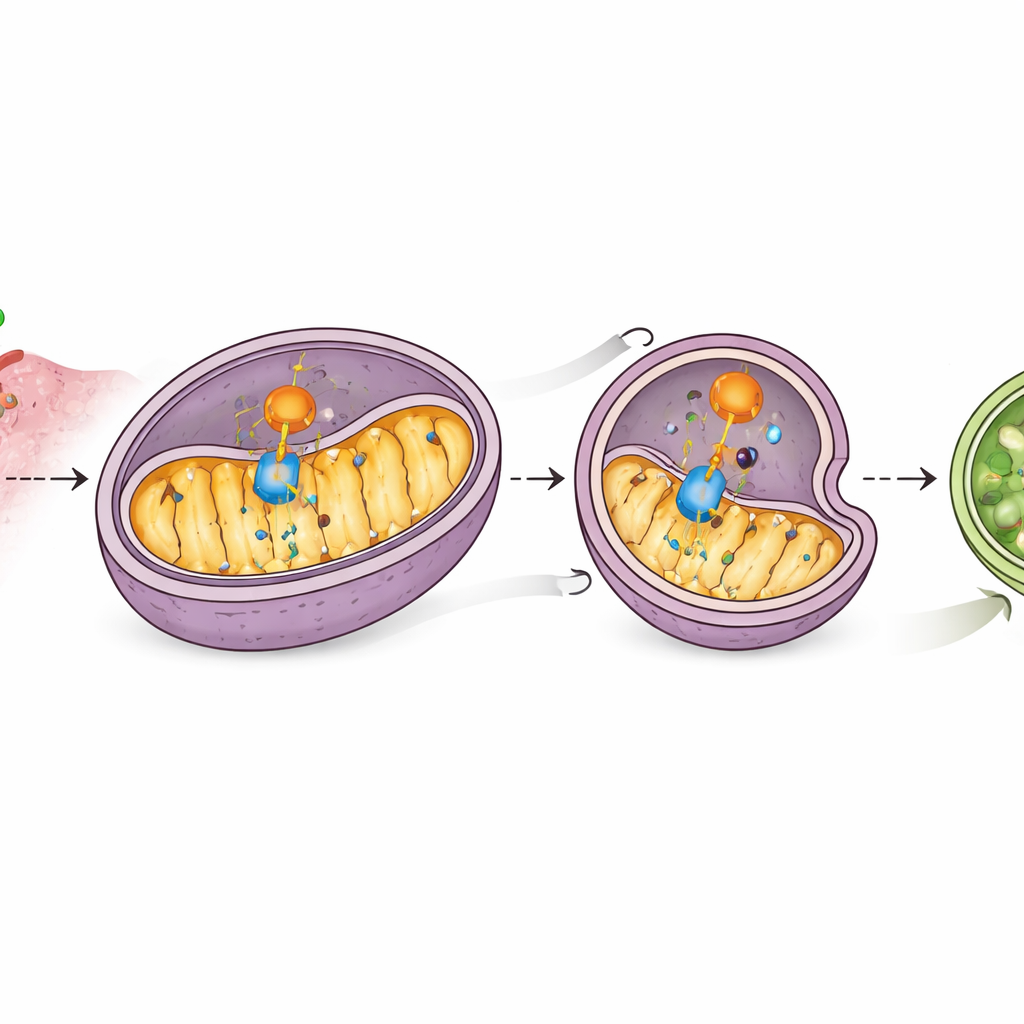
Un auxiliaire qui guide les mitochondries vers l’autodestruction
L’étude a identifié un autre acteur, PHB2, une protéine mitochondriale qui sert de récepteur pour l’élimination ciblée des mitochondries. La spectrométrie de masse et des expériences de liaison ont montré que CD38 interagit avec PHB2 et augmente la présence de PHB2 dans les mitochondries, où PHB2 recrute à son tour la machinerie autophagique centrale. PHB2 se lie également à MAVS, et CD38 renforce ce contact. Lorsque PHB2 était réduit, CD38 ne pouvait plus déclencher efficacement la mitophagie, les niveaux de MAVS rebondissaient et les gènes liés aux interférons se réactivaient. Cela révèle une chaîne d’événements : CD38 engage PHB2, PHB2 engage MAVS, et ensemble ils conduisent MAVS vers des mitochondries destinées à la dégradation, étouffant l’alarme des interférons.
Preuves issues de modèles animaux
Pour tester l’impact in vivo, les chercheurs ont utilisé des tumeurs murines conçues pour être dépourvues de CD38. Chez des souris immunocompétentes, ces tumeurs croissaient plus lentement, contenaient davantage de cellules T CD8 et comportaient une fraction plus élevée de cellules produisant l’interféron-gamma, un marqueur de réponses antitumorales actives. Le blocage du récepteur des interférons de type I supprimait cet avantage, confirmant que la signalisation par les interférons est essentielle à cette immunité renforcée. Chez des souris humanisées porteuses de tumeurs du nasopharynx, la réduction de CD38 ralentissait également la croissance et augmentait l’infiltration des cellules T CD8, mais ce bénéfice disparaissait lorsque MAVS était également réduit dans les cellules tumorales. Ces résultats in vivo confirment que l’axe CD38–PHB2–MAVS au sein des cellules tumorales façonne l’intensité de la réponse des cellules T de l’organisme.
Ce que cela signifie pour les thérapies futures
Dans l’ensemble, ce travail montre que CD38 dans les cellules du carcinome du nasopharynx agit comme un saboteur interne de l’immunité antitumorale. En induisant une forme sélective de recyclage mitochondrial, CD38 épuise MAVS, affaiblit la production d’interférons de type I, réduit la présentation des antigènes et, en définitive, atténue l’attaque des cellules T CD8. Les composés actuels bloquant CD38 ciblent principalement son activité enzymatique et n’éliminent pas la protéine ni ne restaurent MAVS. Les auteurs soutiennent que de nouvelles stratégies visant à réduire les niveaux de CD38 ou à perturber son partenariat avec PHB2 ou MAVS pourraient réactiver l’alarme des interférons à l’intérieur des tumeurs. Associées aux inhibiteurs de point de contrôle existants, de telles approches pourraient transformer davantage de cancers du nasopharynx — et potentiellement d’autres — d’immunologiquement froids en immunologiquement sensibles.
Citation: Liang, L., Li, W., Liu, S. et al. CD38 degrades MAVS through mitophagy to inhibit type I interferon secretion in nasopharyngeal carcinoma cells and impairs CD8+T cell-mediated anti-tumor immunity. Nat Commun 17, 2544 (2026). https://doi.org/10.1038/s41467-026-69339-7
Mots-clés: carcinome du nasopharynx, immunothérapie tumorale, interféron de type I, cellules T CD8, mitophagie