Clear Sky Science · fr
Évaluation comparative de l’inférence de la voie de signalisation EGF en utilisant la phosphoprotéomique et les interactions kinase-substrat
Pourquoi cela compte au-delà du laboratoire
Nos cellules écoutent et répondent en permanence aux signaux de leur environnement. L’un des plus importants est le facteur de croissance épidermique (EGF), qui contribue à réguler la croissance, la division et la survie cellulaires. Lorsque ce système de communication dysfonctionne, il peut favoriser l’apparition de cancers et d’autres maladies. Cette étude pose une question apparemment simple mais aux grandes implications : si l’on utilise les technologies de mesure et les modèles informatiques puissants d’aujourd’hui, dans quelle mesure peut-on mieux comprendre la voie de signalisation EGF par rapport aux schémas présentés dans les manuels ?
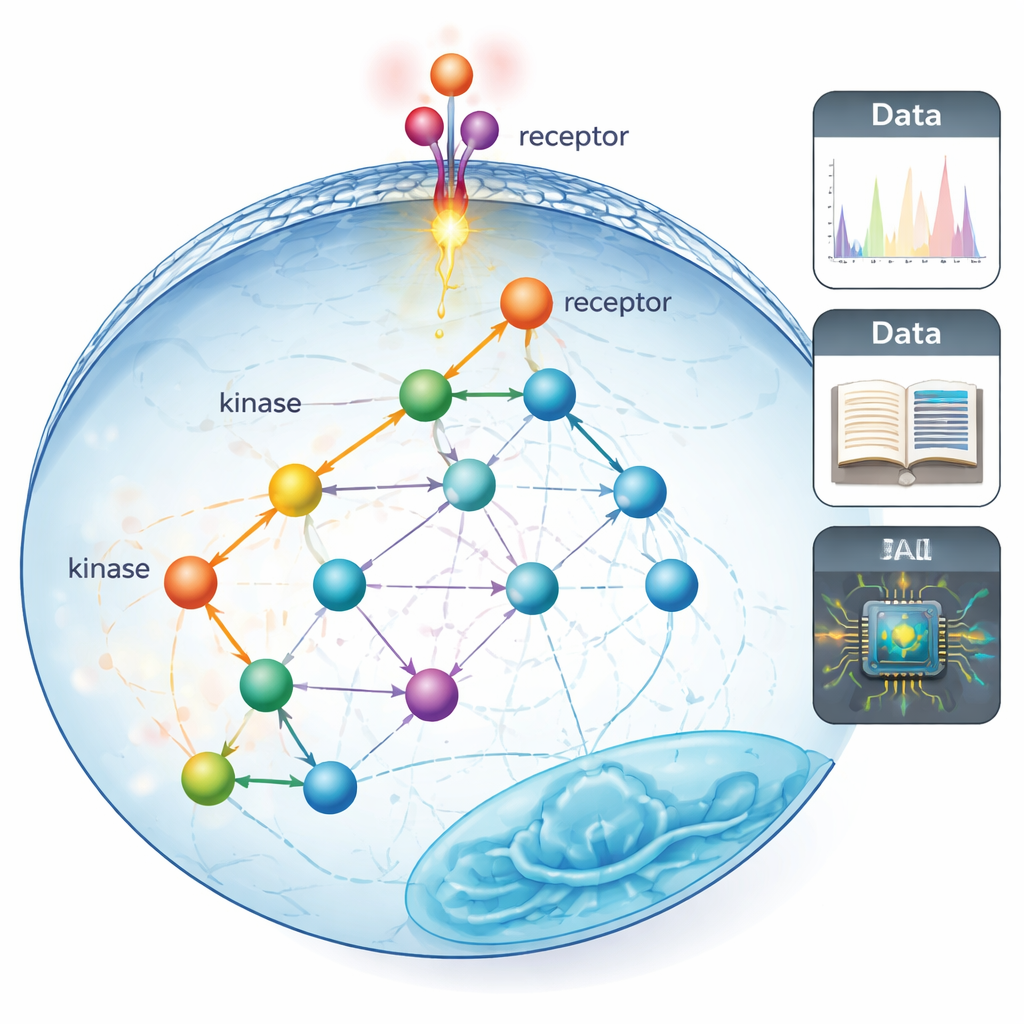
Des lignes droites aux schémas de câblage réels
Les « voies de signalisation » traditionnelles sont souvent représentées comme des chaînes nettes et presque linéaires de protéines transmettant un message de la surface cellulaire au noyau. Ces cartes ont été élaborées sur des décennies à partir d’expériences ciblées, lentes, ne portant que sur quelques protéines à la fois. Les auteurs soutiennent que cela nous a laissé une vision étroite, éclairée uniquement là où la lampe de poche passait : nous savons beaucoup sur les quelques protéines faciles à étudier, et beaucoup moins sur le réseau plus large de connexions qui existe probablement dans les cellules réelles.
Écouter des milliers d’interrupteurs moléculaires à la fois
Pour dépasser cette vue limitée, l’équipe a utilisé la phosphoprotéomique, une méthode de spectrométrie de masse capable de suivre des dizaines de milliers de petites étiquettes chimiques appelées groupes phosphate sur des protéines en une seule expérience. Ces étiquettes sont ajoutées par des enzymes appelées kinases et servent d’interrupteurs rapides d’activation/désactivation pour la signalisation. Les chercheurs ont d’abord assemblé les cartes les plus complètes à ce jour du « qui peut phosphoryler qui » en fusionnant trois types d’informations : des résultats recensés dans la littérature, des prédictions d’un modèle d’intelligence artificielle qui lit les séquences protéiques, et de larges cribles expérimentaux des préférences des kinases. Cela a considérablement élargi la couverture des relations kinase–substrat connues ou suspectées, passant d’environ 5 % des sites mesurables à près de 70–80 %.
Tester la robustesse de la signalisation EGF sur de multiples expériences
Ensuite, ils se sont concentrés sur la réponse à l’EGF, une voie classique et un acteur majeur dans les cancers du poumon, du sein, de la peau et du cerveau. Le groupe a combiné trois jeux de données publiés à la pointe avec trois nouvelles mesures très profondes et résolues dans le temps sur des cellules d’origine rénale, ainsi que deux études de contrôle utilisant différents stimuli. Ensemble, ces expériences ont mesuré plus de 40 000 sites de phosphorylation par jeu de données et suivi leur augmentation ou diminution dans les minutes suivant la stimulation par l’EGF. Bien que les motifs globaux diffèrent quelque peu selon les types cellulaires et les technologies, des sites de phosphorylation clés de la voie EGF ont été activés de manière répétée, confirmant que le signal central est robuste même à travers des expériences diverses.
Reconstruire la conversation cachée entre kinases
Après avoir déduit quelles kinases devenaient plus ou moins actives, les auteurs ont ensuite tenté de reconstituer la « conversation » sous-jacente entre elles : quelles kinases activent ou influencent probablement quelles autres. Ils ont converti leurs cartes kinase–substrat en réseaux kinase–kinase et appliqué trois stratégies computationnelles, allant de schémas de classement simples à une approche plus complexe qui contraint le résultat à ressembler à un arbre orienté raciné au niveau du récepteur EGF. Ils ont comparé les voies inférées obtenues avec plusieurs types de « vérités de référence » : une carte EGF soigneusement curatée dans une base de données, des expériences à grande échelle où des kinases uniques étaient surexprimées, et des paires de sites de kinases dont le comportement était fortement corrélé dans le temps.
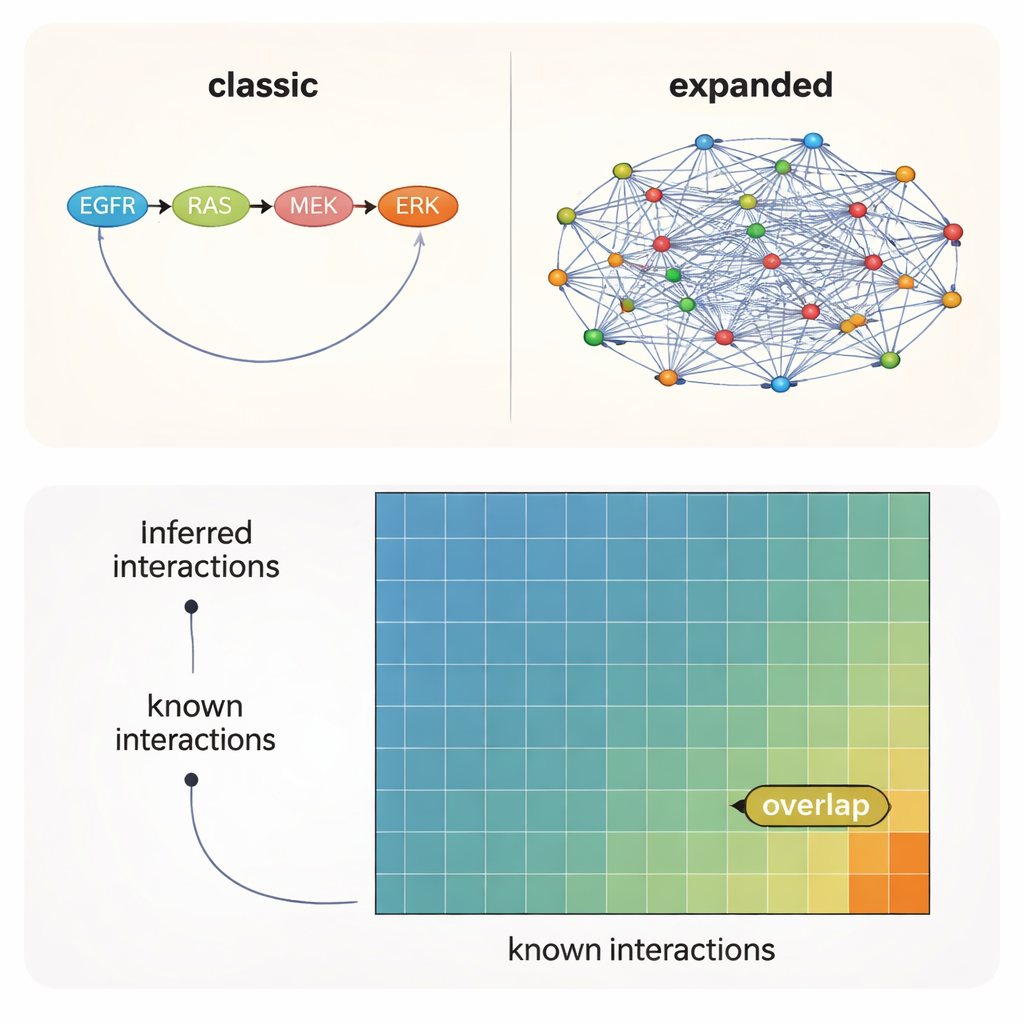
Les liens les plus plausibles sont encore absents de la carte officielle
Dans tous les tests, un message est ressorti clairement : le choix des connaissances a priori — le réseau de départ que vous fournissez à l’algorithme — comptait plus que la méthode particulière ou même le contexte expérimental. Les réseaux bâtis à partir de la littérature ont retrouvé le plus grand nombre d’interactions connues, tandis que des ressources prédictives plus larges indiquaient de nombreuses connexions supplémentaires et plausibles qui n’ont pas encore été documentées formellement. Même dans les meilleures conditions, cependant, seulement environ 10–12 % des interactions suggérées par les données et les modèles figuraient dans l’un des jeux de référence. Autrement dit, environ 90 % des liens kinase–kinase soutenus se trouvent en territoire inexploré.
Ce que cela signifie pour les traitements futurs
Pour les non-spécialistes, la conclusion est que le schéma bien connu de la voie EGF dans les manuels n’est probablement que la partie émergée de l’iceberg. La phosphoprotéomique moderne combinée à des méthodes computationnelles avancées dévoile un réseau de signalisation beaucoup plus riche et enchevêtré. Beaucoup de ces connexions nouvellement suggérées peuvent représenter des moyens négligés par lesquels les cellules cancéreuses contournent les médicaments, ou des opportunités pour concevoir des combinaisons de médicaments plus intelligentes. L’étude ne prouve pas que chaque nouveau lien soit réel, mais elle fournit une feuille de route et des outils ouverts pour que les chercheurs testent ces idées, visant ultimement des thérapies plus précises et efficaces dans les maladies où la signalisation EGF joue un rôle central.
Citation: Garrido-Rodriguez, M., Potel, C., Burtscher, M.L. et al. Benchmarking EGF signaling pathway inference using phosphoproteomics and kinase-substrate interactions. Nat Commun 17, 2071 (2026). https://doi.org/10.1038/s41467-026-69332-0
Mots-clés: signalisation EGF, phosphoprotéomique, kinases protéiques, réseaux de signalisation cellulaire, biologie du cancer