Clear Sky Science · fr
Mycobacterium tuberculosis module la phosphorylation de l’ATP6V1E1 de l’hôte pour favoriser sa survie intracellulaire
Pourquoi cela importe pour lutter contre la tuberculose
La tuberculose reste l’une des maladies infectieuses les plus mortelles au monde, tuant plus d’un million de personnes chaque année. Nos cellules immunitaires sont dotées de puissants « bacs acides de recyclage » qui digèrent normalement les microbes envahisseurs. Cet article révèle comment la bactérie de la tuberculose, Mycobacterium tuberculosis (Mtb), sabote ce système d’acidification à l’intérieur de nos cellules, et montre qu’un médicament visant ce stratagème peut aider des animaux infectés à éliminer l’infection plus efficacement.
Le bain acide de la cellule pour les germes
Lorsque les bacilles de la tuberculose sont inhalés dans les poumons, ils sont rapidement engloutis par des cellules immunitaires appelées macrophages. Les bactéries se retrouvent dans des vésicules membranaires qui sont censées fusionner avec des lysosomes — de petits sacs remplis d’enzymes digestives qui fonctionnent mieux dans un environnement fortement acide. Cette acidité est créée par une pompe moléculaire, la vacuolar ATPase (V-ATPase), qui utilise l’énergie cellulaire pour pousser des protons dans les lysosomes et abaisser le pH interne. Une acidification correcte est cruciale pour dégrader Mtb, pourtant des décennies de travaux ont montré que ce pathogène parvient d’une manière ou d’une autre à maintenir ses compartiments moins acides et à survivre.
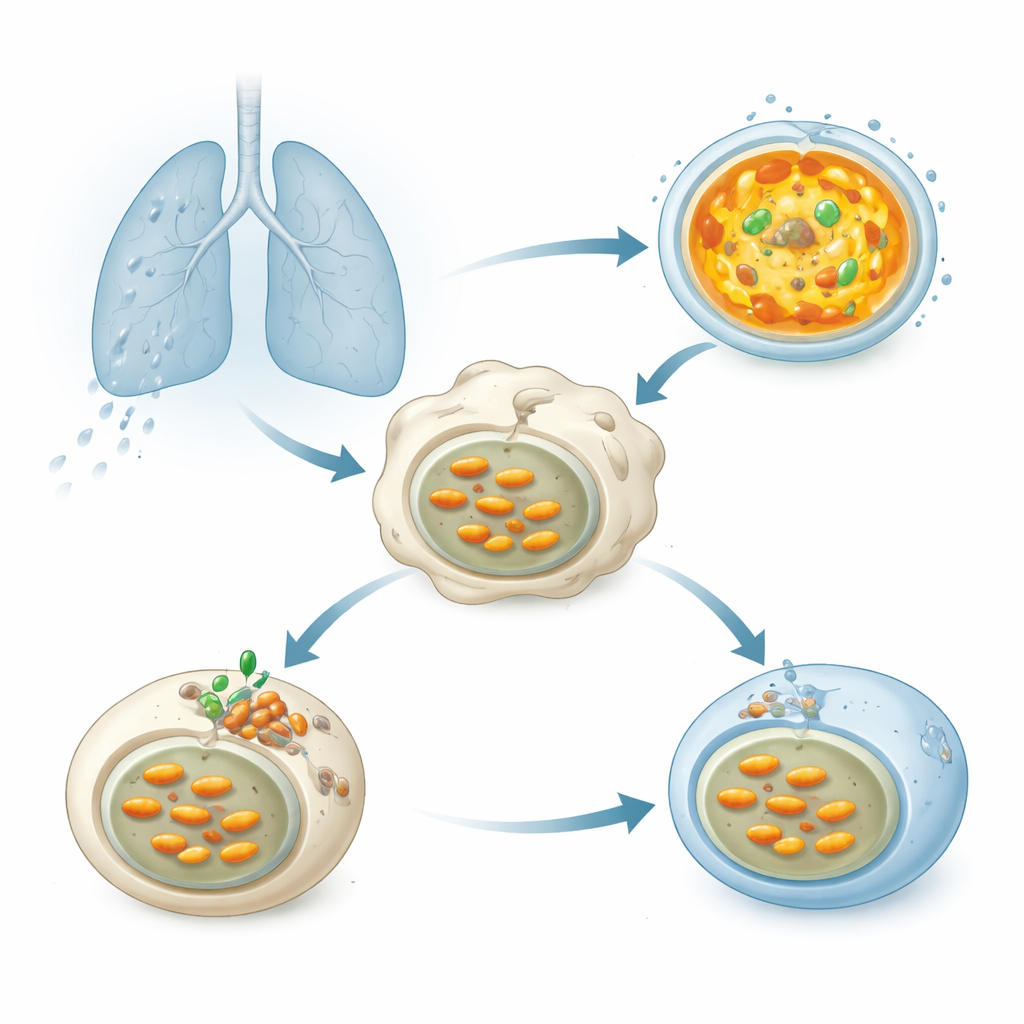
Un auxiliaire bactérien secret qui bloque l’acidification
Les chercheurs ont testé plus de 200 protéines que Mtb peut libérer pour déterminer lesquelles affaiblissent l’acidification lysosomale dans les cellules humaines. Une protéine est ressortie : une enzyme appelée Chp2 (également connue sous le nom Rv1184). Lorsque les cellules produisaient Chp2, leurs lysosomes s’illuminaient moins avec des colorants sensibles à l’acidité, indiquant un pH plus élevé et moins hostile. Les souches de Mtb génétiquement modifiées pour ne pas exprimer Chp2 n’inhibaient plus l’acidification ; dans des macrophages infectés et chez la souris, ces bactéries mutantes étaient éliminées plus efficacement et causaient des lésions pulmonaires plus légères. Le rétablissement de Chp2 dans la souche mutante rétablit à la fois le blocage de l’acidification et la charge bactérienne plus élevée, identifiant Chp2 comme un facteur de virulence qui aide Mtb à persister à l’intérieur des cellules hôtes.
La sous-unité de la pompe de l’hôte qui fait office d’interrupteur
Pour comprendre comment Chp2 interfère avec l’acidification, l’équipe a recherché des composants de l’hôte auxquels il pourrait se lier. Ils ont découvert que Chp2 se fixe directement à une partie particulière de la V-ATPase, une sous-unité appelée ATP6V1E1 (E1 pour faire court), qui contribue à stabiliser la structure de la pompe. Augmenter la quantité d’E1 dans les cellules renforçait l’acidification lysosomale et rendait plus difficile la survie de Mtb, tandis que réduire E1 avait l’effet inverse. Les souris ne portant qu’une copie fonctionnelle du gène E1 présentaient des lysosomes moins acides, des charges bactériennes plus élevées dans leurs poumons et des lésions tissulaires plus sévères après infection, montrant que E1 est un défenseur hôte important contre la tuberculose.
Une balise de kinase sur la pompe qui réduit l’acide
Les auteurs se sont alors demandé si des « étiquettes » chimiques sur E1 pouvaient moduler l’activité de la pompe. Ils ont découvert que l’ajout de groupes phosphate sur deux tyrosines spécifiques (Tyr56 et Tyr57) de E1 agit comme un frein : la mimique de la phosphorylation réduisait l’acidification et empêchait l’assemblage complet de la V-ATPase, tandis qu’empêcher la phosphorylation avait l’effet inverse. En criblant un panel d’enzymes, ils ont identifié une kinase appelée BMX comme la protéine de l’hôte qui appose cette marque. Lorsque BMX était bloquée génétiquement ou par un inhibiteur de petite molécule, la phosphorylation d’E1 diminuait, la pompe s’assemblait plus efficacement sur les membranes lysosomales, les lysosomes devenaient plus acides et la survie de Mtb à l’intérieur des macrophages diminuait.
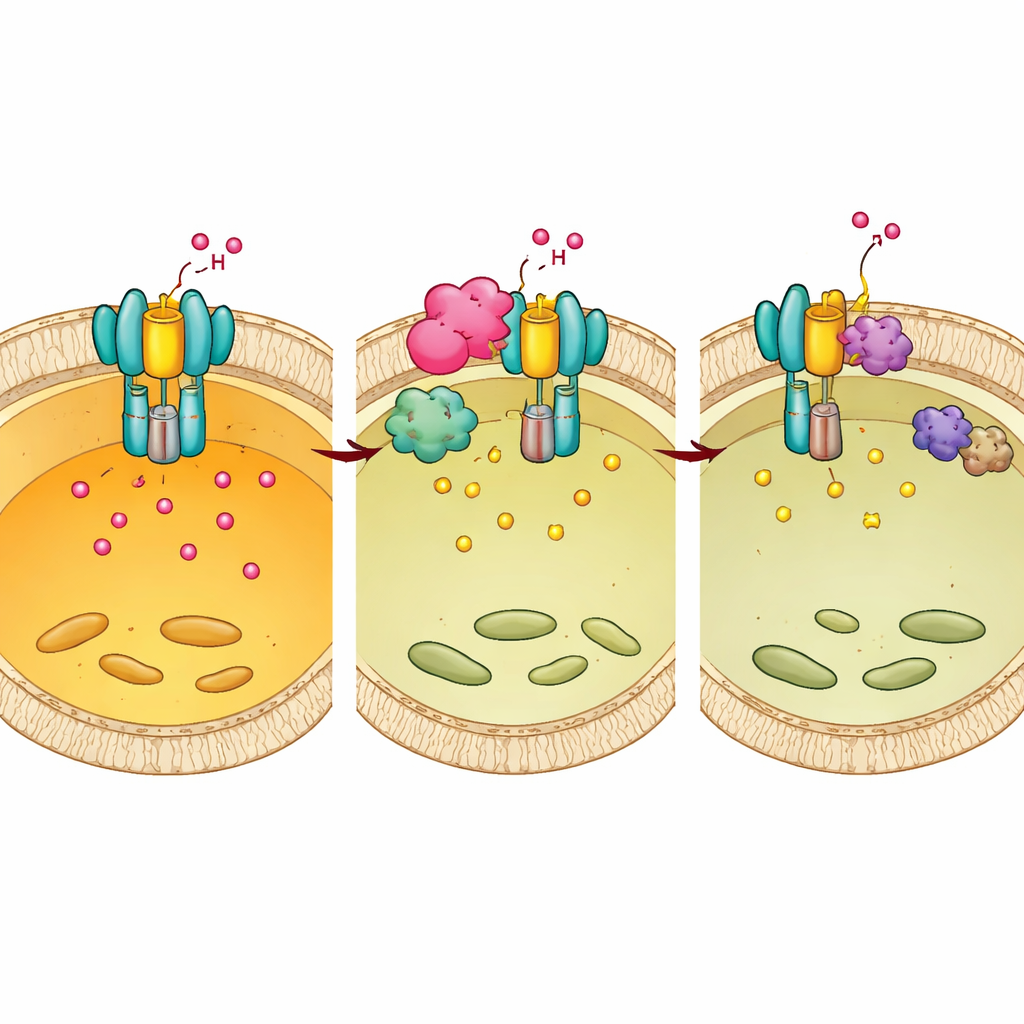
Comment Mtb reprogramme l’interrupteur de l’hôte à son avantage
Chp2 et BMX s’avèrent fonctionner ensemble. Des expériences structurales et biochimiques ont montré que Chp2 agit comme un échafaudage qui rapproche E1 et BMX en surface lysosomale, favorisant la phosphorylation d’E1 sur Tyr56/57. Cette étiquette supplémentaire perturbe l’assemblage complet de la pompe, élève le pH lysosomal et crée un environnement plus clément dans lequel Mtb peut persister. Lorsque BMX était inhibée, l’avantage de survie conféré par Chp2 disparaissait, tant dans des cellules en culture que chez des souris infectées. Fait important, traiter des souris avec l’inhibiteur de BMX après infection réduisait la charge bactérienne et la pathologie pulmonaire chez des animaux normaux, mais pas chez des souris ayant un E1 affaibli, indiquant que le médicament agit en restaurant l’acidification efficace pilotée par E1.
Transformer le stratagème du pathogène en idée thérapeutique
En termes simples, cette étude montre que les bactéries de la tuberculose glissent une protéine auxiliaire dans nos cellules qui perturbe la « pompe acide » du dispositif de nettoyage, l’atténuant juste assez pour que les microbes échappent à la destruction. En identifiant la sous-unité de la pompe qui sert de bouton de contrôle (E1) et l’enzyme de l’hôte qui la bascule (BMX), les auteurs révèlent un point précis où un médicament peut intervenir. L’inhibition de BMX chez la souris réactive efficacement le bain acide interne de la cellule et améliore le nettoyage bactérien. Ces découvertes ouvrent la voie à des thérapies dirigées contre l’hôte qui rendent nos propres cellules plus hostiles à Mtb, pouvant agir en complément des antibiotiques et aider à lutter contre la tuberculose résistante aux médicaments.
Citation: Chen, J., Tang, F., Qin, L. et al. Mycobacterium tuberculosis modulates phosphorylation of host ATP6V1E1 to promote intracellular survival. Nat Commun 17, 2434 (2026). https://doi.org/10.1038/s41467-026-69331-1
Mots-clés: tuberculose, lysosomes, thérapie dirigée contre l’hôte, Mycobacterium tuberculosis, V-ATPase