Clear Sky Science · fr
Développement d’un anticorps monoclonal puissant pour le traitement des infections à métapneumovirus humain
Pourquoi un virus discret en hiver compte
À chaque saison des rhumes et de la grippe, un virus peu connu appelé métapneumovirus humain (HMPV) envoie discrètement des millions de jeunes enfants, de personnes âgées et d’immunodéprimés vers les cliniques et les hôpitaux. Contrairement à son cousin viral, le virus respiratoire syncytial (VRS), il n’existe ni vaccins ni traitements ciblés pour le HMPV. Cette étude rapporte la découverte d’un anticorps fabriqué en laboratoire, nommé 4F11, capable d’arrêter le HMPV en culture cellulaire et de protéger des animaux infectés, ouvrant la voie à un médicament longtemps attendu pour certains des patients les plus vulnérables.
Le virus qui passe sous le radar
Le HMPV est un virus respiratoire courant dans le monde, responsable d’environ 14 millions d’infections des voies respiratoires basses chez les enfants de moins de cinq ans chaque année, et il pèse aussi lourdement sur les adultes de plus de 60 ans. Pour les patients dont le système immunitaire est sévèrement affaibli — comme les receveurs de greffes de cellules souches — le taux de mortalité lié aux infections pulmonaires à HMPV peut être alarmant. Des vaccins commencent seulement à apparaître pour des virus apparentés comme le VRS, et même si un vaccin contre le HMPV existait, de nombreux patients fortement immunodéprimés y répondraient mal. Face à ce vide thérapeutique, les chercheurs se tournent vers les anticorps monoclonaux — des protéines immunitaires précisément ciblées qui peuvent être administrées comme médicaments — pour prévenir ou traiter les formes sévères.
Trouver un anticorps protecteur remarquable
L’équipe a cherché un anticorps réunissant trois caractéristiques clés : une extrême puissance, une activité contre de nombreuses souches de HMPV, et une capacité à laisser peu de place au virus pour développer une résistance. Ils se sont concentrés sur la protéine de fusion du virus, une structure armée à la surface virale qui doit changer de forme pour permettre au virus de fusionner avec et pénétrer dans les cellules pulmonaires. En utilisant une stratégie de « leurre et commutation », ils ont isolé de rares cellules B humaines dans des échantillons de sang et de rate capables de reconnaître une souche de HMPV mais de neutraliser une autre, enrichissant ainsi les anticorps à large spectre. Parmi plus d’un millier de cellules candidates, ils ont isolé trois anticorps prometteurs et découvert qu’un d’entre eux — 4F11 — était exceptionnellement puissant, bloquant l’infection des cellules à des concentrations près de 50 fois plus faibles qu’un anticorps de référence précédemment décrit et agissant contre les quatre principaux sous-types mondiaux du HMPV.
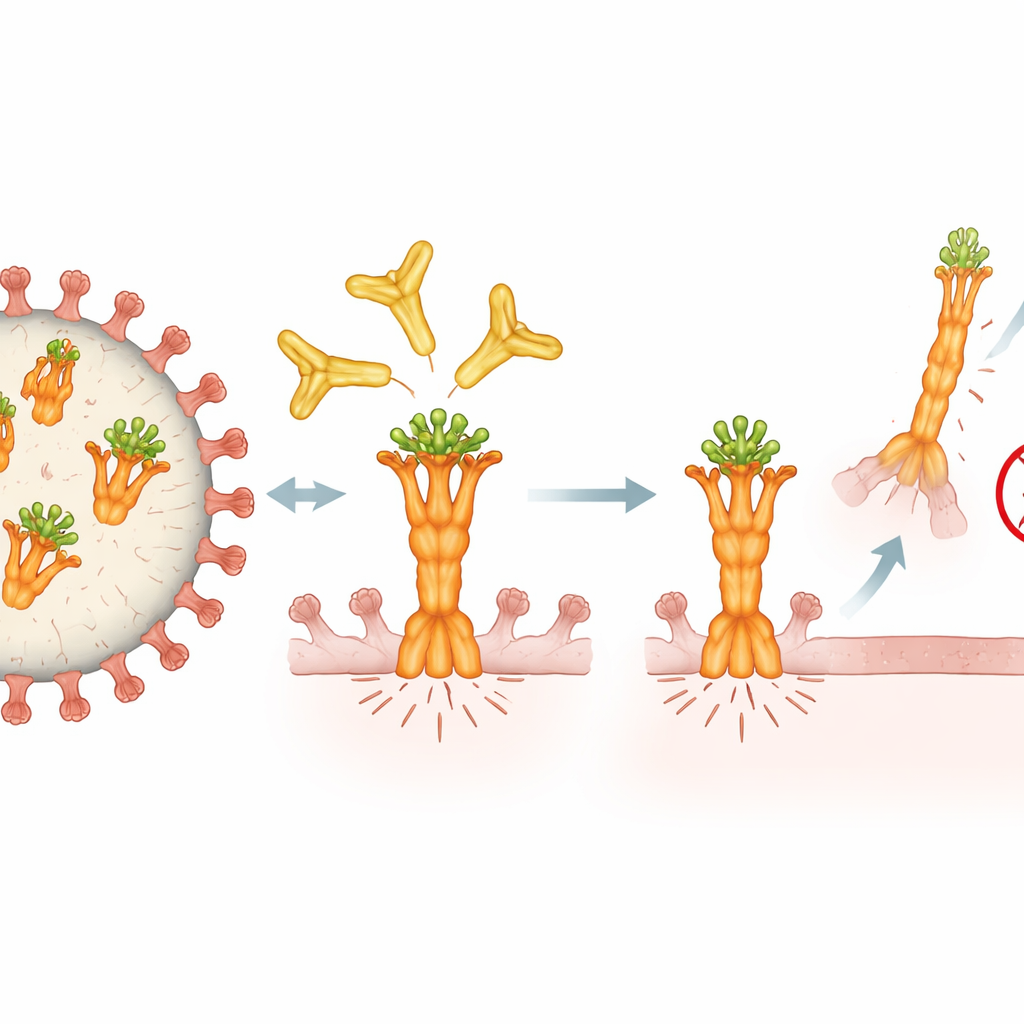
Comment 4F11 saisit le point faible du virus
Pour comprendre pourquoi 4F11 est si efficace, les chercheurs ont utilisé la cryo‑microscopie électronique à haute résolution pour visualiser son ancrage sur la protéine de fusion. Ils ont découvert que 4F11 cible une petite zone conservée située tout en haut de la forme préfusion de la protéine — le ressort avant qu’il ne se déclenche. Contrairement à d’autres anticorps qui se lient trois fois par protéine de fusion, 4F11 se place seule au sommet dans une configuration un-à-un, descendant droit et enserrant même une décoration glucidique qui masque la surface. Cet angle de liaison inhabituel et cette dépendance à ce sucre font de 4F11 un type d’anticorps singulier. Il reconnaît uniquement la forme préfusion, présente sur le virus infectieux, et empêche probablement la protéine de se replier en la conformation nécessaire pour percer et fusionner avec une cellule hôte.
Le virus peut-il échapper — et à quel prix ?
L’équipe a ensuite forcé le virus à croître en culture cellulaire en présence constante de 4F11 pour évaluer la facilité avec laquelle il pourrait évoluer vers l’échappement. Comparé à un anticorps témoin qui a rapidement favorisé l’émergence de plusieurs mutations d’échappement, le HMPV a eu bien plus de mal à contourner 4F11. Une seule modification dans la protéine de fusion, changeant un acide aminé en position 179, a suffi à interrompre complètement la liaison de 4F11. Toutefois, les virus portant cette mutation présentaient une croissance nettement déficiente par rapport au virus normal, indiquant un sérieux coût en termes d’aptitude virale. Des recherches en bases de données portant sur des centaines de séquences de HMPV ont montré que ce changement délétère n’a jamais été observé dans la nature, ce qui suggère que, bien que le virus puisse en principe échapper à 4F11 en laboratoire, il en paie un prix si élevé en termes de croissance qu’il est peu probable qu’il se propage largement dans le monde réel.
Tester la protection dans un modèle animal
La puissance en laboratoire doit encore se traduire par une protection réelle. Pour cela, les chercheurs ont infecté des hamsters syriens dorés par le HMPV puis, un jour plus tard, les ont traités par 4F11 — reproduisant un traitement précoce plutôt qu’une prévention. Une seule injection à faible dose de 4F11 a fortement réduit les niveaux viraux dans les poumons et les voies nasales, et à la dose supérieure elle a éliminé complètement le virus détectable dans les poumons chez la plupart des animaux. Il est notable que ces doses étaient inférieures à celles utilisées pour plusieurs anticorps monoclonaux déjà approuvés contre le VRS chez l’homme. En revanche, un anticorps décrit auparavant et capable de réagir avec plusieurs virus a offert peu de protection à la même dose, soulignant la force particulière de 4F11 comme traitement ciblé contre le HMPV.
Ce que cela pourrait signifier pour les patients
Pris ensemble, ces résultats positionnent 4F11 comme un candidat solide pour le développement clinique. Il combine une grande puissance, une couverture étendue des souches de HMPV en circulation, une manière distinctive d’agripper une région vulnérable de la protéine de fusion, et un paysage de résistance dans lequel la voie d’échappement évidente pour le virus entraîne une pénalité de croissance substantielle. Pour les nourrissons, les personnes âgées et les patients immunodéprimés à haut risque de maladie sévère à HMPV, un médicament basé sur 4F11 pourrait un jour offrir à la fois un traitement d’urgence après infection et une protection supplémentaire aux côtés ou en remplacement des vaccins.
Citation: Harris, E.D., McGovern, M., Pernikoff, S. et al. Development of a potent monoclonal antibody for treatment of human metapneumovirus infections. Nat Commun 17, 2714 (2026). https://doi.org/10.1038/s41467-026-69328-w
Mots-clés: métapneumovirus humain, anticorps monoclonal, infection respiratoire, protéine de fusion, thérapie antivirale