Clear Sky Science · fr
Une plateforme 3D intestin‑cerveau‑vasculature pour un dialogue bidirectionnel dans la neuropathogenèse intestinale
Pourquoi votre intestin pourrait importer pour votre cerveau
L’idée selon laquelle « vous êtes ce que vous mangez » prend une nouvelle tournure : des preuves croissantes suggèrent que ce qui se passe dans votre intestin peut influencer la santé de votre cerveau. Cet article présente un modèle de laboratoire sophistiqué qui relie des versions miniaturisées d’intestin humain, de vaisseaux sanguins et de tissu cérébral sur une seule puce. En observant comment les signaux circulent le long de cette petite autoroute, les chercheurs explorent comment des troubles intestinaux pourraient déclencher des maladies cérébrales comme Alzheimer et Parkinson — et comment des problèmes cérébraux pourraient, en retour, renvoyer du trouble vers l’intestin.
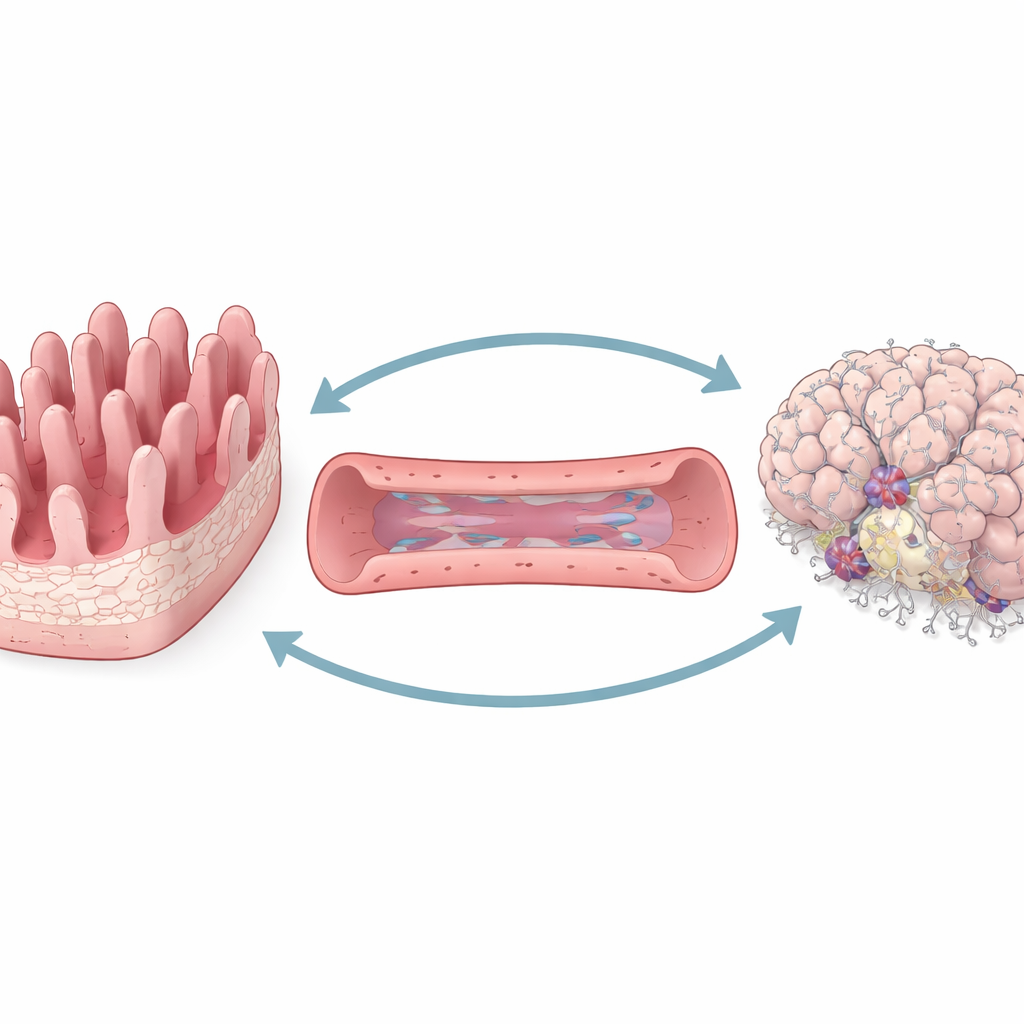
Construire un mini‑corps sur une puce
Pour étudier la communication intestin–cerveau de manière contrôlée, l’équipe a conçu une plateforme « organe‑sur‑puce » en trois parties. Un compartiment imite la surface interne de l’intestin, avec des projections digitiformes qui forment une barrière entre le contenu intestinal et le reste du corps. Un deuxième compartiment représente des vaisseaux sanguins tapissés de cellules vasculaires de type cérébral. Le troisième contient des neurones humains vivants et des cellules de soutien disposés pour ressembler à un petit morceau de cerveau. Des fluides peuvent circuler entre ces compartiments, permettant aux molécules de voyager de façon analogue à la circulation dans l’organisme.
Rendre le modèle comparable à un tissu réel
La puce est conçue de sorte que les cellules subissent un flux doux et oscillant plutôt que de rester dans une boîte statique. Ce mouvement favorise le développement de replis plus épais et plus réalistes de la couche intestinale et le renforcement des jonctions entre cellules, la rendant moins perméable. La couche vasculaire réagit en s’étirant dans la direction du flux, un signe caractéristique de vaisseaux sains, et manifeste une forte barrière contre les grosses molécules. Dans le compartiment cérébral, les neurones forment des réseaux actifs qui émettent des signaux calciques rythmiques, témoin d’activité électrique, tandis que les cellules de soutien entourent les vaisseaux voisins comme dans le tissu cérébral réel. Ensemble, ces caractéristiques montrent que les trois régions se comportent davantage comme dans l’organisme que dans les cultures cellulaires plates traditionnelles.
Quand des irritants intestinaux déclenchent des troubles cérébraux
Pour modéliser une maladie d’origine intestinale, les chercheurs ont ajouté des produits bactériens — soit du matériau issu de cultures d’E. coli, soit une toxine purifiée appelée LPS — du côté intestinal de la puce. Ces stimuli ont affaibli la barrière intestinale, permettant à davantage de grosses molécules et de traces bactériennes de traverser vers le compartiment vasculaire puis vers le compartiment cérébral. À mesure que la fuite augmentait, la paroi vasculaire devenait moins étanche et les cellules gliales étoilées du cerveau entraient dans un état réactif et d’alerte. Dans le tissu de type cérébral, des fragments protéiques nocifs associés à Alzheimer et Parkinson s’accumulaient, les connexions protectrices entre neurones déclinaient et les signaux inflammatoires montaient en puissance. Cette séquence, commençant par un intestin perturbé et se terminant par des cellules cérébrales stressées, reflète des schémas observés chez l’animal et chez les patients.
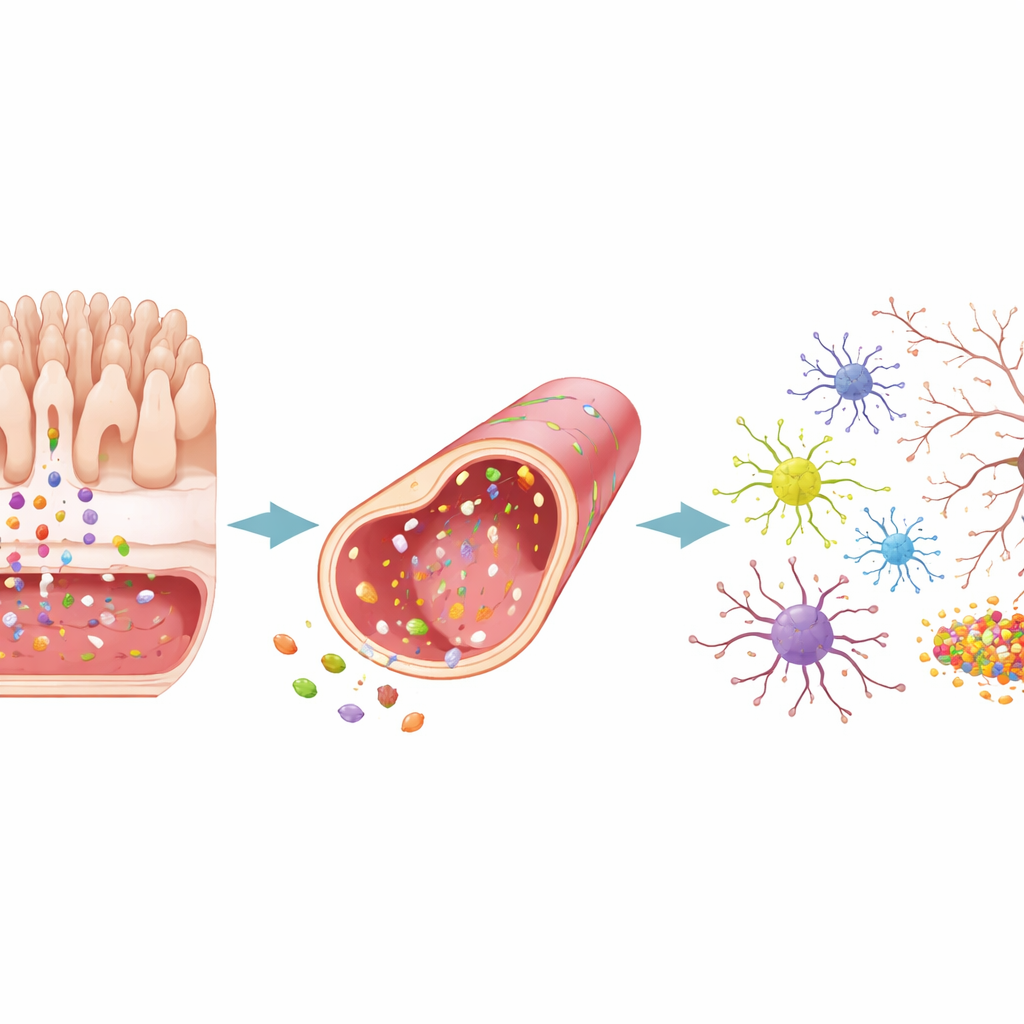
Quand la maladie cérébrale renvoie des signaux en retour
L’équipe a ensuite inversé la direction de l’expérience. Ils ont recréé des conditions de type Alzheimer en programmant des cellules cérébrales sur la puce pour surproduire des fragments amyloïdes collants, et des conditions de type Parkinson en les exposant à des agrégats de la protéine α‑synucléine. Dans les deux scénarios, des protéines toxiques se sont d’abord accumulées dans le compartiment cérébral puis sont apparues dans les régions vasculaires et intestinales. Le tissu cérébral a libéré des ondes de molécules inflammatoires, perdu des connexions synaptiques et montré d’autres signes de dégénérescence. Ces signaux de danger d’origine cérébrale ont fortement perturbé la couche vasculaire, relâchant sa barrière et activant les cellules de soutien voisines. La couche intestinale, en revanche, n’a présenté que des changements structurels modestes : sa surface s’est quelque peu altérée et est devenue plus « activée », mais ses jonctions serrées sont restées largement intactes et la fuite n’a augmenté que légèrement.
Ce que cela signifie pour les traitements futurs
En termes simples, cette puce suggère qu’un intestin malade peut provoquer l’inflammation et les dommages cérébraux de façon plus directe qu’un cerveau malade ne perturbe l’intestin. Les produits bactériens d’origine intestinale et l’inflammation semblent capables d’affaiblir à la fois les vaisseaux et le tissu cérébral, tandis que l’inflammation d’origine cérébrale cible surtout les vaisseaux sanguins et ne remodèle l’intestin que de façon subtile. Parce que l’ensemble du système est construit à partir de cellules humaines, il offre un banc d’essai prometteur pour des thérapies visant à calmer l’inflammation intestinale, sceller les barrières ou bloquer la propagation de protéines nuisibles. À terme, des plateformes comme celle‑ci pourraient aider les cliniciens à identifier quels patients pourraient le mieux bénéficier de stratégies ciblant l’intestin pour ralentir ou prévenir les maladies neurodégénératives.
Citation: Tran, M., Jeong, H.W., An, M. et al. A 3D gut-brain-vascular platform for bidirectional crosstalk in gut-neuropathogenesis. Nat Commun 17, 2504 (2026). https://doi.org/10.1038/s41467-026-69318-y
Mots-clés: axe intestin‑cerveau, organe sur puce, neuroinflammation, maladie d’Alzheimer, maladie de Parkinson