Clear Sky Science · fr
Le réseau neuronal préoptique kisspeptine-nNOS-GnRH (KiNG) régule la rythmicité de la LH par activation-inhibition chez la souris
Pourquoi cette histoire cérébrale compte pour la fertilité
L’ovulation et la fertilité dépendent d’un petit groupe de cellules cérébrales qui libèrent une hormone maîtresse par impulsions et par épisodes de forte libération. Lorsque ce timing se dérègle, la reproduction peut échouer. Cette étude révèle comment deux types de molécules de signalisation dans le cerveau de la souris — l’un qui active l’activité et l’autre qui la coupe discrètement — coopèrent pour façonner ces rythmes hormonaux. Comprendre ce circuit de temporisation caché pourrait, à terme, aider à expliquer certaines formes d’infertilité et suggérer de nouvelles pistes de traitement des troubles reproductifs.
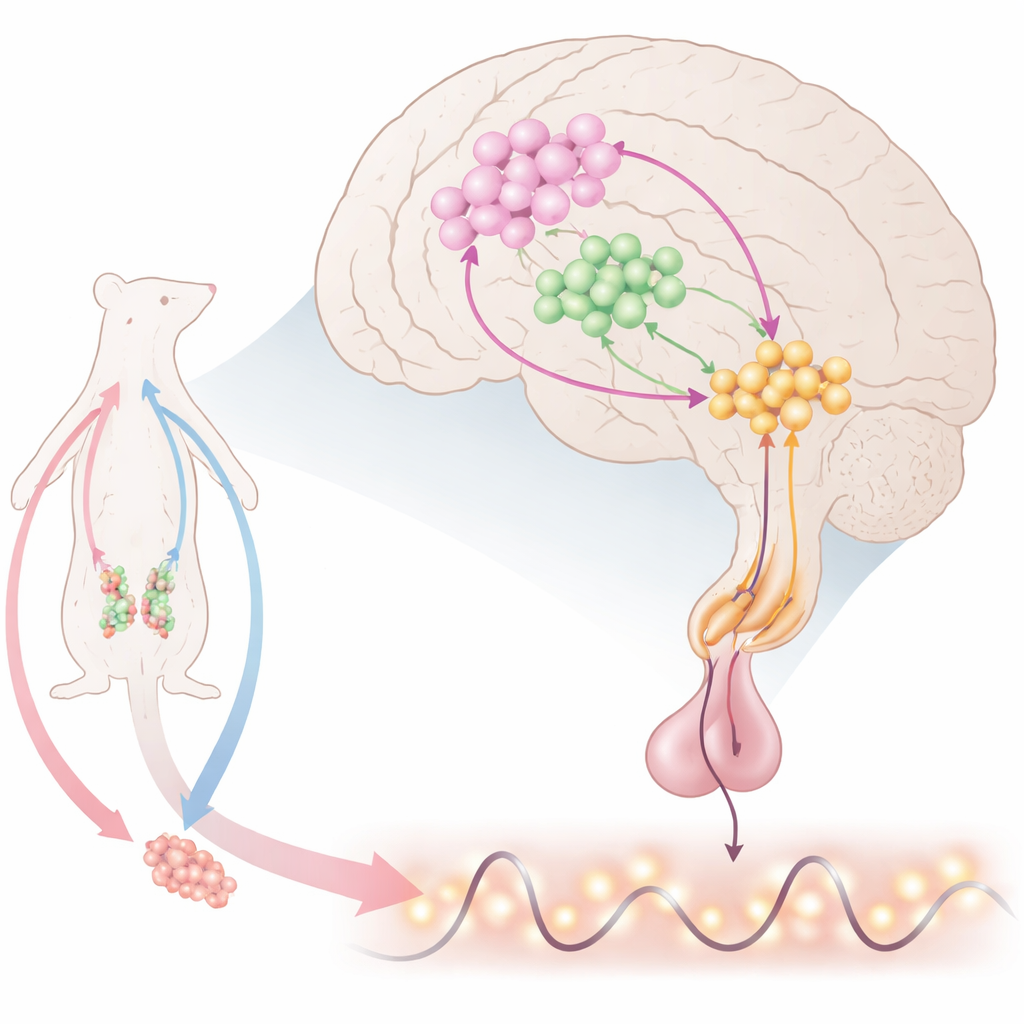
Le chronomètre cérébral de la reproduction
Au cœur du cerveau, des cellules nerveuses spécialisées libèrent l’hormone de libération des gonadotrophines (GnRH), qui commande à l’hypophyse de sécréter l’hormone lutéinisante (LH) et l’hormone folliculo-stimulante. Celles-ci contrôlent à leur tour les ovaires et les testicules. La GnRH n’est pas sécrétée de façon continue ; elle apparaît sous forme d’impulsions régulières et, chez la femelle, d’une forte poussée pré-ovulatoire. Les scientifiques savent que de nombreux signaux convergent vers les cellules GnRH, mais la combinaison précise qui produit à la fois les impulsions et les poussées est restée floue. Ce travail se concentre sur une petite région en avant de l’hypothalamus, où les cellules GnRH côtoient deux autres acteurs importants : des neurones producteurs de kisspeptine qui excitent la GnRH, et des neurones synthétisant l’oxyde nitrique (NO), un signal gazeux pouvant diffuser sur de courtes distances.
Un partenariat marche-arrêt entre deux signaux
Les chercheurs proposent un réseau « KiNG » en trois parties, composé de kisspeptine, de neurones producteurs de NO (nNOS) et de cellules GnRH. La kisspeptine est un activateur puissant capable de provoquer la libération de GnRH et de LH, mais une stimulation constante finit par neutraliser le système, ce qui suggère la nécessité d’un frein interne. À l’aide de sondes moléculaires très sensibles, d’outils génétiques et d’enregistrements sur coupes cérébrales de souris, l’équipe montre que la kisspeptine fait plus qu’exciter directement les neurones GnRH. Elle active également des neurones nNOS proches dans la zone préoptique, en particulier dans une région appelée OV/MePO. Quand les niveaux de kisspeptine augmentent, ces cellules nNOS produisent des bouffées de NO, qui déclenchent la production d’un second messager, le GMP cyclique (cGMP), dans les cellules environnantes, y compris les neurones GnRH eux‑mêmes. Ce signal NO–cGMP atténue le déclenchement des GnRH, fournissant un interrupteur d’arrêt intégré à la poussée de kisspeptine.
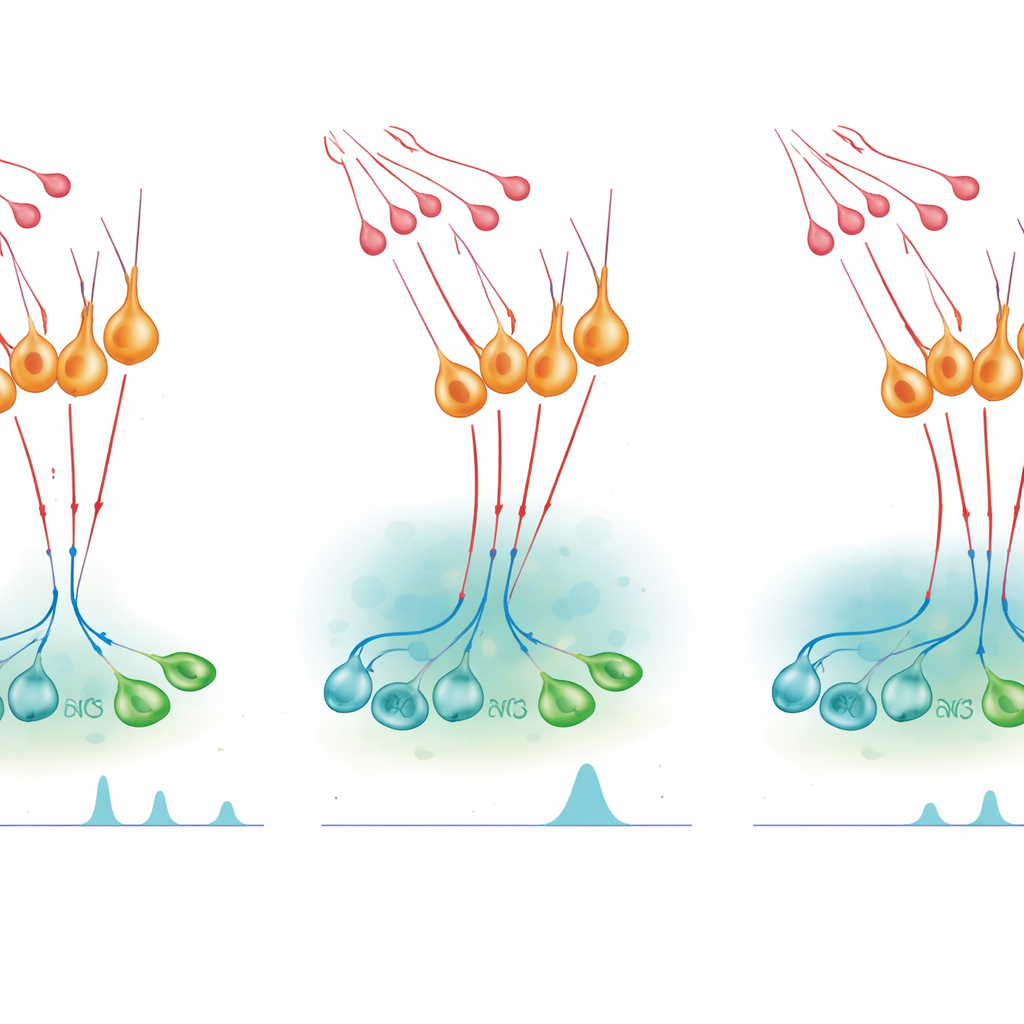
Provoquer des poussées hormonales et les modérer
Pour tester comment ce microcircuit affecte la libération hormonale, l’équipe a utilisé des interrupteurs chimiogénétiques — des récepteurs modifiés activés par un médicament par ailleurs inerte — pour activer ou inhiber les neurones nNOS in vivo chez la souris. L’activation artificielle des cellules nNOS pendant une phase normalement calme du cycle féminin suffisait à provoquer une élévation du taux de LH en sang semblable à une poussée, et l’effet était similaire chez les mâles. Le blocage de la production de NO abolissait cet effet, montrant que le NO produit par ces neurones est nécessaire à la poussée. Pourtant, lorsque les scientifiques ont inhibé les neurones nNOS ou réduit leur sensibilité à la kisspeptine, une injection de kisspeptine entraînait une montée de LH exagérée et prolongée. Des médicaments bloquant la synthèse du NO avaient un effet amplificateur comparable, tandis qu’un médicament prolongeant la signalisation du cGMP raccourcissait la réponse à la kisspeptine et diminuait la sécrétion ultérieure de LH. Ensemble, ces expériences indiquent que le NO aide à synchroniser les neurones GnRH pour créer des poussées tout en limitant la durée pendant laquelle la kisspeptine peut les maintenir en activité.
Un rythme flexible au cours du cycle ovarien
L’étude révèle aussi que cet équilibre marche‑arrêt change au fil du cycle féminin. À l’aide d’une méthode sensible de détection de l’ARN, les auteurs ont observé qu’un plus grand nombre de neurones nNOS expriment le récepteur de la kisspeptine le jour précédant l’ovulation, lorsque les taux d’œstrogènes sont élevés et que la poussée de LH survient. Pendant les phases plus calmes, moins de neurones nNOS répondent à la kisspeptine, produisant seulement de petites quantités locales de NO qui freinent doucement les impulsions de GnRH sans les arrêter. Le jour de la poussée, une entrée de kisspeptine plus forte et une expression réceptrice accrue amplifient massivement la production de NO, permettant à ce dernier de se diffuser plus loin et de mettre brièvement en silence de nombreux neurones GnRH simultanément. Au fur et à mesure que le signal NO s’estompe, ces cellules rebondissent ensemble, générant la forte et coordonnée poussée de LH nécessaire à l’ovulation.
Ce que cela signifie pour la santé humaine
En termes simples, ce travail montre que le même signal qui déclenche les neurones GnRH — la kisspeptine — recrute aussi un système de freinage différé via le NO, garantissant que les poussées hormonales soient puissantes mais pas incontrôlées. Le réseau KiNG agit donc à la fois comme accélérateur et comme frein de la temporalité reproductive, ajustant les impulsions de GnRH pendant la majeure partie du cycle et modulant la poussée qui déclenche l’ovulation. Étant donné que des altérations génétiques des voies de la kisspeptine et du NO ont été identifiées chez des personnes présentant des problèmes de reproduction, la compréhension de ce circuit finement équilibré pourrait éclairer de nouvelles approches pour diagnostiquer et traiter l’infertilité et les affections connexes.
Citation: Delli, V., Moulinier, M., Lazaridou, AM. et al. Preoptic kisspeptin-nNOS-GnRH (KiNG) neuronal network regulates LH rhythmicity through activation-inhibition in mice. Nat Commun 17, 2558 (2026). https://doi.org/10.1038/s41467-026-69316-0
Mots-clés: hormones reproductrices, hypothalamus, kisspeptine, oxyde nitrique, moment de l’ovulation