Clear Sky Science · fr
La lactylation des histones augmente l’expression de CXCL1 favorisant l’infiltration de neutrophiles et l’échappement immunitaire dans le cancer du pancréas
Pourquoi cette étude sur le cancer est importante
Le cancer du pancréas est l’un des cancers les plus mortels, en partie parce qu’il résiste souvent aux immunothérapies modernes efficaces dans d’autres tumeurs. Cette étude révèle comment les tumeurs pancréatiques réorientent leur propre métabolisme du glucose pour neutraliser discrètement le système immunitaire, et comment bloquer ce processus pourrait rouvrir une voie pour que les défenses de l’organisme — et des médicaments existants — puissent riposter.
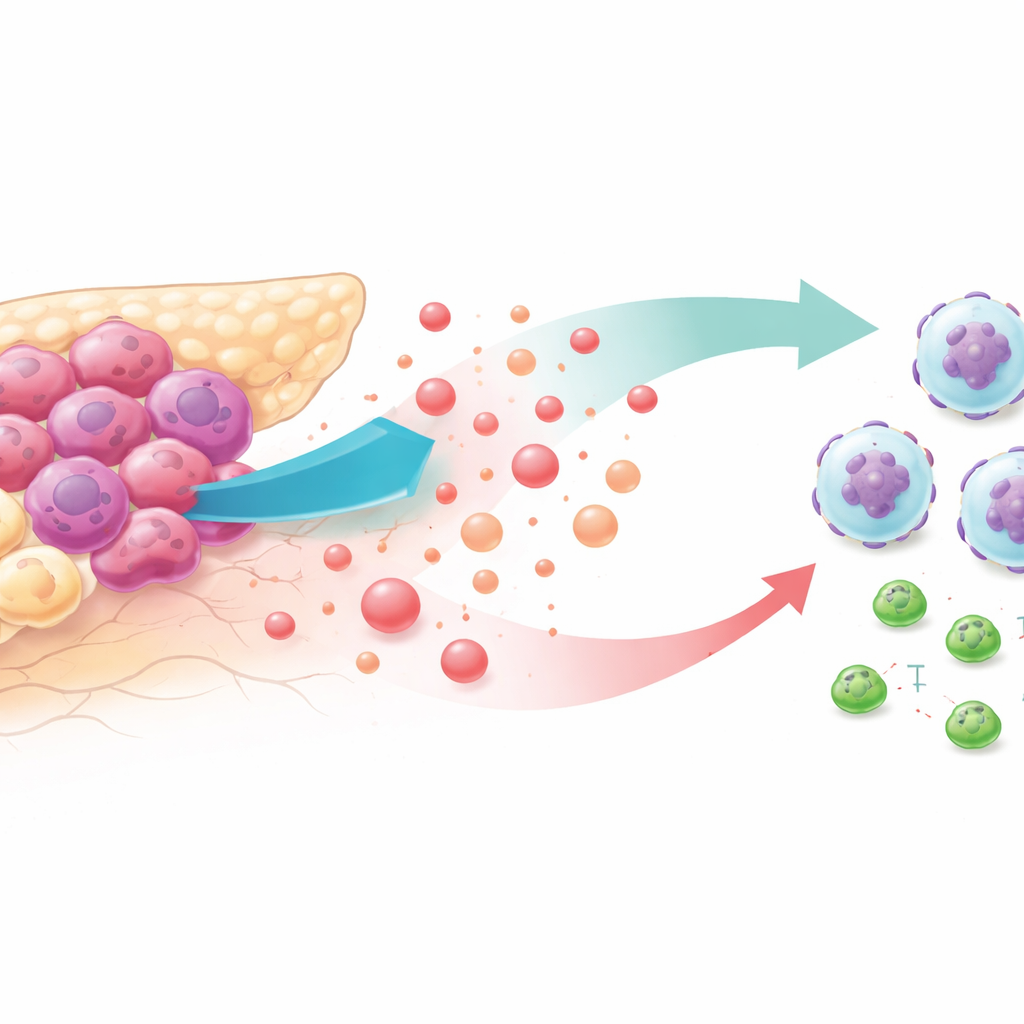
Tumeurs gluco-dépendantes et voisinage hostile
Les cellules cancéreuses sont réputées pour brûler le glucose à un rythme effréné, même lorsque l’oxygène est disponible. Ce « mode de vie à haute glycolyse » inonde le microenvironnement tumoral de lactate, un produit considéré autrefois comme un déchet métabolique. En analysant des bases de données de tumeurs de patients et des modèles murins, les chercheurs ont découvert que les cancers du pancréas les plus glycolytiques étaient fortement infiltrés par des neutrophiles — des globules blancs qui, dans ce contexte, favorisent la croissance tumorale — et présentaient moins de lymphocytes T CD8 tueurs de cancer. Les patients dont les tumeurs avaient ce profil avaient tendance à avoir une survie plus courte, ce qui suggère un lien étroit entre altération métabolique et échappement immunitaire.
Comment les tumeurs utilisent le lactate pour appeler la mauvaise aide
Pour comprendre comment la glycolyse attire les neutrophiles, l’équipe a réduit la glycolyse tumorale avec des médicaments ou des manipulations génétiques dans des lignées de cancer du pancréas et chez la souris. Lorsque la dégradation du sucre était bloquée, les cellules tumorales libéraient beaucoup moins un signal chimique appelé CXCL1, et les niveaux circulants de ce signal diminuaient chez la souris et dans des échantillons de patients. Lors d’essais de migration en laboratoire, les neutrophiles se déplaçaient volontiers vers le milieu issu de cellules cancéreuses très glycolytiques mais pas vers le milieu provenant de cellules avec glycolyse inhibée — sauf si les chercheurs réintroduisaient du CXCL1 purifié. Chez des souris vivantes, restaurer le CXCL1 dans des tumeurs dont la glycolyse était réduite ramenait le nombre de neutrophiles et affaiblissait l’effet anti-tumoral de l’inhibition de la glycolyse.
Un nouvel interrupteur épigénétique contrôlé par le lactate
L’étude est ensuite descendue au niveau de l’emballage de l’ADN. Nos gènes sont enroulés autour de protéines en forme de bobines appelées histones, dont les marques chimiques agissent comme des interrupteurs d’activité des gènes. Les auteurs montrent que, dans le cancer du pancréas, le lactate produit par la glycolyse ajoute une marque spécifique « lactyle » à une position d’histone connue sous le nom H3K18. Cette modification, appelée lactylation de l’histone H3K18, était nettement plus élevée dans les tissus tumoraux que dans le pancréas normal. Lorsque la glycolyse était bloquée, la lactylation en H3K18 diminuait, en particulier près de la région régulatrice du gène CXCL1, et la production de CXCL1 chutait. La réintroduction de lactate rétablissait à la fois la marque sur l’histone et l’expression de CXCL1. Dans les échantillons de patients, les tumeurs présentant plus de lactylation H3K18 montraient également des niveaux plus élevés de CXCL1, reliant ainsi cette marque moléculaire à un paysage immunitaire pro-tumoral.
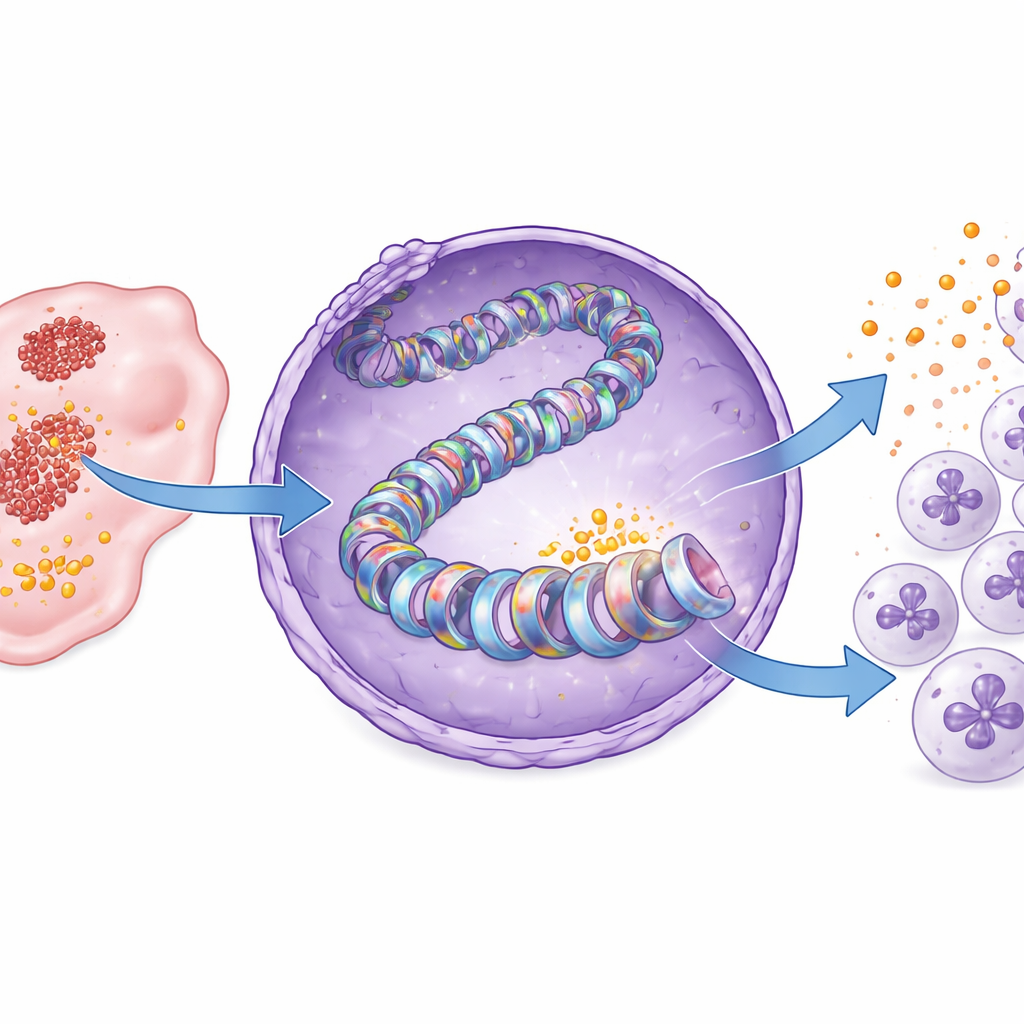
Identification de l’enzyme et d’une faiblesse exploitable
Les marques histoniques sont écrites par des enzymes spécialisées. En testant des inhibiteurs de protéines connues modifiant les histones, les chercheurs ont identifié une enzyme appelée PCAF comme rédactrice clé de la marque de lactylation H3K18 dans le cancer du pancréas. La modélisation structurale suggérait que PCAF peut se lier au lactyl-CoA, la forme activée du lactate utilisée pour le marquage, et des essais biochimiques ont confirmé que la PCAF purifiée peut directement ajouter des groupes lactyle à l’histone H3. Bloquer PCAF avec une petite molécule, la bromosporine, réduisait la lactylation H3K18 et la production de CXCL1 dans les cellules cancéreuses et dans les tumeurs de souris. En conséquence, moins de neutrophiles pénétraient dans les tumeurs, davantage de lymphocytes T CD8 s’accumulaient, et la croissance tumorale ralentissait, sans perte de poids ou toxicité évidente chez les souris.
Rendre une tumeur « froide » plus « chaude » par une thérapie combinée
Étant donné que les inhibiteurs de points de contrôle immunitaires standard, tels que les anticorps anti–PD-1, ont montré un succès limité dans le cancer du pancréas, l’équipe a évalué si démanteler la voie lactate–PCAF–CXCL1 pouvait rendre ces tumeurs plus réceptives. Dans des modèles murins sous-cutanés et orthotopes pancréatiques, la bromosporine associée à une thérapie anti–PD-1 a réduit les tumeurs davantage que chaque traitement seul, diminué l’infiltration de neutrophiles, augmenté les lymphocytes T CD8 actifs, et prolongé significativement la survie. Cela suggère que couper la « sirène » métabolique tumorale attirant les neutrophiles aide à transformer une tumeur immunologiquement « froide » en une tumeur plus « chaude » que la thérapie de blocage de points de contrôle peut mieux cibler.
Ce que cela signifie pour les traitements futurs
En termes clairs, l’étude révèle une chaîne d’événements : les tumeurs pancréatiques brûlent du sucre, libèrent du lactate, utilisent ce lactate pour actionner un interrupteur épigénétique sur leurs protéines d’empaquetage de l’ADN, augmentent la production de CXCL1, et attirent ainsi des neutrophiles qui les aident à se cacher des lymphocytes T tueurs. Interrompre cette chaîne au niveau de la PCAF avec un médicament ralentit non seulement les tumeurs mais rend aussi l’immunothérapie existante plus efficace chez la souris. Bien que des travaux supplémentaires soient nécessaires pour garantir la sécurité et définir la meilleure façon de cibler cette voie chez l’homme, ces résultats soulignent une stratégie prometteuse : reprogrammer le métabolisme tumoral et les commutateurs géniques pour donner au système immunitaire une chance équitable.
Citation: Zhang, P., Ma, J., Wan, Y. et al. Histone lactylation increases CXCL1 expression for neutrophil infiltration and immune escape in pancreatic cancer. Nat Commun 17, 2526 (2026). https://doi.org/10.1038/s41467-026-69311-5
Mots-clés: cancer du pancréas, métabolisme tumoral, lactylation des histones, microenvironnement tumoral, immunothérapie du cancer