Clear Sky Science · fr
Exploiter la cinétique de liaison prévisible du DNA-PAINT pour débruiter des images en super-résolution
Des vues plus nettes du monde minuscule
Les microscopes modernes peuvent désormais « voir » des molécules individuelles à l’intérieur des cellules, mais ces images sont souvent parsemées de points de fond trompeurs. Cette étude présente une méthode pour nettoyer ces images en tirant parti de la façon dont des fragments d’ADN s’assemblent et se détachent naturellement au fil du temps. Le résultat est des images plus nettes des machines moléculaires intracellulaires, ce qui compte pour tout, de la biologie fondamentale à la découverte de médicaments.
Comment un clignotement révèle des détails cachés
Une méthode d’imagerie puissante, appelée DNA-PAINT, transforme l’adhérence aléatoire de courts brins d’ADN en un microscope super‑résolution. Un brin d’ADN est attaché à la protéine que le chercheur souhaite observer ; un brin complémentaire portant une sonde fluorescente flotte dans la solution. Lorsque le brin flottant se lie brièvement à son partenaire, il produit un minuscule éclat de lumière. En enregistrant de nombreux clignotements et en localisant précisément leur position, les chercheurs peuvent reconstruire les emplacements des protéines avec une précision nanométrique — bien plus fine que celle des microscopes optiques conventionnels.
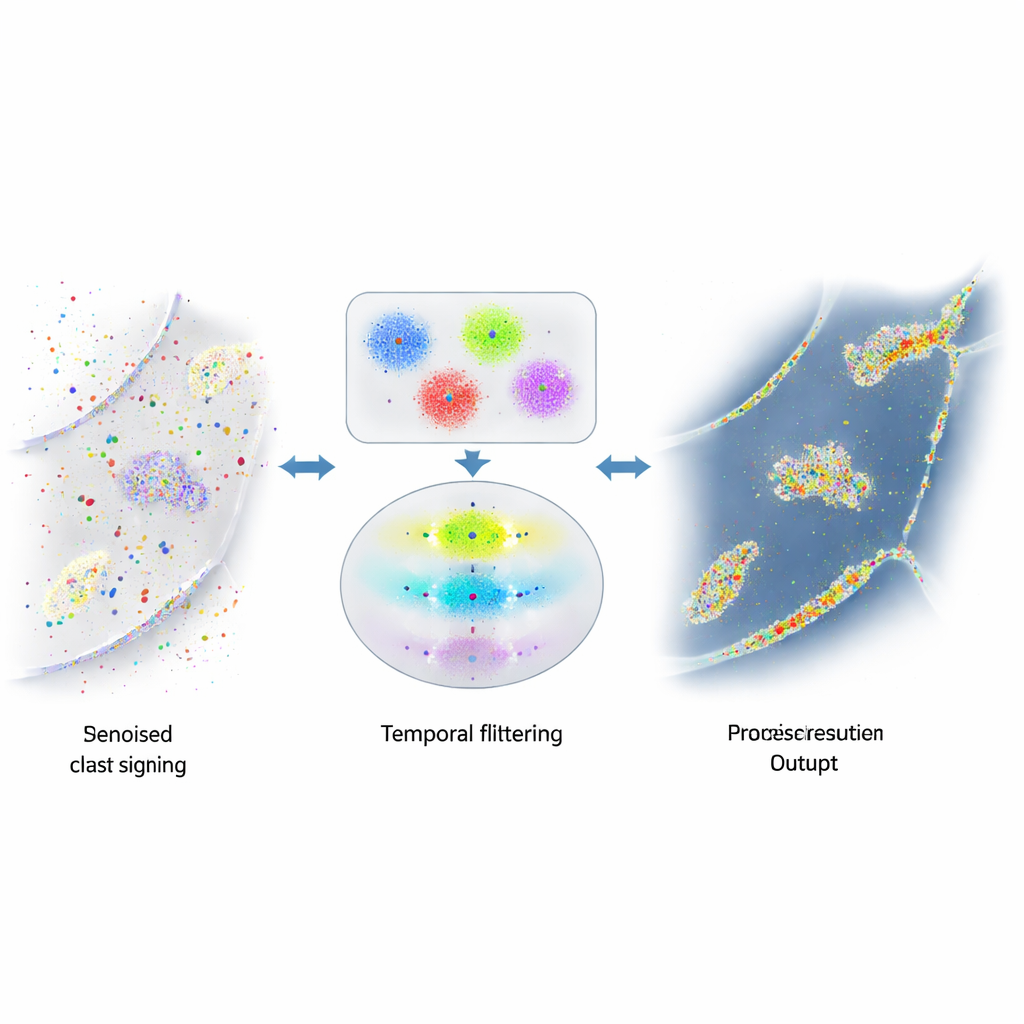
Quand les signaux utiles sont noyés dans le bruit
La force du DNA-PAINT — la présence de nombreux brins fluorescents libres — crée aussi un problème. Ces brins adhèrent parfois là où ils ne devraient pas, par exemple à des surfaces cellulaires aléatoires ou à l’ADN abondant du noyau. Ces éclairs accidentels sont indiscernables visuellement des vrais et encombrent l’image finale de points et d’amas faux. Les tentatives antérieures pour réduire ce bruit se sont concentrées sur la chimie pour rendre les adhérences indésirables plus rares, ou sur des règles grossières pour repérer les outliers évidents. Pourtant une quantité substantielle de signal trompeur persistait, limitant la fiabilité des mesures du nombre de protéines ou de leurs relations spatiales.
Utiliser le temps pour distinguer vérité et tromperie
Les auteurs ont réalisé que les véritables paires d’ADN en DNA-PAINT obéissent à une règle temporelle simple : les pauses entre événements de liaison authentiques suivent un comportement exponentiel prévisible. En revanche, les adhérences aléatoires n’obéissent pas à ce schéma. Ils ont construit un algorithme en plusieurs étapes qui regroupe d’abord les clignotements proches en petits amas selon leur emplacement, en combinant un clustering basé sur la densité et le k‑means pour décomposer des formes complexes en unités de la taille d’une localisation. Pour chaque amas, ils construisent ensuite une « trace temporelle » des événements de liaison, en fusionnant soigneusement les clignotements on‑off rapides provenant d’une même liaison en événements uniques. Enfin, ils appliquent un test statistique pour vérifier si les intervalles entre événements dans chaque amas correspondent au comportement exponentiel attendu. Les amas qui passent le test sont considérés comme réels ; ceux qui échouent sont écartés comme bruit.
Mettre la méthode à l’épreuve dans des cellules réelles
Pour tester leur approche, l’équipe a imagé la protéine d’adhésion cellulaire E‑cadherin dans des chambres d’œufs de drosophile, où certaines cellules produisaient la protéine marquée et les cellules voisines n’en produisaient pas. Cela a créé des zones juxtaposées riches en signal authentique et des zones qui ne devraient contenir que du fond. En ajustant le nombre d’événements de liaison qu’un amas doit montrer avant d’être testé, ils ont trouvé des paramètres qui éliminaient plus de 90 % des amas spurieux tout en conservant plus de 98 % des vrais amas aux frontières cellulaires. Dans les images débruitées, des détails fins comme de minces structures tubulaires et des vésicules sont devenus beaucoup plus nets. La même stratégie a fonctionné sur d’autres systèmes, y compris les mitochondries et les microtubules, et même sur des protéines à distribution plus diffuse et amorphe, où les seuls motifs spatiaux ne permettent pas de distinguer le réel du faux.
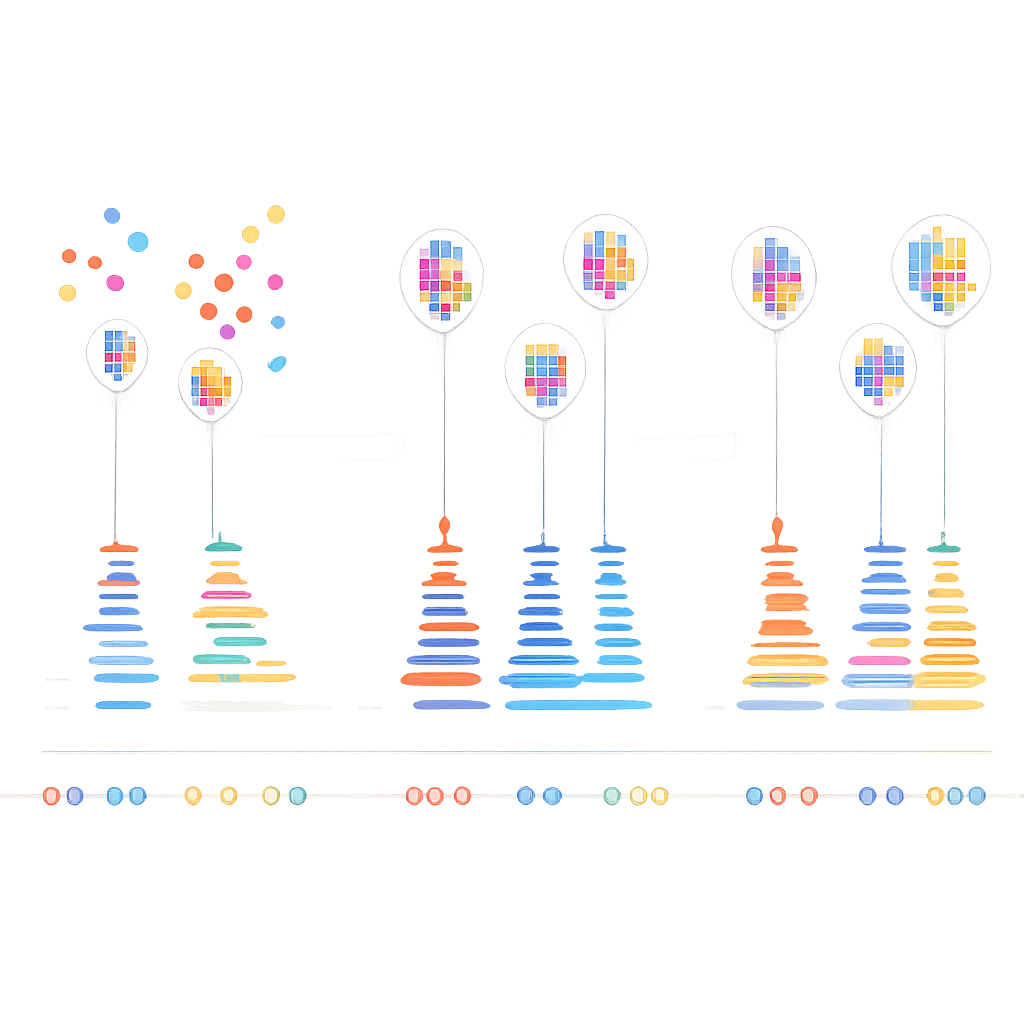
Des cartes moléculaires plus claires pour les études futures
En « écoutant » le « rythme » de la liaison de l’ADN plutôt qu’en se contentant d’examiner où se produisent les clignotements, cette méthode élimine de manière fiable le fond trompeur des données DNA‑PAINT. Pour les non‑spécialistes, le résultat clé est simple : des cartes moléculaires intracellulaires plus nettes et plus fiables. Cela rend plus sûr le comptage du nombre de molécules de protéines présentes, l’évaluation de la proximité entre différentes protéines et la construction d’images plus précises de la vie intérieure des cellules. À mesure que l’imagerie basée sur l’ADN se développe, ce type de débruitage intelligent sera essentiel pour transformer des images criblées de points en connaissances biologiques solides.
Citation: Sirinakis, G., Allgeyer, E.S., Richens, J.H. et al. Utilizing the predictable binding kinetics of DNA-PAINT to denoise super-resolution images. Nat Commun 17, 2397 (2026). https://doi.org/10.1038/s41467-026-69304-4
Mots-clés: DNA-PAINT, microscopie super-résolution, dénosion d'image, imagerie mono‑moléculaire, cartographie des protéines