Clear Sky Science · fr
L’activation de STING induit des réponses cytotoxiques et immunitaires dans les méningiomes via des voies de mort cellulaire inflammatoire
Retourner les alarmes du corps contre les tumeurs cérébrales
Les méningiomes font partie des tumeurs cérébrales les plus fréquentes ; si la chirurgie et la radiothérapie sont souvent efficaces, certaines tumeurs récidivent. Ces lésions réfractaires peuvent provoquer des crises, des céphalées et un handicap, et il n’existe pas de traitement médicamenteux largement accepté. Cette étude examine une stratégie consistant à faire déclencher une alarme interne puissante par les cellules tumorales elles‑mêmes et les cellules immunitaires avoisinantes, en utilisant une molécule qui active un système inné de détection du danger appelé STING. L’objectif est non seulement de tuer directement les cellules tumorales, mais aussi d’éveiller le système immunitaire et d’assouplir l’armature dense du tumeur.
Une tumeur dissimulée dans un voisinage immunitaire calme
Les auteurs ont d’abord cartographié le « quartier » cellulaire des méningiomes humains par séquençage unicellulaire et imagerie spatiale. Ils ont observé que ces tumeurs sont riches en cellules immunitaires innées, en particulier des macrophages, tandis que les lymphocytes T et les cellules NK, effecteurs classiques de l’antitumoral, sont rares et souvent épuisés. Autour des cellules tumorales se trouve une coque dense de collagène et d’autres protéines de matrice formant une structure superposée et protectrice. De nombreux macrophages dans ces régions portent des récepteurs inhibiteurs activés par le collagène, créant un environnement fortement suppressif où les cellules immunitaires sont présentes mais retenues plutôt que libérées contre le cancer.
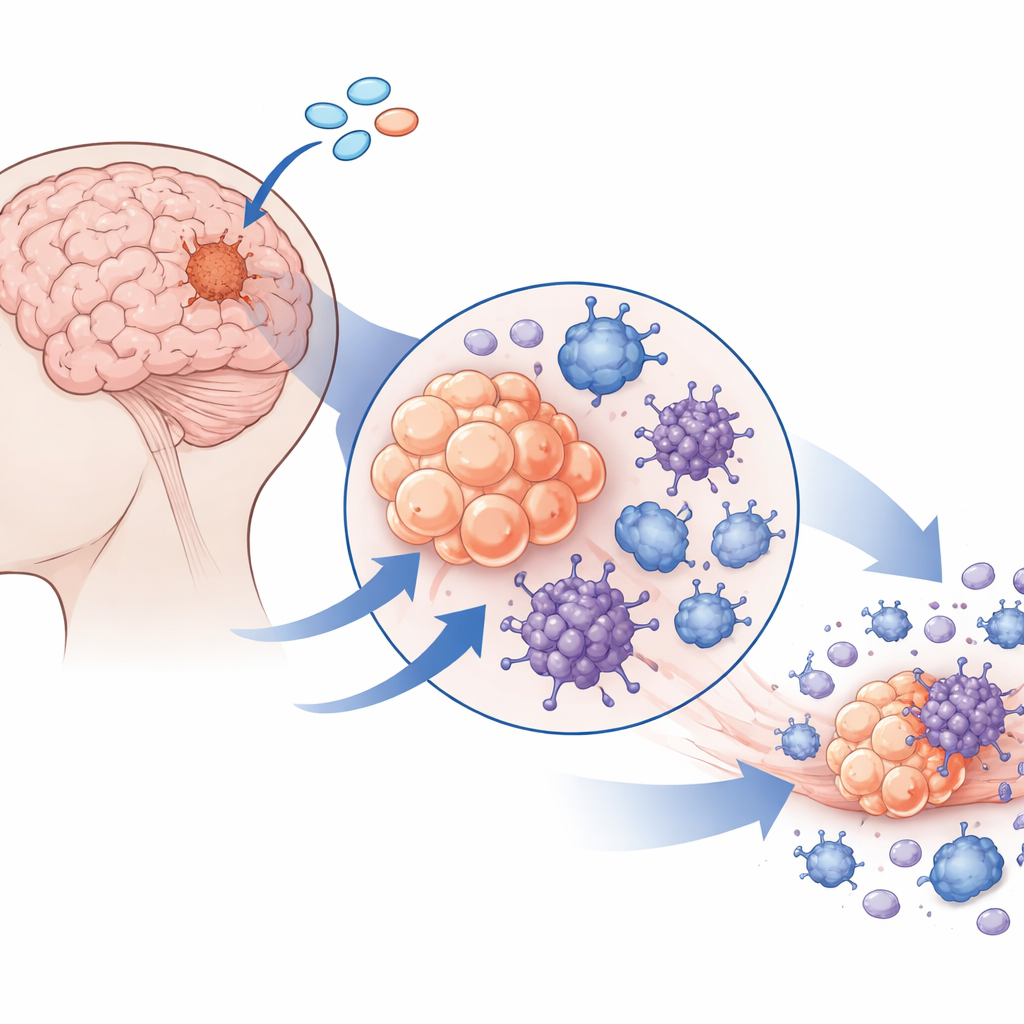
Découvrir un interrupteur que les cellules tumorales conservent
Ensuite, l’équipe a recherché des voies capables d’inverser cet état suppressif en un état inflammatoire hostile à la tumeur. Ils se sont concentrés sur STING, un capteur qui répond normalement à l’ADN anormalement localisé dans les cellules et déclenche des réponses antivirales et inflammatoires. Contrairement à de nombreuses autres tumeurs cérébrales, les cellules de méningiome présentaient des niveaux de STING inhabituellement élevés. Cela s’expliquait par une chromatine ouverte et une faible méthylation de l’ADN au niveau du gène STING, ce qui signifie que le gène est épigénétiquement prêt à être actif. STING était abondant non seulement dans les cellules tumorales mais aussi dans les cellules vasculaires voisines et les macrophages, suggérant qu’un seul médicament pourrait simultanément affecter de nombreux acteurs clés du microenvironnement tumoral.
Forcer les cellules tumorales dans une autodestruction enflammée
Les chercheurs ont traité des échantillons de méningiomes fraîchement prélevés chez des patients avec un agoniste puissant de STING appelé 8803. Même lorsqu’on avait éliminé les cellules immunitaires, les cellules tumorales mouraient, prouvant un effet direct. En ajoutant des médicaments qui bloquent sélectivement différentes voies de mort cellulaire et en analysant l’activité génique, ils ont montré que 8803 ne provoquait pas simplement une apoptosis calme. Au contraire, il poussait les cellules de méningiome vers plusieurs formes inflammatoires de mort — pyroptose, nécroptose et ferroptose — qui provoquent l’éclatement des cellules plutôt que leur démantèlement ordonné. Une étape clé était l’activation et la clivage d’une protéine appelée gasdermine D, qui forme des pores dans la membrane cellulaire. La microscopie électronique a révélé des cellules tumorales criblées de trous membranaires et de mitochondries endommagées ; le blocage des espèces réactives de l’oxygène a réduit la mort cellulaire, reliant le stress mitochondrial à cette disparition enflammée.
Des débris tumoraux à l’éveil immunitaire et à l’érosion de la matrice
Lorsque les cellules tumorales meurent de façon aussi dramatique, elles libèrent des molécules de « danger » capables de stimuler les cellules immunitaires. L’équipe a exposé des macrophages de souris à des cellules de méningiome lysées et observé une montée de facteurs inflammatoires et d’enzymes qui dégradent le collagène, en particulier la métalloprotéinase de matrice‑3 (MMP‑3). En travaillant avec des souris déficientes pour certains adaptateurs de signalisation, ils ont montré que les récepteurs de type toll, un autre système de détection du danger, sont cruciaux pour cette réponse, tandis que l’activation de STING par 8803 ajoute une couche supplémentaire de stimulation immunitaire. Dans des modèles murins de méningiome, l’injection directe de 8803 dans les tumeurs a réduit ou stabilisé la croissance, prolongé la survie et converti le site tumoral d’une masse calme et riche en collagène en une région envahie par des macrophages actifs, des cellules NK et T, avec une coloration du collagène fortement diminuée.
Pourquoi cette approche pourrait changer le traitement des patients
Globalement, l’étude montre que les méningiomes recèlent une vulnérabilité intrinsèque : leurs cellules tumorales conservent un interrupteur STING accessible qui, lorsqu’il est actionné par 8803, les conduit à une mort cellulaire explosive et inflammatoire. Ce processus tue les cellules cancéreuses et inonde la région de signaux d’alarme qui recrutent et stimulent les cellules immunitaires, tout en contribuant à la dégradation de l’armature de collagène responsable de l’effet de masse. Parce que les méningiomes sont généralement localisés plutôt que massivement métastatiques, et que les options standards sont limitées pour les formes récidivantes, un agoniste STING délivré localement comme 8803 pourrait offrir une nouvelle manière ciblée à la fois de décharger les tumeurs et de reprogrammer leur microenvironnement immunitaire pour un contrôle durable.
Citation: Youngblood, M.W., Tripathi, S., Najem, H. et al. STING activation induces cytotoxic and immune responses in meningiomas via inflammatory cell death pathways. Nat Commun 17, 2685 (2026). https://doi.org/10.1038/s41467-026-69296-1
Mots-clés: méningiome, voie STING, immunothérapie des tumeurs cérébrales, mort cellulaire inflammatoire, microenvironnement tumoral