Clear Sky Science · fr
Adgrg6/Gpr126 est nécessaire à l'intégrité de la paroi compacte et à l'établissement de l'identité trabéculaire lors de la trabéculation cardiaque
Pourquoi l'architecture de la paroi cardiaque compte
Chaque battement de cœur dépend d'une paroi interne finement structurée. Chez les embryons en développement, cette paroi se forme d'abord comme une couche lisse puis pousse une forêt de crêtes musculaires appelées trabécules qui aident le cœur à pomper efficacement. Lorsque ce processus s'altère, des cardiomyopathies graves peuvent apparaître chez l'enfant et l'adulte. Cette étude explore comment un récepteur peu connu, Gpr126, aide les cellules cardiaques à choisir entre rester dans la paroi compacte lisse ou devenir partie de ces crêtes internes.
Un récepteur à fonctions séparées dans le cœur
Gpr126 appartient à une famille de récepteurs couplés aux protéines G d'adhésion qui siègent dans la membrane cellulaire et détectent l'environnement cellulaire. Ces récepteurs sont particulièrement intéressants car de nombreux médicaments existants ciblent des récepteurs apparentés, ce qui en fait des candidats thérapeutiques attractifs. Gpr126 est inhabituel en ce qu'il est naturellement clivé en deux grandes fragments : un fragment N-terminal (NTF), qui dépasse de la cellule et peut faciliter l'adhésion cellule–cellule, et un fragment C-terminal (CTF), qui traverse la membrane et déclenche la signalisation intracellulaire. Des travaux antérieurs avaient relié Gpr126 au développement cardiaque, mais il restait flou ce que chaque fragment accomplissait pendant la formation des trabécules.
Utiliser le poisson zèbre pour observer la formation du cœur
Les chercheurs ont utilisé le poisson zèbre, dont les embryons transparents permettent l'imagerie en temps réel du cœur battant. Ils ont étudié deux variantes génétiques de gpr126. L'une (stl47) produit seulement une protéine très courte et sévèrement tronquée ; l'autre (st49) produit un NTF sécrété et stable qui est dépourvu de la partie CTF assurant la signalisation. En combinant ces mutants avec des lignées rapporteurs fluorescentes, l'équipe a pu voir les cellules cardiaques individuelles, suivre la formation des trabécules et surveiller des molécules clés comme la N-cadhérine (qui aide les cellules à rester liées) et Notch (une voie de signalisation qui indique aux cellules quelle identité adopter).
Maintenir la paroi vs. former les crêtes
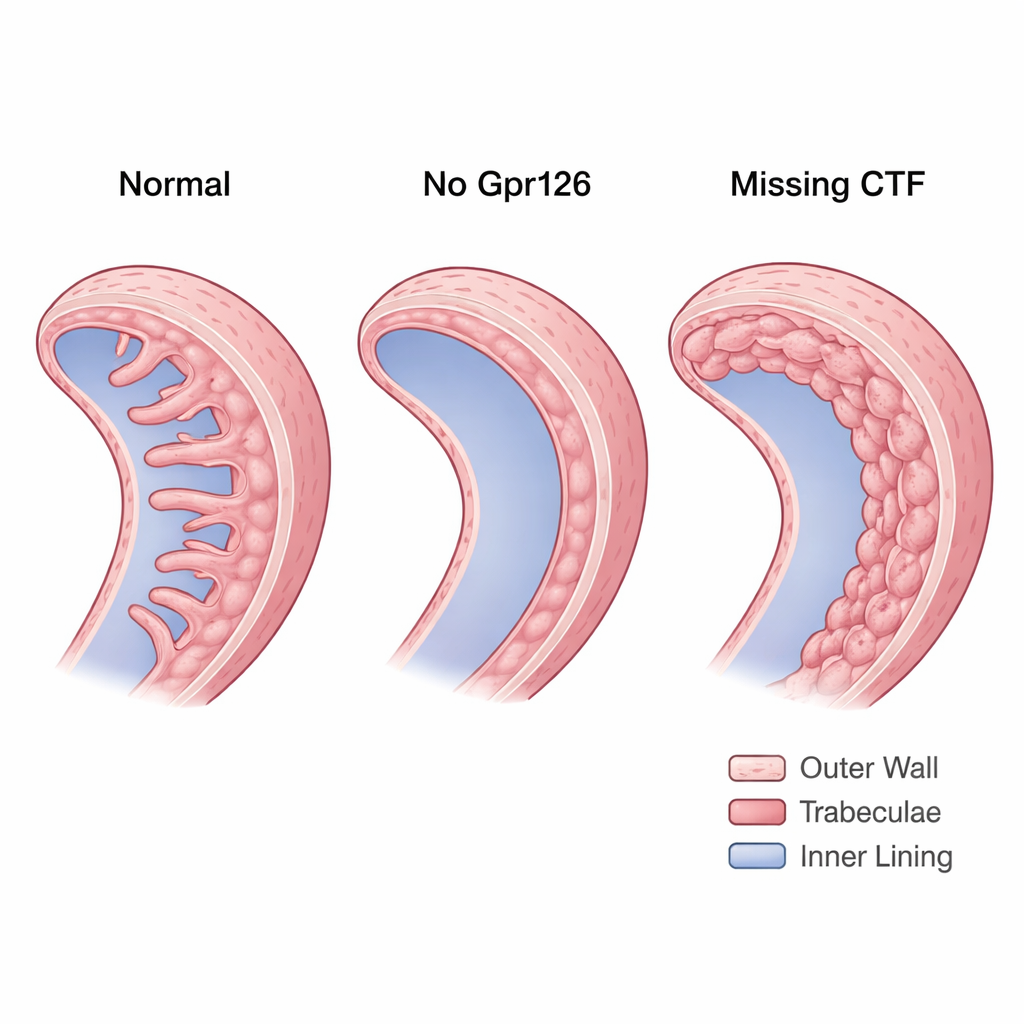
Les mutants stl47, qui manquent essentiellement des deux fragments fonctionnels, ont montré que Gpr126 est nécessaire à la formation de trabécules normales. Dans les embryons materno-zygotiques stl47 — où aucun Gpr126 sain ne provient d'aucun parent — de nombreux cœurs se sont développés avec des trabécules absentes ou fortement réduites. La N-cadhérine, qui dans les cœurs sains se concentre proprement sur les côtés des cardiomyocytes de la paroi compacte, apparaissait dispersée à la surface cellulaire. Cette désorganisation suggérait que, sans le NTF, l'adhésion cellule–cellule dans la paroi compacte devient instable, sapant la fondation sur laquelle les trabécules devraient se construire.
Trop de paroi, pas assez d'identité
Les mutants st49, qui produisent toujours le NTF mais n'ont pas le CTF, montraient le problème opposé. Au lieu d'un manque de trabécules, leurs cœurs formaient une paroi interne épaisse et multilamellaire. Ces couches supplémentaires n'étaient pas de véritables trabécules : les cellules restaient polarisées comme des cellules de la paroi compacte et n'ont pas remodelé leurs contacts de N-cadhérine en le motif ponctué typique des cellules formant des crêtes. À l'aide d'un rapporteur d'activité Notch, l'équipe a constaté que ces cœurs présentaient une signalisation Notch anormalement élevée dans le myocarde. Une activité Notch élevée est connue pour maintenir les cellules dans la paroi compacte et les empêcher de se délaminer en trabécules. De manière importante, lorsque les chercheurs ont réintroduit uniquement le CTF dans les cellules endocardiales, les trabécules sont réapparues et l'activité Notch est redescendue vers la normale, montrant que la signalisation du CTF est cruciale pour conférer une identité trabéculaire aux cardiomyocytes.
Équilibrer les signaux pour un cœur sain
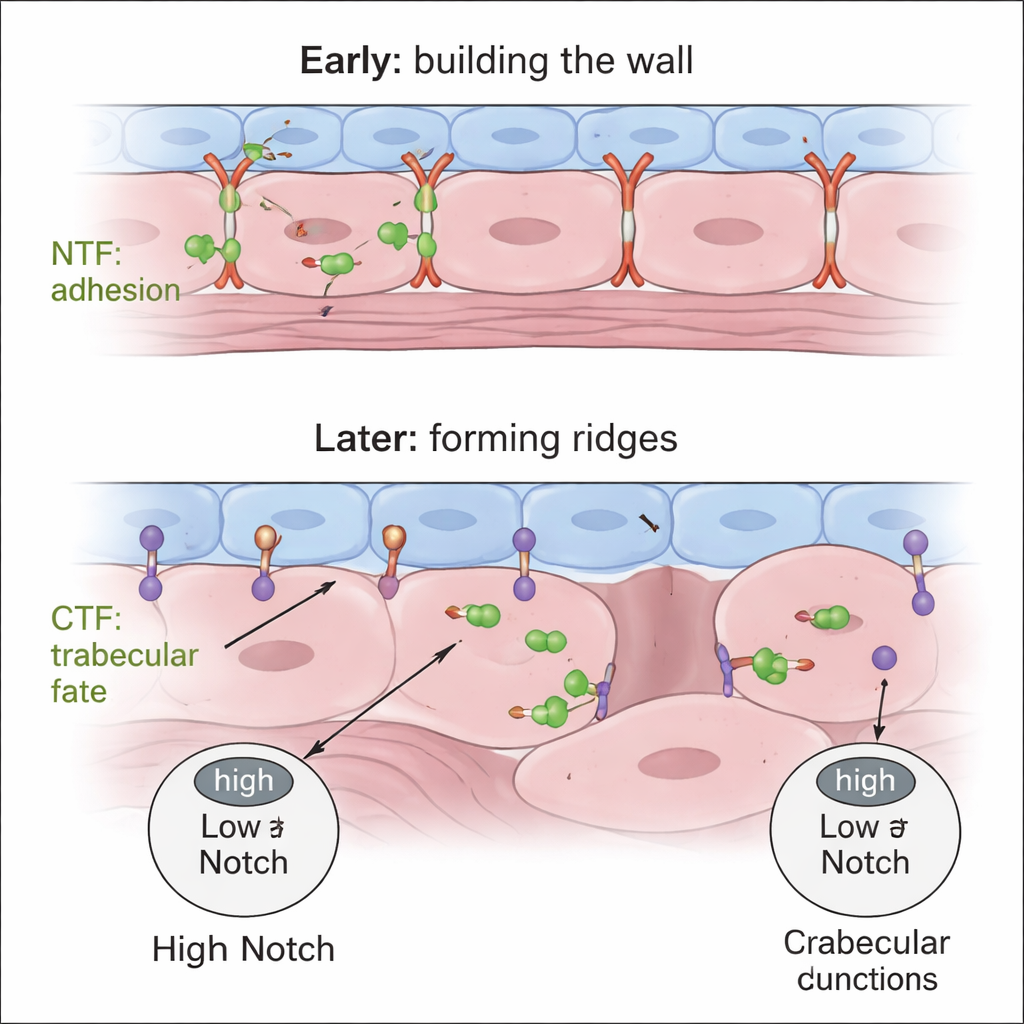
Pris ensemble, les résultats soutiennent un modèle en deux étapes et en deux parties. D'abord, le NTF sécrété de Gpr126 aide les cardiomyocytes de la paroi compacte à maintenir des jonctions serrées et correctement positionnées, assurant une paroi monolamellaire robuste. Plus tard, le CTF — agissant depuis les cellules endocardiales — module la signalisation Notch myocardiale afin qu'une partie seulement des cardiomyocytes se dépolarisent, relâchent leurs jonctions et protrudent vers l'intérieur pour former des trabécules, tandis que leurs voisines restent dans la paroi compacte. Si le NTF manque, la paroi ne s'organise jamais correctement ; si le CTF manque, la paroi prolifère excessivement et les cellules n'adoptent pas l'identité trabéculaire. Ce contrôle spécifique des domaines de l'architecture de la paroi cardiaque met en évidence Gpr126 comme un lien potentiel entre l'adhésion cellulaire, des voies de signalisation comme Notch et les cardiopathies structurelles, et suggère que régler différentes parties d'un même récepteur pourrait un jour aider à corriger des défauts du développement.
Citation: Srivastava, S., Gunawan, F., Vergarajauregui, S. et al. Adgrg6/Gpr126 is required for compact wall integrity and establishing trabecular identity during cardiac trabeculation. Nat Commun 17, 1484 (2026). https://doi.org/10.1038/s41467-026-69292-5
Mots-clés: trabéculation cardiaque, Gpr126, développement cardiaque, signalisation Notch, modèle de poisson zèbre