Clear Sky Science · fr
Le moteur génétique de l’encéphalopathie nécrosante aiguë, RANBP2, régule la réponse inflammatoire à l’infection par le virus de la grippe A
Quand la grippe endommage le cerveau
La plupart des gens imaginent la grippe comme une semaine de fièvre, de toux et de repos au lit. Pourtant, dans de rares cas, en particulier chez les enfants, une infection grippale banale peut soudainement dégénérer en un trouble cérébral potentiellement mortel appelé encéphalopathie nécrosante aiguë (ENA). Les familles et les médecins ont longtemps suspecté que des facteurs génétiques contribuent à déterminer qui développera cette complication catastrophique. Cette étude révèle comment une seule protéine gardienne cellulaire, RANBP2, maintient normalement le virus de la grippe sous contrôle et empêche la propre réponse inflammatoire de l’organisme de se déchaîner.
Une complication grippale rare mais dévastatrice
L’ENA survient brusquement après une maladie fébrile, souvent une grippe, et peut rapidement provoquer des convulsions, un coma et des lésions neurologiques permanentes. Environ la moitié des épisodes d’ENA connus dans le monde sont liés au virus de la grippe A, en particulier la souche H1N1. Les enfants qui héritent de certaines altérations du gène RANBP2 présentent un risque beaucoup plus élevé, dans une pathologie appelée ENA1. Jusqu’à présent, cependant, les scientifiques ne comprenaient pas ce que faisait réellement cette protéine lors d’une infection grippale, ni pourquoi sa modification rendrait l’inflammation cérébrale si sévère.
Portes cellulaires et génomes viraux
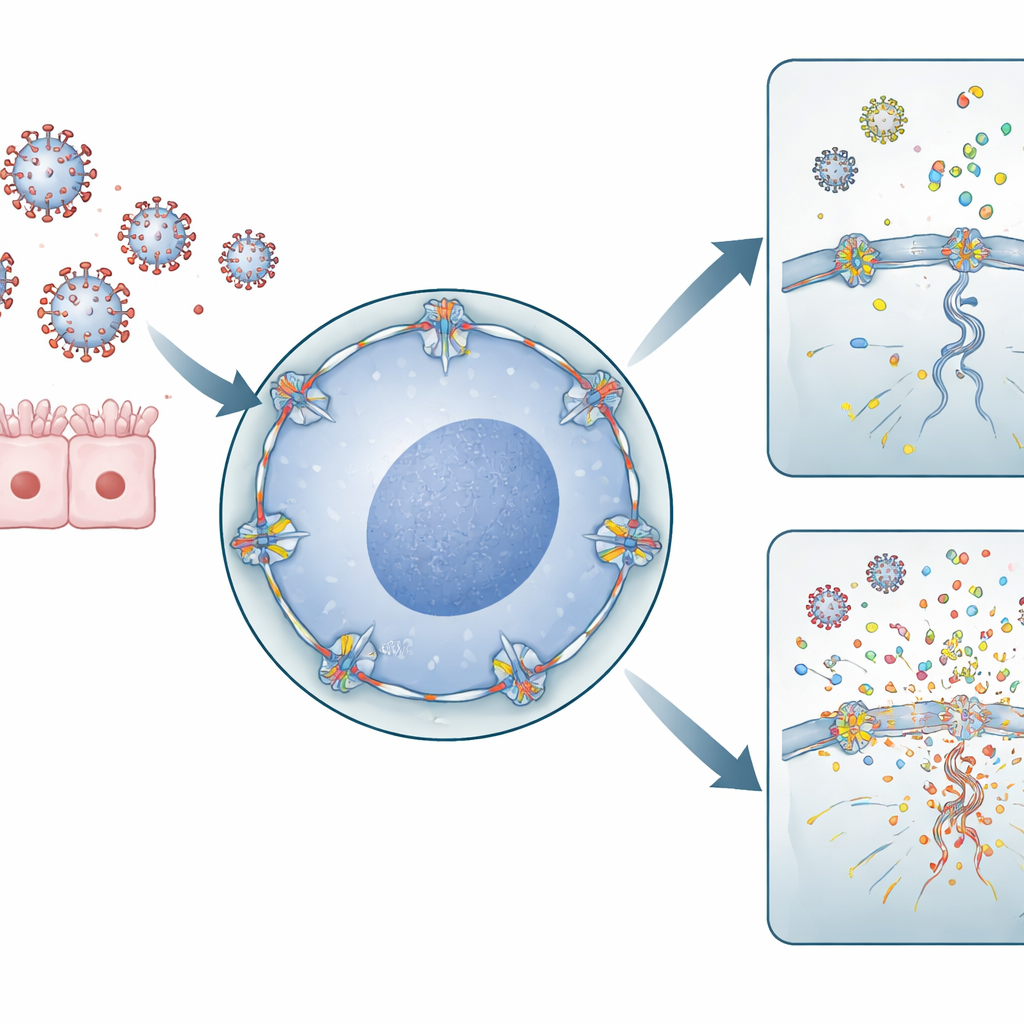
Le virus de la grippe A a un mode de vie inhabituel pour un virus à ARN : il doit pénétrer dans le noyau de la cellule pour copier son matériel génétique. Pour ce faire, il passe par les pores nucléaires — de grandes portes dans l’enveloppe nucléaire qui contrôlent le trafic entre le noyau et le cytoplasme environnant. RANBP2 est un composant majeur du côté externe de ces pores. Les auteurs ont utilisé des cellules dérivées du poumon humain et des cellules immunitaires pour réduire les niveaux de RANBP2 ou introduire la mutation liée à l’ENA. Ils ont constaté que lorsque RANBP2 était absent ou déplacé, les génomes grippaux étaient copiés de manière plus importante à l’intérieur du noyau, et les segments génétiques viraux étaient exportés vers le cytoplasme de façon déséquilibrée. De manière surprenante, cet excès d’ARN viral ne produisait pas davantage de particules virales infectieuses, mais modifiait l’endroit et la manière dont le matériel viral s’accumulait à l’intérieur de la cellule.
Quand les débris viraux nourrissent le système d’alarme
Le système immunitaire s’appuie sur des capteurs moléculaires qui détectent les fragments d’ARN viral errants dans le cytoplasme comme des signaux de danger. L’équipe a montré que, dans les cellules dépourvues de RANBP2 normal, des segments viraux supplémentaires s’accumulaient dans le cytoplasme, créant exactement les motifs que ces capteurs sont conçus pour reconnaître. Dans les cellules dérivées du poumon, cela a déclenché des niveaux plus élevés de molécules inflammatoires telles que IL‑6 et IL‑1β. Dans des macrophages humains primaires — cellules immunitaires de première ligne issues de donneurs sanguins — la perte de RANBP2 a entraîné une forte hausse des chimiokines pro‑inflammatoires, notamment CXCL8, CXCL10, CCL2, CCL3 et CCL4. Ces messagers chimiques recrutent et activent d’autres cellules immunitaires, amplifiant la réaction globale à l’infection.
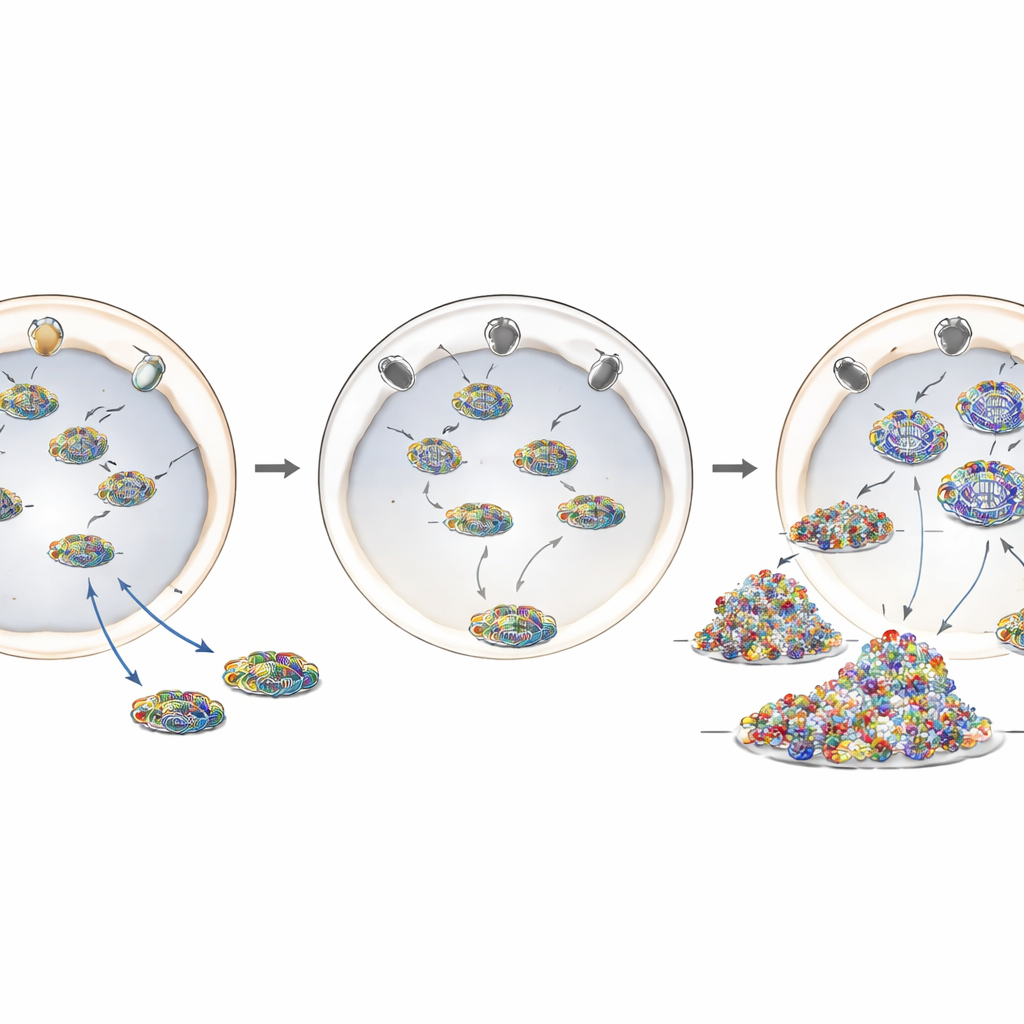
Une mutation de la maladie qui déplace un gardien
Pour modéliser plus fidèlement l’ENA1, les chercheurs ont utilisé l’édition génomique CRISPR‑Cas9 pour introduire la modification la plus courante associée à la maladie, T585M, dans le gène RANBP2 humain. Dans ces cellules éditées, les niveaux de protéine RANBP2 étaient globalement normaux, mais sa localisation ne l’était pas : au lieu de former un halo lumineux autour de l’enveloppe nucléaire, une grande partie de la protéine était déplacée à l’intérieur de la cellule. Les cellules portant cette mutation, qu’elle soit présente sur une ou deux copies du gène, se comportaient de manière très similaire aux cellules appauvries en RANBP2. Elles permettaient une réplication accrue du génome de la grippe, présentaient davantage de matériel viral dans le cytoplasme et déclenchaient une réponse inflammatoire plus forte après l’infection. Cela suggère que le positionnement correct de RANBP2 aux pores nucléaires — plutôt que son abondance globale — est crucial pour son rôle protecteur.
Pourquoi cela compte pour les enfants à risque
Pris ensemble, ces résultats dessinent RANBP2 comme un gardien cellulaire qui ajuste finement la façon dont le matériel génétique grippal entre et sort du noyau. Lorsque RANBP2 est absent ou mal localisé, l’ARN viral est sur‑répliqué et exporté de manière chaotique, encombrant le cytoplasme de débris moléculaires qui intensifient considérablement la signalisation immunitaire. Pour la plupart des tissus, cela peut se traduire par un épisode grippal plus sévère mais surmontable. Chez les enfants vulnérables atteints d’ENA1, cependant, une telle inflammation incontrôlée — surtout si elle atteint le cerveau — peut aider à expliquer les lésions neurologiques soudaines et graves observées après des infections autrement ordinaires. Comprendre cette voie pourrait orienter des stratégies futures pour identifier tôt les patients à risque et adapter des traitements anti‑inflammatoires avant que la réponse immunitaire ne passe du protecteur au destructeur.
Citation: Desgraupes, S., Decorsière, A., Perrin, S. et al. The genetic driver of Acute Necrotizing Encephalopathy, RANBP2, regulates the inflammatory response to Influenza A virus infection. Nat Commun 17, 2427 (2026). https://doi.org/10.1038/s41467-026-69288-1
Mots-clés: grippe, encéphalopathie nécrosante aiguë, RANBP2, hyperinflammation, pore nucléaire