Clear Sky Science · fr
La classe II du CMH agit comme récepteur d’entrée spécifique de l’hôte pour des virus représentatifs de la grippe A H3N2 humains et porcins
Pourquoi cette étude sur la grippe est importante
La grippe saisonnière semble familière, mais le virus qui la cause cherche en permanence de nouvelles façons d’infecter nos cellules et de franchir les barrières d’espèces. Cette étude révèle qu’un sous-type courant de la grippe, H3N2, peut utiliser non seulement sa porte d’entrée classique dans les cellules, mais aussi une seconde porte inattendue qui diffère entre les humains et les porcs. Comprendre cette voie d’entrée de secours aide à expliquer comment la grippe s’adapte à de nouveaux hôtes et pourrait améliorer la surveillance et la préparation face à des souches à potentiel pandémique. 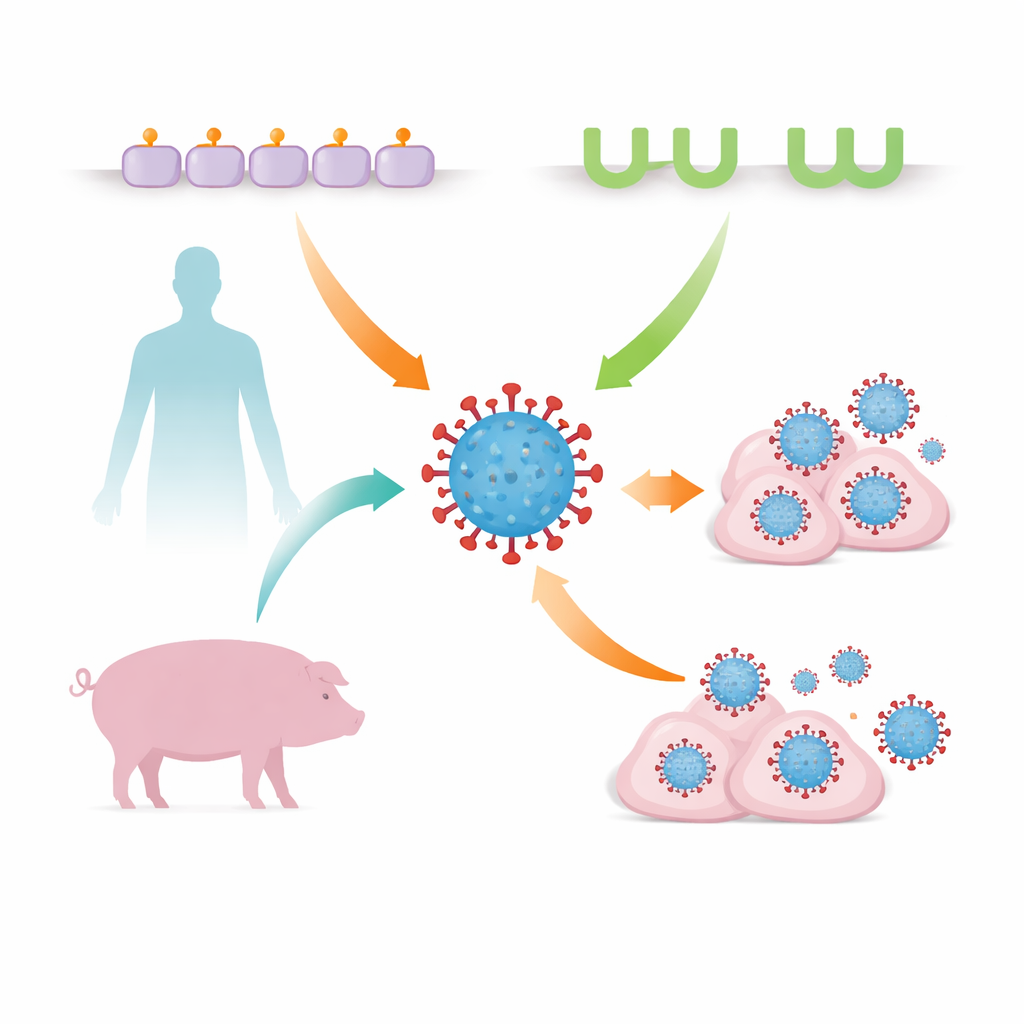
La voie habituelle d’entrée du virus
Depuis des décennies, les scientifiques savent que les virus de la grippe A pénètrent typiquement dans les cellules en s’attachant à des molécules sucrées appelées acides sialiques qui ornent la surface cellulaire. L’« ancre » virale, une protéine appelée hémagglutinine, reconnaît des formes et des liaisons spécifiques de ces sucres, qui diffèrent entre les oiseaux, les humains et d’autres animaux. De petits changements dans l’hémagglutinine peuvent modifier sa préférence pour certains sucres, aidant un virus aviaire à s’adapter aux mammifères. Récemment, toutefois, des virus de chauve-souris et de canard inhabituels ont été découverts qui ignorent complètement les acides sialiques et utilisent à la place une protéine appelée CMH de classe II comme porte d’entrée, suggérant que notre compréhension de l’entrée virale était incomplète.
Une seconde porte apparaît
Le nouveau travail montre que des virus H3N2 plus familiers peuvent aussi utiliser le CMH de classe II comme voie d’entrée alternative, en plus des acides sialiques. Le CMH de classe II aide normalement les cellules immunitaires à présenter des fragments de microbes pour alerter le système immunitaire. L’équipe s’est concentrée sur deux virus étroitement liés construits sur le même arrière-plan génétique : l’un ressemblant à une souche humaine saisonnière H3N2 (hVIC/11) et l’autre adaptée aux porcs (sOH/04). Dans les poumons de porc, le virus adapté aux porcs a été trouvé en association étroite avec des cellules riches en CMH de classe II porcin, en particulier les macrophages alvéolaires — des cellules immunitaires de première ligne dans les sacs d’air pulmonaires — ce qui suggère que cette molécule pourrait servir de poignée que le virus peut saisir.
Désactiver une porte pour tester l’autre
Pour vérifier si le CMH de classe II agit réellement comme un récepteur d’entrée indépendant, les chercheurs ont chimiquement retiré les acides sialiques des macrophages porcins et de lignées cellulaires humaines modifiées. Lorsque seuls les sucres classiques ont été supprimés, les deux virus ont quand même provoqué une certaine infection. Mais lorsque les acides sialiques ont été enlevés et que le CMH de classe II a été simultanément bloqué par des anticorps, l’infection a fortement chuté, en particulier pour le virus adapté aux porcs. Dans des cellules humaines rénales et pulmonaires génétiquement empêchées de produire des acides sialiques, l’ajout de la version humaine du CMH de classe II a permis une infection efficace par le virus de type humain, tandis que l’ajout de la version porcine favorisait le virus porcin. Le traitement des cellules par des médicaments qui empêchent l’acidification des compartiments internes a également bloqué cette infection médiée par le CMH, indiquant qu’une fois à l’intérieur, le virus suit la même voie interne que lors de l’entrée virale classique. 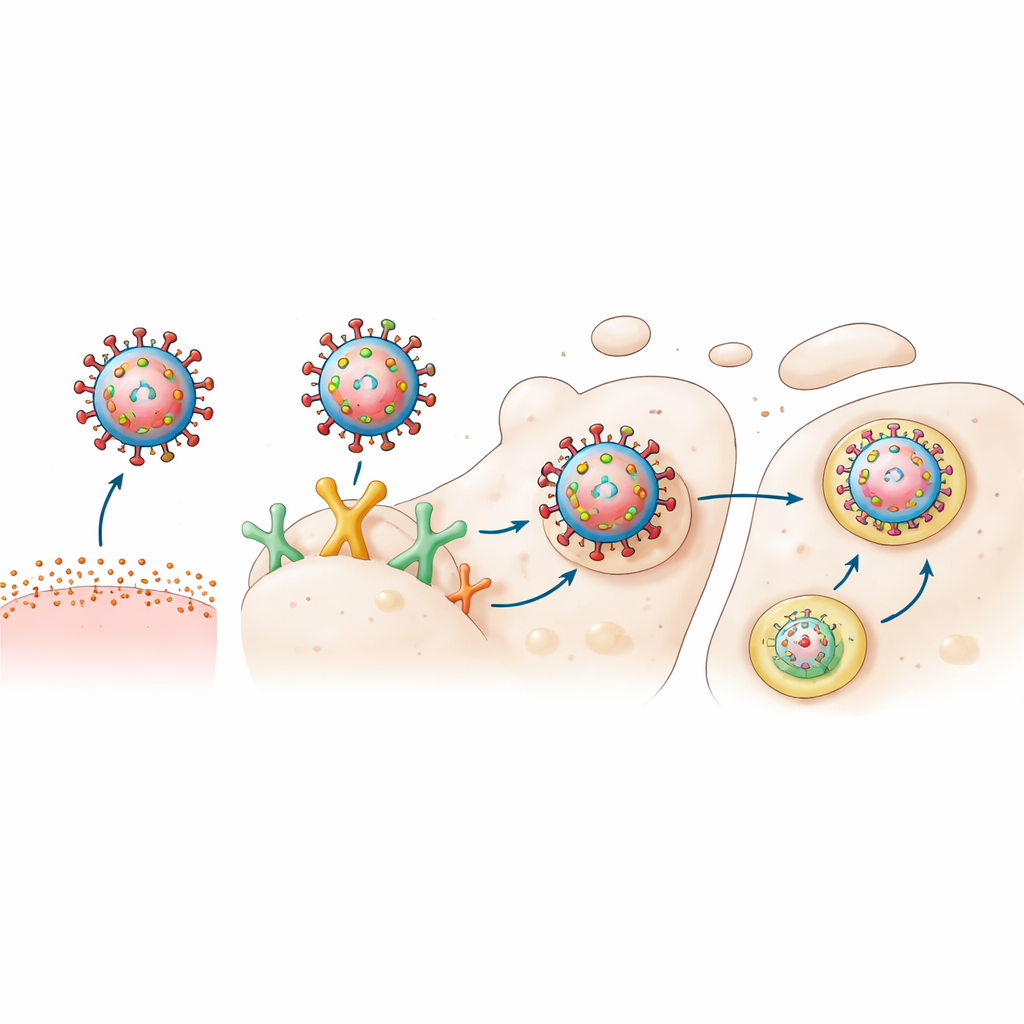
Comment de petits changements aident le virus à changer d’hôte
Les auteurs se sont ensuite demandé quelles parties de l’hémagglutinine virale contrôlent ce nouveau type de liaison. Des travaux antérieurs avaient montré que lorsqu’un virus H3N2 humain passe par les porcs, il acquiert souvent certains changements d’une seule lettre proches, mais pas directement à l’intérieur, de la poche de liaison aux acides sialiques. Des virus portant l’un quelconque de ces trois changements (aux positions désignées 138, 186 ou 193 dans la protéine) ont été testés. Ces virus mutants pouvaient utiliser à la fois le CMH de classe II humain et porcin pour pénétrer dans des cellules dépourvues d’acides sialiques, et dans certains essais ils ont même préféré la version porcine. Parallèlement, ces mêmes mutations modifiaient la force d’affinité des virus pour des acides sialiques de type humain ou aviaire. En d’autres termes, des ajustements proches du site de liaison aux sucres habituel peuvent régler à la fois le récepteur classique et le nouveau récepteur, offrant au virus de la flexibilité lors de son adaptation à une nouvelle espèce.
Ce que cela signifie pour la grippe et les menaces futures
Pris ensemble, ces résultats montrent que les virus H3N2 courants ne sont pas limités à un seul type de « poignée » à la surface cellulaire : ils peuvent utiliser à la fois les acides sialiques et le CMH de classe II, et ce de manière reflétant l’aptitude du virus aux humains ou aux porcs. Lors des premières étapes d’adaptation à un nouvel hôte, un virus peut temporairement engager le CMH de classe II des deux espèces, élargissant ainsi sa gamme de cibles et facilitant son implantation. Parce que le CMH de classe II est abondant sur des cellules immunitaires clés dans le poumon, cette voie alternative peut permettre à la grippe d’attaquer sélectivement des cellules censées nous défendre, favorisant potentiellement la propagation virale et la maladie. Reconnaître le CMH de classe II comme récepteur d’entrée spécifique de l’hôte ajoute une pièce importante au puzzle de la façon dont la grippe franchit les barrières d’espèces et souligne la nécessité de surveiller non seulement la liaison aux sucres mais aussi les récepteurs protéiques lors de l’évaluation du risque pandémique des souches émergentes.
Citation: Cardenas, M., Compton, S., Caceres, C.J. et al. MHC class II functions as a host-specific entry receptor for representative human and swine H3N2 influenza A viruses. Nat Commun 17, 2560 (2026). https://doi.org/10.1038/s41467-026-69267-6
Mots-clés: influenza A H3N2, récepteurs d’entrée virale, CMH de classe II, adaptation à l’hôte, transmission zoonotique