Clear Sky Science · fr
Assemblage asymétrique de 4‑alkyl‑butenolide catalysé par une flavoenzyme trifonctionnelle dans la biosynthèse de l’avenolide
Pourquoi de petits cycles bactériens nous concernent
De nombreux médicaments qui sauvent des vies, des antiparasitaires aux agents de protection des cultures, reposent sur un petit motif chimique appelé butenolide. Aujourd’hui, ces cycles sont majoritairement synthétisés à partir de matières premières pétrolières via des procédés industriels en plusieurs étapes qui consomment de l’énergie et génèrent des déchets. Cette étude révèle comment des bactéries du sol construisent l’un de ces cycles, une hormone nommée avenolide qui active la production des puissants antiparasitaires appelés avermectines. Comprendre cette voie naturelle ouvre la voie à des méthodes plus propres et moins coûteuses pour fabriquer des produits utiles et pourrait aider à découvrir de nouveaux antibiotiques.
Le cycle particulier au cœur de nombreux médicaments
Les butenolides sont des cycles compacts à cinq atomes que les chimistes apprécient parce qu’ils réagissent de façon polyvalente et figurent dans de nombreux produits naturels et médicaments contemporains. Ils contribuent à façonner des molécules aux activités anticancéreuses, antifongiques, anti‑inflammatoires et insecticides utilisées en médecine et en agriculture. Pourtant, les voies de synthèse traditionnelles de ces cycles exigent généralement plusieurs étapes soigneusement contrôlées, des catalyseurs coûteux et des matières premières pétrochimiques. Cette combinaison augmente les coûts et l’impact environnemental, poussant les chercheurs à chercher des raccourcis biologiques que la nature a déjà perfectionnés.
Une hormone bactérienne qui déclenche un médicament phare
Chez la bactérie du sol Streptomyces avermitilis, la molécule contenant un butenolide appelée avenolide agit comme une petite hormone. À des concentrations extrêmement faibles, elle se lie à une protéine régulatrice et lève le frein moléculaire sur les gènes qui produisent les avermectines, des agents puissants qui paralysent les vers parasites et certains insectes. Des travaux génétiques antérieurs avaient laissé entendre que deux enzymes, nommées SavA et SavB, construisaient l’avenolide, mais les étapes réelles restaient inconnues. L’équipe a d’abord transféré les gènes concernés dans un parent plus coopératif, Streptomyces albidoflavus, et optimisé les conditions de culture jusqu’à ce que la souche modifiée produise des quantités milligrammiques d’avenolide pur — suffisamment pour disséquer la voie en détail. 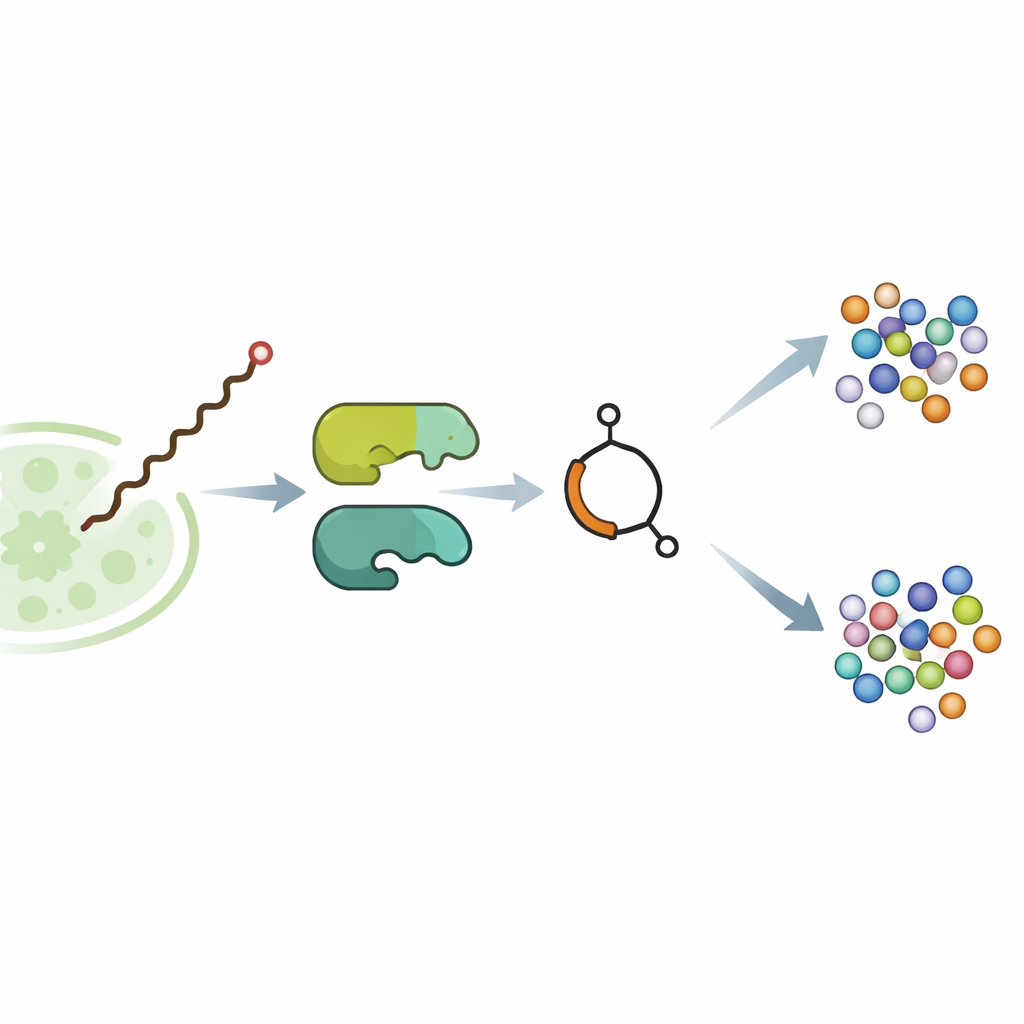
Une seule enzyme qui fait trois travaux à la suite
La surprise centrale de l’étude est SavA, une enzyme contenant un flavine qui réalise trois transformations chimiques distinctes sur un fragment de départ apparenté à un acide gras prélevé du métabolisme cellulaire normal. En travaillant en réactions test‑tube avec des substrats mimétiques soigneusement synthétisés, les chercheurs ont montré que SavA enlève d’abord des atomes d’hydrogène pour introduire une double liaison, puis ajoute un groupe oxygéné en une position spécifique, et enfin favorise la fermeture de la chaîne en un cycle butenolide. Des expériences d’isotopie utilisant de l’oxygène gazeux enrichi ont confirmé que l’oxygène du cycle provient directement de l’air. La modélisation structurale et des mutations ciblées ont identifié un acide aminé unique comme la base qui déclenche la réaction, et ont révélé comment le cofacteur flavine lié bascule entre formes oxydées et réduites sans jamais être consommé.
Une enzyme finale qui affine la chaîne latérale
Une fois que SavA a construit l’échafaudage butenolide chiral, SavB — une enzyme cytochrome P450 — prend le relais pour décorer la chaîne carbonée attachée. En présence de ses partenaires rédox et d’un cofacteur cellulaire courant, SavB effectue une série précise d’oxydations sur deux atomes de carbone adjacents. Une analyse résolue dans le temps a mis au jour deux molécules intermédiaires : d’abord un produit mono‑hydroxylé, puis une forme cétone, avant l’apparition de l’avenolide pleinement fonctionnel. Des mesures par résonance magnétique nucléaire ont confirmé les positions et l’arrangement tridimensionnel de ces nouveaux groupes. Le travail montre que SavB introduit ces atomes d’oxygène dans un ordre défini et avec un contrôle strict de l’orientation, caractéristique importante pour l’activité biologique de l’hormone. 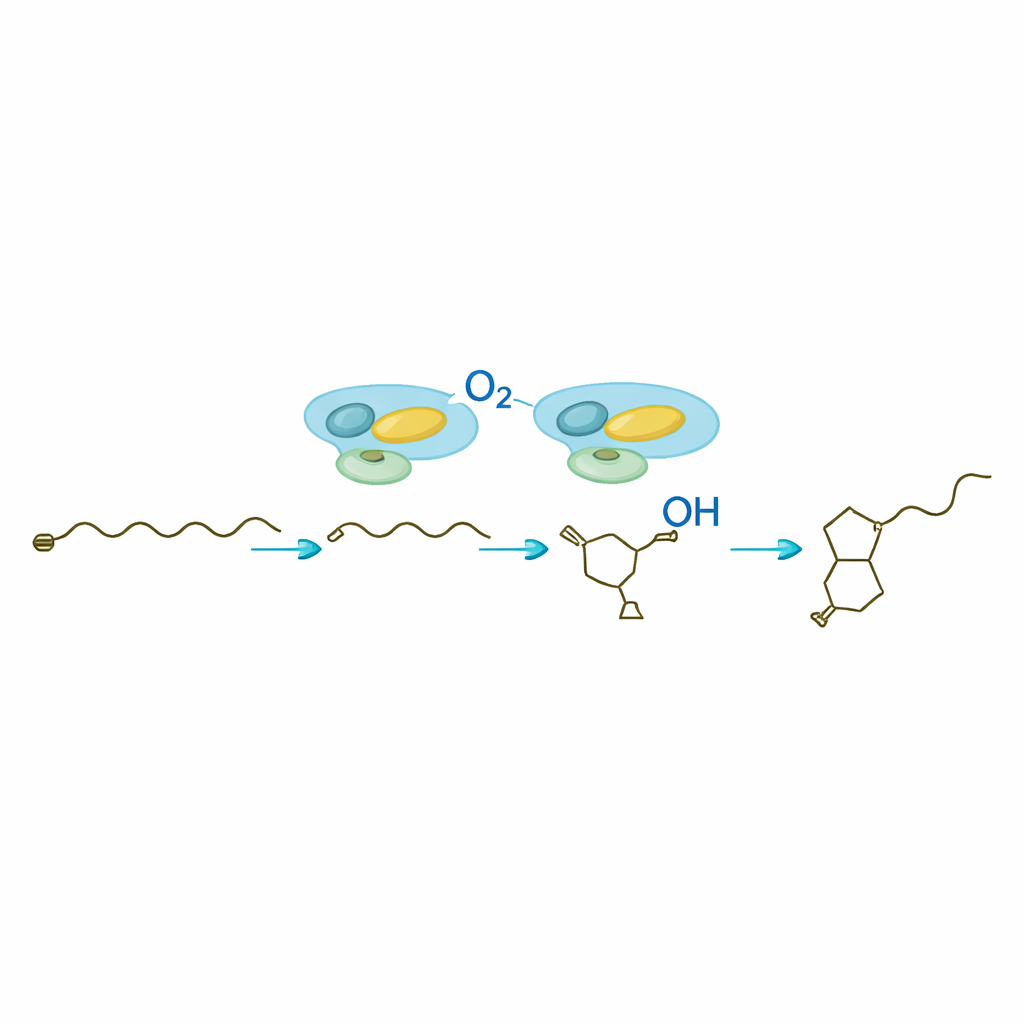
Leçons de chimie verte tirées d’enzymes bactériennes
Ensemble, SavA et SavB convertissent un bloc de construction dérivé d’un acide gras ordinaire en une molécule de signalisation finement réglée en n’utilisant que l’oxygène de l’air et des aides cellulaires standards. Contrairement à de nombreux procédés industriels, SavA n’a pas besoin d’agents réducteurs supplémentaires ni de réactifs sacrificiels ; son cofacteur flavine se contente de transférer des électrons pendant que le substrat lui‑même fournit la force motrice. Les auteurs soulignent SavA comme un nouveau type de flavoenzyme multi‑talent avec un fort potentiel en tant que biocatalyseur pour la fabrication durable de butenolides et de motifs apparentés. En termes pratiques, exploiter ou modifier de telles enzymes pourrait un jour permettre à des usines — ou à des microbes ingénierés — de produire des fragments de médicaments et des produits agrochimiques importants à partir de matières premières renouvelables sous des conditions douces, réduisant à la fois les coûts et l’empreinte environnementale.
Citation: Li, W., Zhao, J., Zeng, W. et al. Trifunctional flavoenzyme-catalyzed asymmetric 4-alkyl-butenolide assembly in avenolide biosynthesis. Nat Commun 17, 2459 (2026). https://doi.org/10.1038/s41467-026-69265-8
Mots-clés: biosynthèse de butenolide, flavoenzyme SavA, hormone avenolide, biocatalyse, signalisation Streptomyces