Clear Sky Science · fr
Les dégradeurs de la protéine de capside du virus de la dengue présentent une pharmacologie différenciée par rapport aux inhibiteurs de la capside
Retourner la coquille du virus contre lui-même
La dengue infecte des centaines de millions de personnes chaque année, et pourtant les médecins disposent toujours de peu d'antiviraux fiables pour la traiter. Cette étude explore une approche nouvelle pour neutraliser le virus de la dengue en détruisant l’un de ses éléments essentiels à l’intérieur des cellules infectées, plutôt que de se contenter d’en bloquer l’activité. Les travaux montrent que des molécules soigneusement conçues peuvent marquer une protéine virale clé pour qu’elle soit éliminée par le système de gestion des déchets de la cellule, réduisant ainsi la production virale et affaiblissant la capacité du virus à se cacher des défenses immunitaires.
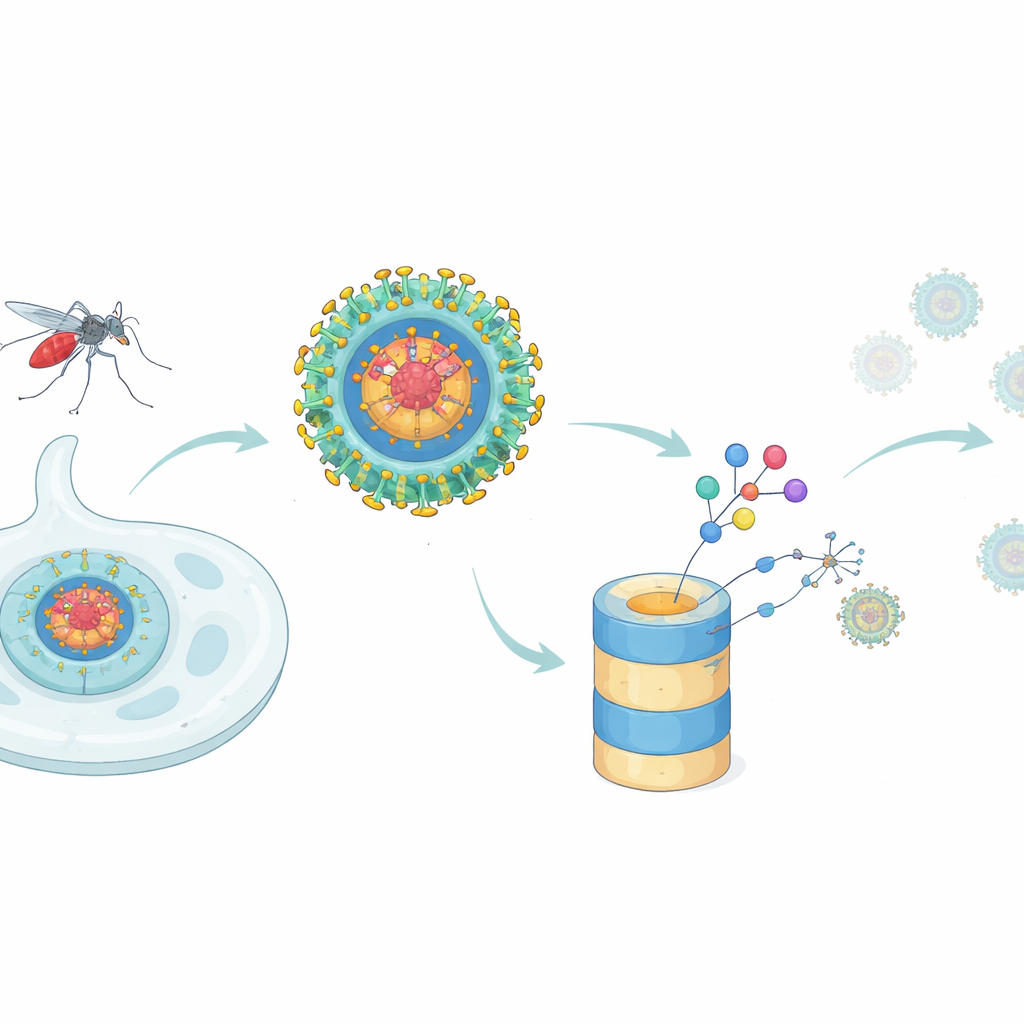
Une nouvelle tactique pour arrêter la dengue
La plupart des antiviraux agissent comme des bouchons dans une machine : ils se fixent sur un site fonctionnel d’une protéine virale et tentent de le bloquer. Cette stratégie est mise à l’épreuve quand une seule protéine virale accomplit de nombreuses tâches, ou quand de petites mutations affaiblissent l’affinité du médicament. La protéine de la capside de la dengue en est un bon exemple. Elle forme la coque centrale qui empaquette le génome viral dans de nouveaux particules, mais elle interfère aussi avec la cellule hôte en interagissant avec de nombreuses protéines humaines et en atténuant la réponse par interféron de l’organisme, un signal antiviral de première ligne. Les auteurs se sont demandé si un concept plus récent — la dégradation ciblée des protéines — pouvait dépasser les inhibiteurs classiques en éliminant effectivement la protéine de capside des cellules infectées.
Concevoir un « chasseur de primes » moléculaire
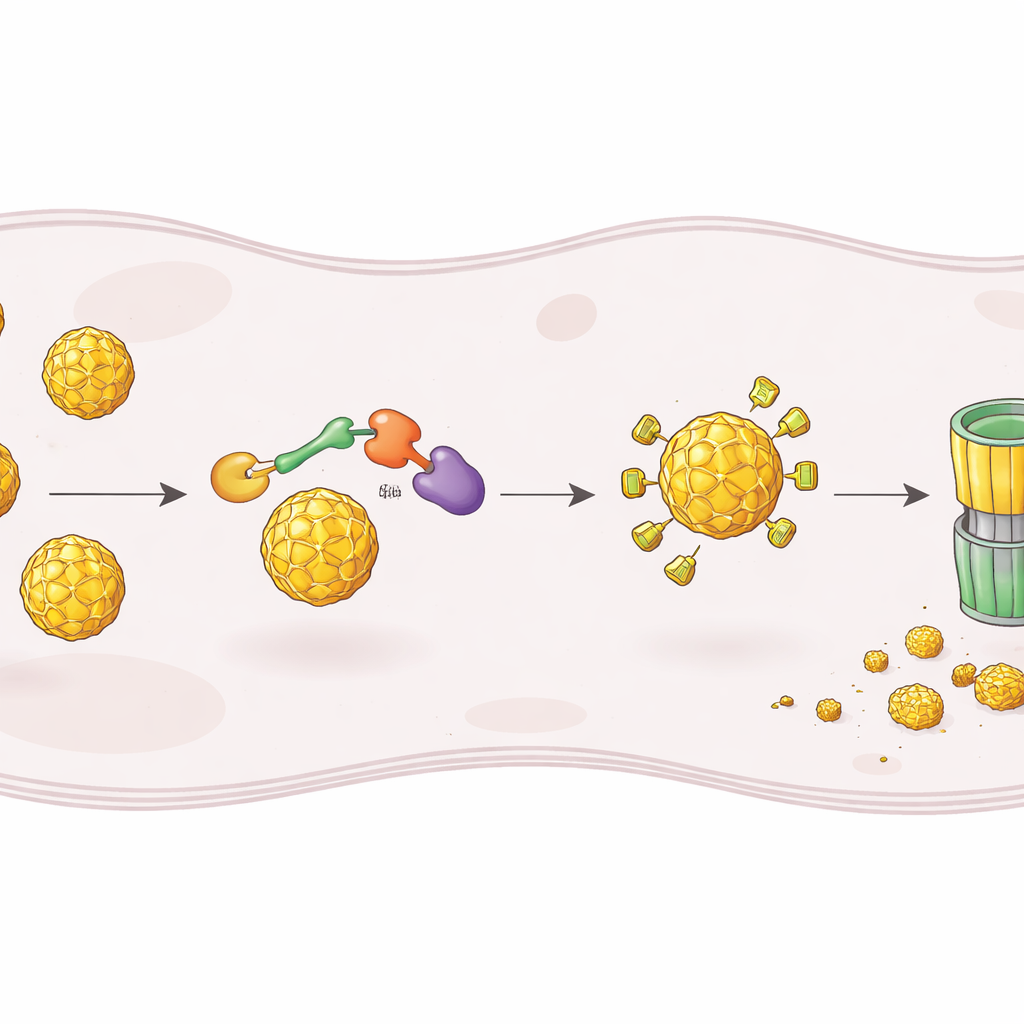
Pour construire un tel dégradeur, les chercheurs sont partis de ST148, une petite molécule connue pour se lier à la capside de la dengue et perturber l’assemblage de nouvelles particules virales. Ils ont relié chimiquement ST148 à un second module qui recrute un complexe enzymatique humain responsable du marquage des protéines en vue de leur destruction. Les molécules chimériques obtenues, appelées PROTACs, sont conçues pour attraper la capside d’un côté et un ligase E3 de l’autre, les rapprochant de sorte que la capside soit marquée par l’ubiquitine et dirigée vers le protéasome de la cellule, le principal broyeur de protéines. En testant de nombreuses longueurs de liaisons et différents groupes recruteurs de ligases, ils ont identifié un composé remarquable, nommé RPG‑01‑132, qui réduisait de manière fiable les niveaux de capside dans les cellules infectées, de façon dépendante de la forme CRBN de la ligase et du bon fonctionnement du protéasome.
Arrêter la production virale et l’évasion immunitaire
Une fois le dégradeur opérationnel, l’équipe a évalué son effet sur l’infection par la dengue. Dans des cellules d’origine hépatique infectées par le virus de la dengue, RPG‑01‑132 provoquait une forte baisse du nombre de virus infectieux libérés, à des concentrations où il ne diminuait que partiellement les niveaux totaux de capside. Fait important, les autres protéines virales et l’ARN viral restaient inchangés, montrant que le composé n’empoisonnait pas simplement la réplication globale mais agissait spécifiquement via la perte de la capside. La microscopie électronique apportait une lecture visuelle : les cellules traitées par l’inhibiteur initial ST148 accumulaient des empilements de particules virales partiellement formées dans le réticulum endoplasmique, cohérent avec un blocage de l’assemblage, tandis que les cellules traitées par le dégradeur montraient presque aucune particule virale visible. Le dégradeur a également atténué la capacité de la capside à supprimer la signalisation de l’interféron‑β dans un système rapporteur, suggérant que le rôle non‑structural de la capside dans la neutralisation de l’immunité innée peut être inversé en la dégradant.
Contrecarrer la diversité virale et la résistance aux médicaments
Le virus de la dengue existe en quatre sérotypes majeurs qui diffèrent quant à leur sensibilité aux inhibiteurs ciblant la capside, et la résistance peut apparaître par une seule mutation. Les auteurs ont comparé le dégradeur à ST148 sur des souches représentatives des quatre sérotypes et contre un virus portant une mutation (S34L dans la capside) précédemment montrée comme rendant ST148 inefficace. Comme prévu, ST148 fonctionnait mieux sur un sérotype et perdait son activité contre le mutant résistant. RPG‑01‑132, en revanche, affichait une puissance antivirale similaire sur tous les sérotypes et conservait son activité contre le mutant S34L, tout en agissant via la même voie de dégradation dépendante de CRBN. Cela illustre un avantage clé de la pharmacologie « pilotée par l’événement » : le dégradeur n’a pas besoin de rester fortement lié à chaque molécule de capside en permanence, pourvu qu’il déclenche suffisamment d’événements de dégradation pour faire pencher la balance.
Ce que cela signifie pour les futurs traitements de la dengue
Cette étude démontre que la protéine de la capside de la dengue peut être visée non seulement en tant que composant structurel du virus, mais aussi en tant que carrefour amovible qui soutient plusieurs étapes de l’infection et l’évasion immunitaire. En convertissant un inhibiteur traditionnel en dégradeur, les chercheurs ont créé un composé qui bloque la production virale, soulève une partie de la suppression de l’immunité innée par le virus, et reste efficace à travers des souches virales diverses et une mutation de résistance connue. RPG‑01‑132 lui‑même nécessitera des optimisations — meilleure pénétration cellulaire, activité renforcée dans des modèles animaux et contrôles de sécurité approfondis — mais il fournit une preuve de concept convaincante. Plus généralement, ce travail suggère que détourner la machinerie de recyclage de la cellule pourrait ouvrir de nouvelles voies pour des antiviraux plus difficiles à contourner par les virus et capables de neutraliser des protéines ayant de multiples rôles au sein des cellules infectées.
Citation: Chakravarty, A., Wang, LN., Golden, R.P. et al. Degraders of the dengue virus capsid protein exhibit differentiated pharmacology relative to capsid inhibitors. Nat Commun 17, 2594 (2026). https://doi.org/10.1038/s41467-026-69263-w
Mots-clés: virus de la dengue, protéine de la capside, dégradation ciblée des protéines, conception de médicaments antiviraux, PROTACs