Clear Sky Science · fr
Cibler la NHEJ active la signalisation STING via la dégradation de MYC pour renforcer l’immunité antitumorale dans le CCPP
Pourquoi cette recherche est importante
Le cancer du poumon à petites cellules est l’un des cancers les plus meurtriers, la plupart des patients vivant moins d’un an après le diagnostic. De façon frappante, ces tumeurs présentent de nombreuses mutations de l’ADN qui devraient en faire des cibles faciles pour le système immunitaire, pourtant elles répondent mal aux immunothérapies modernes. Cette étude met au jour un frein moléculaire caché qui empêche le système immunitaire de reconnaître ces tumeurs et montre comment l’inactivation d’une protéine clé de la réparation de l’ADN peut transformer ces cancers, de « froids » en « chauds », permettant aux traitements existants d’être beaucoup plus efficaces.
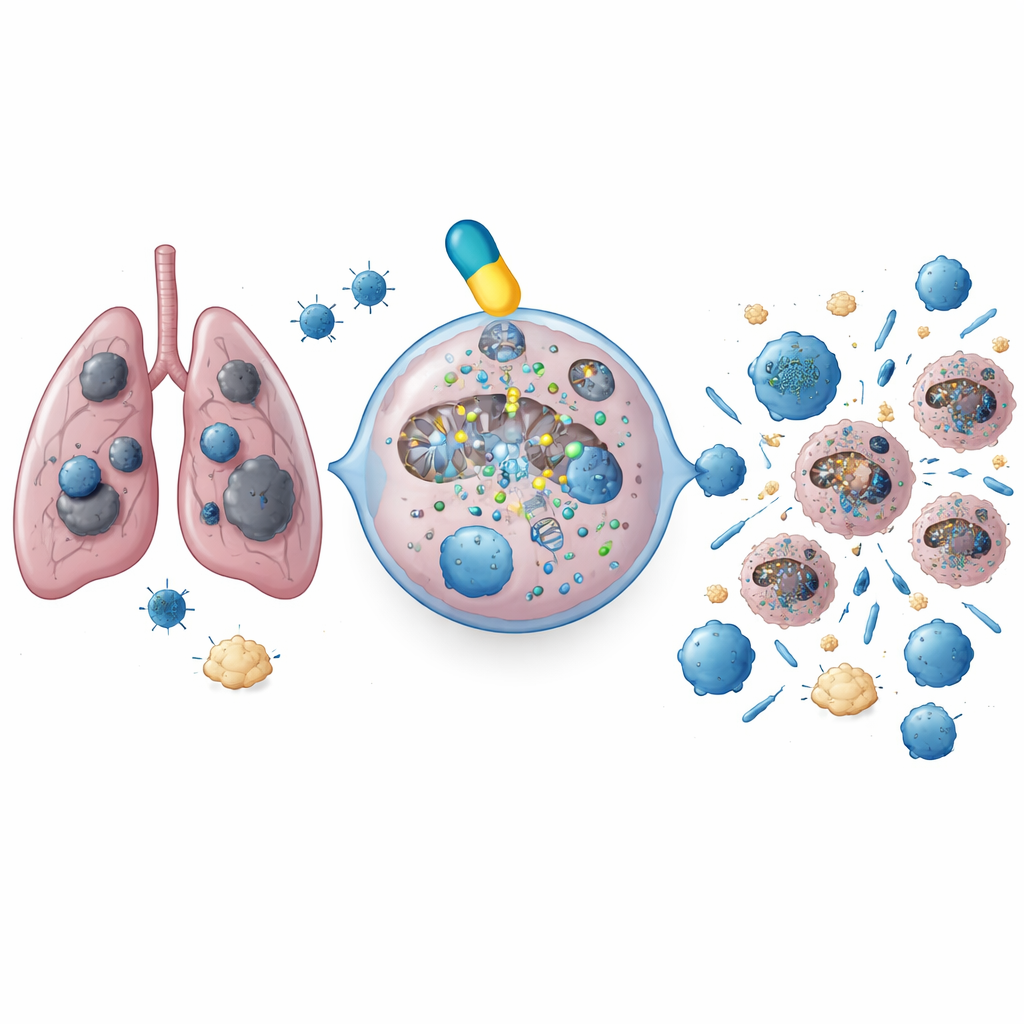
Un interrupteur de réparation caché dans les tumeurs pulmonaires
Les chercheurs ont commencé par examiner des données génétiques provenant de plus de 179 000 tumeurs humaines couvrant 24 types de cancer. Ils se sont concentrés sur une voie de réparation de l’ADN appelée jonction d’extrémités non homologues (NHEJ), qui répare des cassures dangereuses des brins d’ADN. Un contrôleur central de cette voie, une protéine appelée DNAPKcs (codée par le gène PRKDC), s’est révélée anormalement élevée dans le cancer du poumon à petites cellules. Parmi des milliers d’échantillons de tumeurs pulmonaires, les cas de petites cellules montraient l’activité la plus forte de cet interrupteur de réparation. Les patients dont les tumeurs présentaient des niveaux élevés de PRKDC vivaient moins longtemps et bénéficiaient moins des chimiothérapies standard et des inhibiteurs de points de contrôle immunitaire, ce qui suggère que DNAPKcs aide les tumeurs à survivre tant aux dommages de l’ADN qu’à l’attaque immunitaire.
Des dommages à l’ADN à une alarme interne
Pour voir ce qui se passe lorsque cet interrupteur de réparation est désactivé, l’équipe a utilisé des médicaments et des outils d’invalidation génétique pour bloquer DNAPKcs dans des panels de cellules de cancer du poumon à petites cellules et dans des modèles tumoraux murins. Dans de nombreux modèles, en particulier ceux ressemblant à des sous-types humains à forte activité de l’oncogène MYC, les inhibiteurs de DNAPKcs ont fortement réduit la croissance des cellules tumorales et ont même fait régresser des tumeurs dérivées de patients chez la souris. Au niveau cellulaire, le blocage de DNAPKcs entraînait une accumulation d’ADN cassé, visible sous forme de ponctuations d’un marqueur de dommage dans le noyau et de minuscules corps supplémentaires remplis d’ADN appelés micronoyaux. Ces fragments d’ADN s’écoulaient dans le cytoplasme de la cellule, où ils pouvaient être perçus comme des signaux de danger.
Activation du système d’alarme « viral » de la cellule
De l’ADN libre au mauvais endroit est normalement un signe d’infection virale. Les cellules le détectent via un senseur appelé cGAS, qui déclenche une voie d’alarme en aval nommée STING. Les auteurs montrent qu’après inhibition de DNAPKcs, cGAS se regroupe sur les micronoyaux, STING s’active et une cascade de molécules stimulant l’immunité est déclenchée. Les cellules produisent davantage d’interférons de type I et II et de chimiokines qui attirent les cellules immunitaires. L’expression à la surface de protéines « drapeau » clés (molécules du CMH de classe I), qui aident les cellules immunitaires à reconnaître les antigènes tumoraux, augmente également. Lorsque la voie STING est bloquée chimiquement ou neutralisée génétiquement, ces changements disparaissent en grande partie et les effets antitumoraux de l’inhibition de DNAPKcs sont beaucoup plus faibles, ce qui souligne que ce système d’alarme interne est essentiel à la réponse.
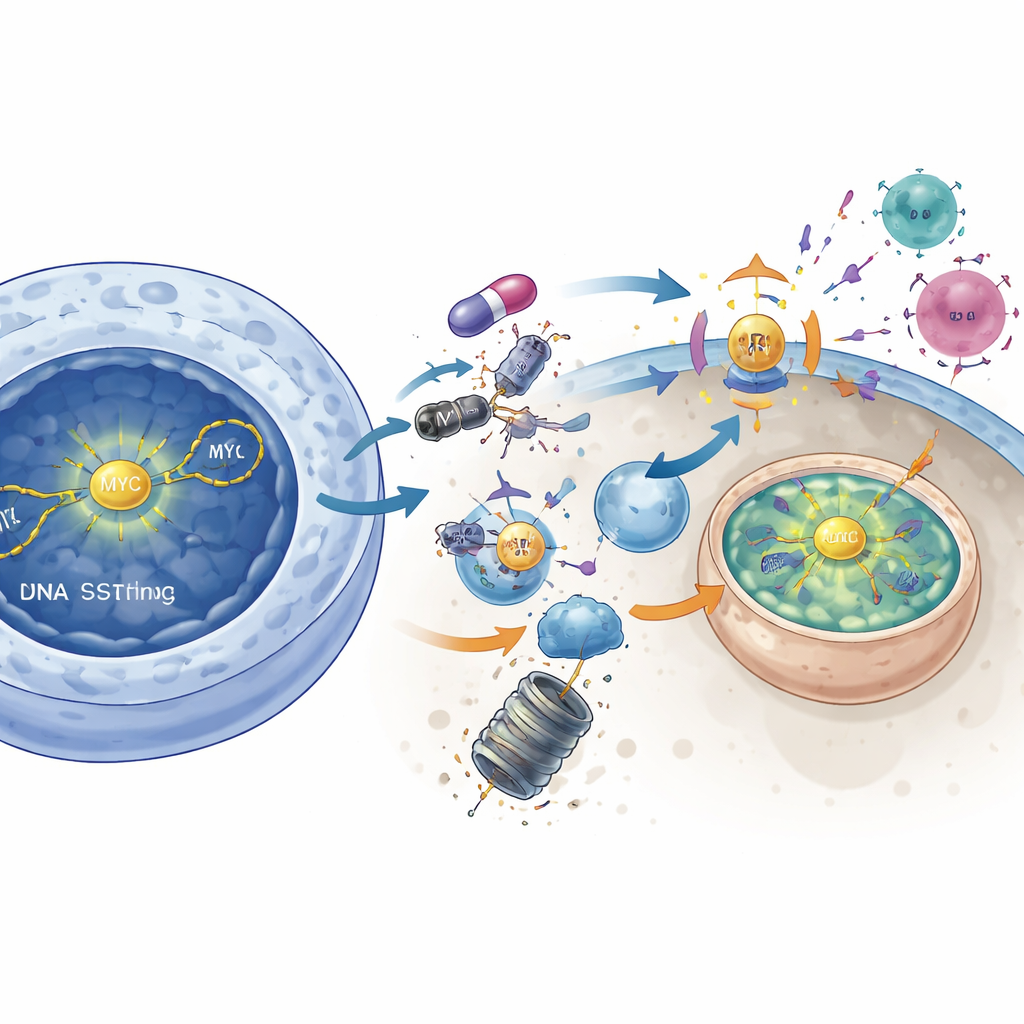
Désarmer MYC pour démasquer la tumeur
L’étude relie en outre DNAPKcs au puissant moteur de croissance MYC, une protéine longtemps considérée comme « non ciblable ». Dans les tumeurs à forte activité de MYC, l’inhibition de DNAPKcs réduit la signalisation AKT active et libère un frein moléculaire sur une autre enzyme, GSK3β. Une fois activée, GSK3β étiquette MYC pour sa destruction, entraînant une chute des niveaux de protéine MYC. La réduction directe de MYC par des outils génétiques reproduisait nombre des effets activateurs de l’immunité observés après blocage de DNAPKcs : la signalisation STING augmentait, les gènes d’interféron s’allumaient et le CMH de classe I augmentait. À l’inverse, forcer une surexpression de MYC effaçait en grande partie l’effet d’activation immunitaire de l’inhibiteur de DNAPKcs. Cela suggère que DNAPKcs stabilise normalement MYC, et que pousser MYC vers la dégradation est une étape clé pour réveiller l’immunité antitumorale.
De tumeurs « froides » à « chaudes » dans des modèles vivants
Dans des modèles murins immunocompétents qui ressemblent étroitement au cancer du poumon à petites cellules humain, le traitement par un inhibiteur de DNAPKcs seul a ralenti ou réduit significativement les tumeurs. De manière importante, la combinaison de l’inhibiteur avec un médicament anti–PD-L1 existant a transformé des tumeurs précédemment résistantes, entraînant des régressions tumorales spectaculaires et, dans certains cas, une disparition complète. Un profilage immunitaire détaillé a montré que l’inhibition de DNAPKcs augmentait les cellules T CD8 tueuses de cancer, favorisait les macrophages pro-inflammatoires de type M1, réduisait les cellules T suppressives et élevait les niveaux de CMH de classe I dans les tumeurs. L’élimination des cellules T CD8 ou l’inactivation de STING inversait ces bénéfices, confirmant que la thérapie fonctionne en transformant la tumeur en un signal attirant l’attaque immunitaire plutôt qu’en tuant directement les cellules cancéreuses seules.
Ce que cela signifie pour les patients
Ensemble, ces résultats révèlent DNAPKcs comme un coordonnateur central de la réparation de l’ADN et de l’évasion immunitaire dans le cancer du poumon à petites cellules. En bloquant DNAPKcs, les tumeurs accumulent des dommages de l’ADN, MYC est déstabilisé, l’alarme cGAS–STING est déclenchée et les voies d’interféron et de présentation d’antigène sont activées. Cette chaîne d’événements convertit des tumeurs immunologiquement silencieuses en tumeurs répondant fortement au blocage des points de contrôle et à la chimiothérapie dans des modèles précliniques. Bien que des essais cliniques restent nécessaires, le travail suggère que les inhibiteurs de DNAPKcs existants pourraient être associés à l’immunothérapie pour offrir aux patients atteints de ce cancer agressif une meilleure chance de contrôle durable.
Citation: Chakraborty, S., Elliott, A., Sen, U. et al. Targeting NHEJ activates STING signaling through MYC degradation to boost antitumor immunity in SCLC. Nat Commun 17, 2597 (2026). https://doi.org/10.1038/s41467-026-69262-x
Mots-clés: cancer du poumon à petites cellules, inhibition de la réparation de l’ADN, voie STING, dégradation de MYC, immunothérapie tumorale