Clear Sky Science · fr
Activation coopérative d’anions sur un centre cobalt par appariement ionique et conception de ligand
Pourquoi les partenaires minuscules autour des métaux comptent
Les chimistes se concentrent souvent sur le « protagoniste » principal d’une réaction — un atome métallique qui aide à rompre et former des liaisons. Mais cet article montre que les partenaires discrets qui gravitent à proximité, invisibles à l’œil nu, peuvent modifier complètement le rôle du métal. En façonnant soigneusement l’espace autour d’un atome de cobalt, les auteurs révèlent comment deux anions presque interchangeables, souvent considérés comme des figurants passifs en chimie et dans les batteries, peuvent conduire à des résultats très différents. 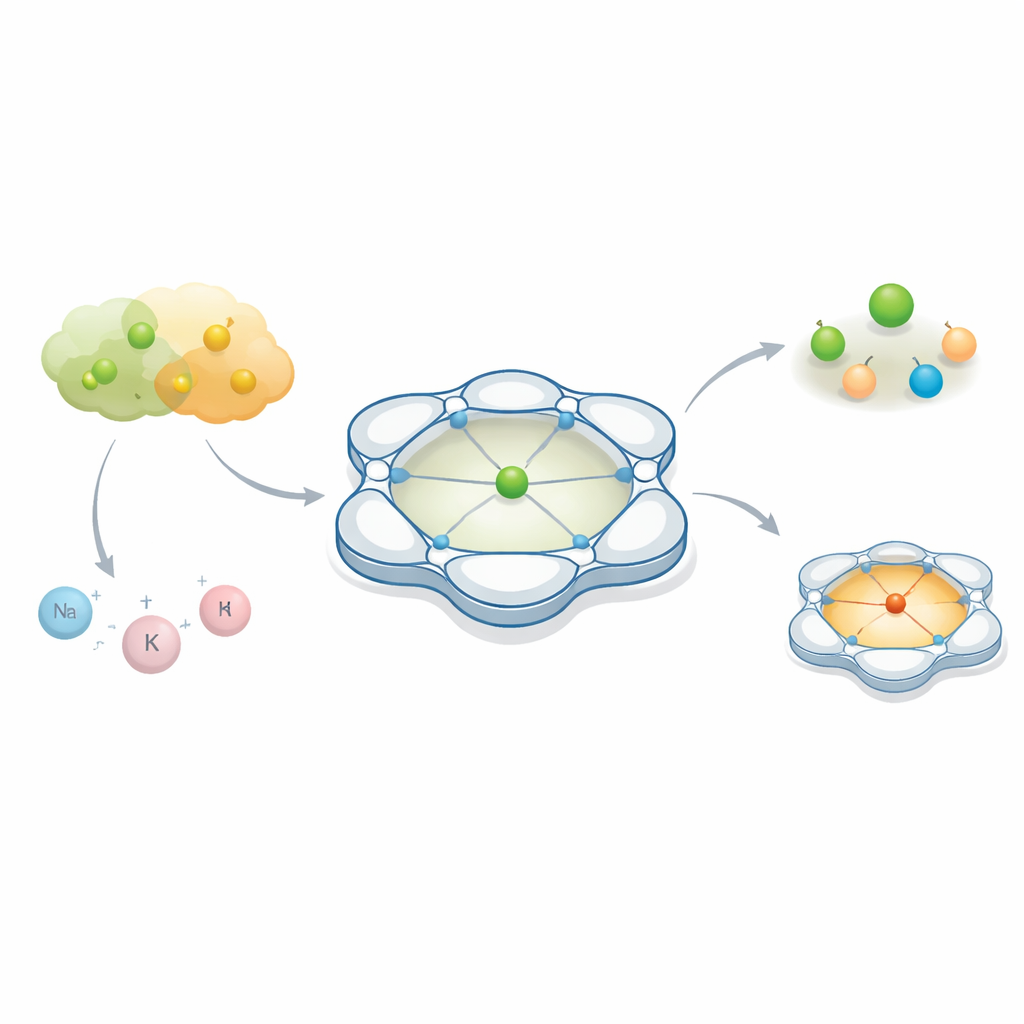
Construire une poche sur mesure autour du cobalt
Les chercheurs ont conçu une structure organique en forme de cage appelée Py4Im qui enveloppe étroitement un ion cobalt. Ce motif est construit à partir de plusieurs cycles pyridine liés et d’une unité imidazolidine, qui ensemble créent une cavité rigide en forme de coupe contenant un seul groupe N–H. Cette petite cavité est « protique », c’est‑à‑dire qu’elle peut former des liaisons hydrogène, et elle pointe dans une direction précise, comme une minuscule baie d’amarrage pour les anions entrants. Lorsque le cobalt est assemblé avec ce ligand, on obtient une famille de complexes chargés positivement dont la forme globale et la poche interne restent identiques tandis que l’anion contre‑ion — le partenaire chargé négativement — peut être échangé. Cela fait du système un banc d’essai idéal pour observer le comportement de différents anions dans le même environnement contrôlé.
Deux anions qui se ressemblent, deux comportements très différents
L’équipe a comparé deux anions couramment utilisés, le tétrafluoroborate (BF4−) et l’hexafluorophosphate (PF6−), souvent qualifiés d’anions faiblement coordonnants. Ils sont prisés parce qu’ils gardent généralement leurs distances avec les centres métalliques, stabilisant des espèces fortement chargées sans s’impliquer directement. De manière surprenante, à l’intérieur de la cavité Py4Im, ils ne se comportent pas de la même façon. Dans des conditions douces, PF6− cède un ion fluorure au cobalt, rompant une liaison P–F robuste et formant un complexe cobalt–fluorure bien défini. En revanche, BF4−, habituellement considéré comme le plus « fragile » des deux, refuse de céder un fluorure dans le même environnement. Il se positionne plutôt dans un agencement stable lié au centre de cobalt sans accomplir l’étape de rupture de liaison.
Observer l’appariement et le mouvement des ions
Pour comprendre ces comportements contrastés, les auteurs ont utilisé une combinaison de techniques RMN de haute résolution et de calculs quantiques‑chimiques. Des expériences de RMN de diffusion ont mesuré la vitesse de déplacement des espèces positives et négatives en solution, révélant ainsi le degré d’appariement ionique. Ces mesures ont montré que BF4− forme une paire ionique plus proche et plus persistante avec le complexe de cobalt que PF6−. La cavité Py4Im positionne l’anion directement sous l’anneau imidazolidine, où des liaisons hydrogène provenant du N–H et des groupes C–H voisins le maintiennent en place. Les calculs informatiques ont confirmé que cet appariement directionnel plus fort avec BF4− stabilise tellement l’état initial que la rupture de la liaison B–F devient légèrement défavorable, même si cette liaison est intrinsèquement plus faible que la liaison P–F dans PF6−. PF6−, en s’appariement plus lâche, peut s’approcher, transférer un fluorure au cobalt, puis s’éloigner sous forme de PF5, conduisant à un complexe de cobalt porteur de fluorure thermodynamiquement accessible. 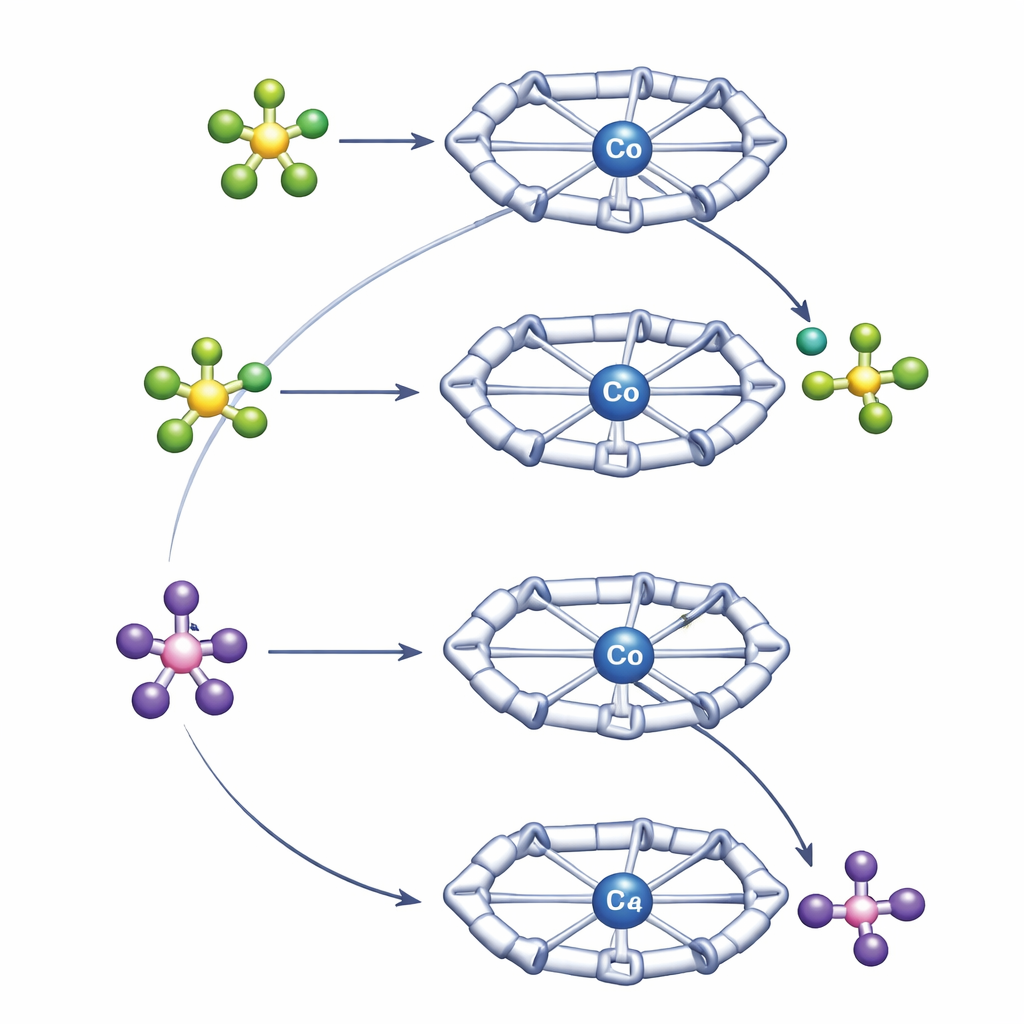
Transformer un fluorure lié en un outil utile
Une fois formé, le complexe cobalt–fluorure n’est pas une impasse. Les auteurs montrent qu’il se comporte comme une source de fluorure nucléophile — en termes plus simples, il peut fournir du fluorure à des partenaires chargés positivement ou pauvres en électrons. En solution, cette espèce cobalt–fluorure transfère proprement du fluorure à des centres carbonés réactifs, à des atomes de silicium dans des chlorosilanes, et à des chlorures d’acyle, générant des fluorures organiques tandis que le complexe de cobalt repasse à sa forme chlorure ou se lie au nouveau partenaire. Astucieusement, l’équipe démontre aussi que BF4− peut être amené à céder du fluorure si une base séparée est présente pour « piéger » le fragment BF3 restant. Cela convertit la voie autrement réticente de BF4− en une route qui donne également le même produit cobalt–fluorure.
Que signifie cela pour la conception de catalyseurs plus intelligents
Pour un non‑spécialiste, le message clé est que des ions autrefois considérés comme des sels de fond inertes peuvent en réalité orienter les réactions chimiques de façon puissante. En sculptant une poche précise autour d’un centre métallique et en contrôlant la force de l’appariement des anions avec celui‑ci, les auteurs ont inversé la réactivité attendue de deux espèces presque identiques. PF6−, normalement perçu comme très robuste, devient la source de fluorure la plus accessible, tandis que BF4− est verrouillé par un appariement plus fort à moins que le système ne soit assisté. Ce travail fournit une feuille de route pour utiliser conjointement la conception de ligands et le choix du contre‑ion afin d’ajuster la réactivité d’un complexe métallique — une idée qui pourrait influencer des domaines allant de la catalyse homogène à la conception d’électrolytes pour batteries avancées, où les « partenaires silencieux » en solution peuvent être tout sauf passifs.
Citation: Tarifa, L., Cano-Asensio, J., López, J.A. et al. Cooperative anion activation at a cobalt center through ion pairing and ligand design. Nat Commun 17, 2469 (2026). https://doi.org/10.1038/s41467-026-69257-8
Mots-clés: complexes de cobalt, anions faiblement coordonnants, transfert de fluorure, appariement ionique, conception de ligand