Clear Sky Science · fr
Des hépatocytes reprogrammés fonctionnellement par des cellules de cancer colorectal riches en KIAA1199 favorisent l'accumulation de neutrophiles Egr1+ pro‑métastatiques
Quand le cancer du côlon vise le foie
La plupart des gens imaginent la dissémination du cancer comme des cellules voyous qui se détachent et dérivent vers de nouveaux organes. Cette étude décrit une histoire plus inquiétante : les tumeurs colorectales peuvent discrètement reprogrammer le foie bien avant l'arrivée de cellules cancéreuses, préparant un « sol » accueillant dans lequel de futures tumeurs s’enracinent facilement. Comprendre cette phase de préparation cachée pourrait ouvrir la voie à des traitements visant à empêcher les métastases hépatiques — principale cause de décès dans le cancer colorectal — avant qu’elles ne commencent.
Une mise en place furtive avant l’arrivée des tumeurs
Le cancer colorectal colonise souvent le foie, mais seules certaines tumeurs le font de façon agressive. Les auteurs se sont concentrés sur une molécule appelée KIAA1199, abondante dans les cancers colorectaux à haut risque. Chez la souris et dans des échantillons de patients, les tumeurs riches en KIAA1199 ne se contentaient pas de croître plus rapidement : elles préparaient aussi le foie à devenir un « niche pré‑métastatique », un microenvironnement particulièrement favorable aux cellules cancéreuses entrantes. Même lorsque des tumeurs hépatiques étaient implantées expérimentalement à partir d’une source distincte, les animaux porteurs de tumeurs colorectales KIAA1199‑élevées développaient beaucoup plus de métastases hépatiques et mouraient plus tôt. Cela montre que des signaux issus de la tumeur primaire, et pas seulement des cellules cancéreuses circulantes, remodelaient le foie à l’avance.
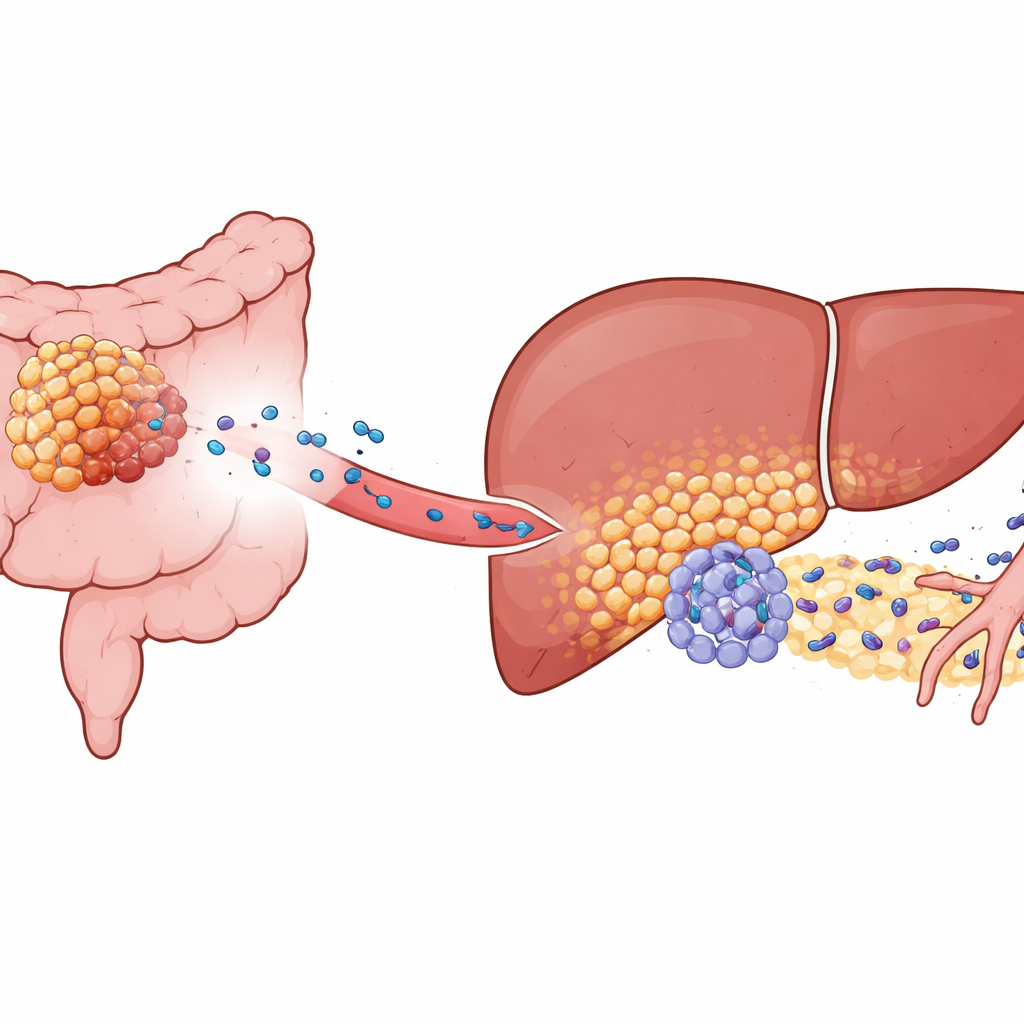
Des cellules hépatiques reprogrammées en auxiliaires tumoraux
En creusant davantage, les chercheurs ont utilisé le séquençage unicellulaire et le cartographage spatial pour examiner le tissu hépatique à haute résolution. Ils ont découvert un sous‑ensemble distinct d’hépatocytes — normalement les cellules travailleuses du foie — qui avaient été « reprogrammés fonctionnellement ». Ces cellules n’apparaissaient que lorsque des tumeurs KIAA1199‑élevées étaient présentes. Plutôt que de gérer silencieusement le métabolisme, les hépatocytes altérés adoptaient un profil métabolique plus proche de celui des cellules malignes et réduisaient l’activité d’un régulateur protecteur appelé PPARγ, qui aide habituellement à limiter l’inflammation et les réponses au stress. Avec PPARγ supprimé, ces hépatocytes ont commencé à produire de fortes quantités d’une protéine nommée SAA2, qu’ils libéraient dans leur environnement, en particulier à la frontière où le tissu hépatique rencontre les cellules tumorales envahissantes.
Transformer des défenseurs ordinaires en neutrophiles pro‑métastatiques
Les neutrophiles — globules blancs surtout connus pour combattre les infections — se comportaient aussi de façon anormale dans ce foie préparé. Les auteurs ont identifié un sous‑ensemble particulier portant une signature « Egr1+ », ainsi nommé d’après un facteur de transcription qui modifie la façon dont ces cellules fonctionnent. Plutôt que d’arriver déjà modifiés depuis la circulation sanguine, les neutrophiles semblaient être rééduqués localement par les hépatocytes reprogrammés. La SAA2 libérée par les hépatocytes se liait à un récepteur appelé FPR2 sur les neutrophiles voisins, activant une cascade interne PI3K‑AKT qui stabilisait l’activité d’Egr1. Le résultat était des neutrophiles plus durables et très actifs, sécrétant de grandes quantités de VEGFA, un puissant inducteur d’angiogenèse. Ces neutrophiles Egr1+ se regroupaient à l’interface tumeur‑foie, exactement là où de nouveaux vaisseaux fragiles émergent.
Construire des vaisseaux qui accueillent les cellules tumorales
L’étude montre que ces neutrophiles rééduqués ne sont pas des spectateurs — ils remodelent activement la vascularisation du foie. En culture cellulaire, les facteurs libérés par les neutrophiles Egr1+ incitaient les cellules endothéliales à croître, migrer et former des structures tubulaires rappelant des néovaisseaux. Chez la souris, l’ajout de neutrophiles Egr1+ augmentait les métastases hépatiques et accélèrait la mortalité. Bloquer des étapes clés de cette chaîne — soit le signal SAA2–FPR2 vers les neutrophiles, soit la voie PI3K‑AKT en aval — supprimait la survie des neutrophiles et la production de VEGFA, réduisant la croissance vasculaire et la dissémination métastatique. De même, restaurer l’activité de PPARγ dans les hépatocytes avec le médicament antidiabétique rosiglitazone réduisait les niveaux de SAA2, freinait l’émergence des neutrophiles Egr1+ et diminuait fortement les métastases hépatiques dans des modèles précliniques.
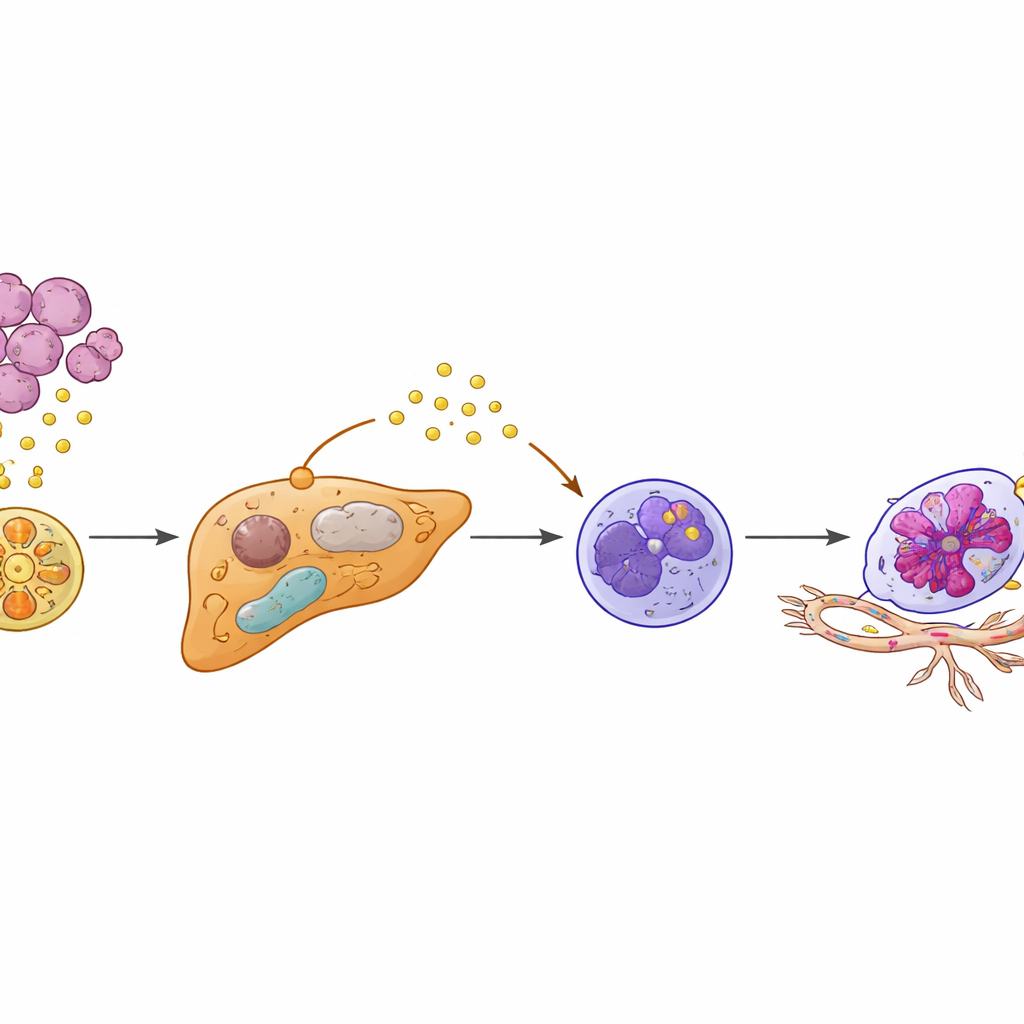
Du mécanisme à la prédiction et à la prévention
Parce que KIAA1199 dans les tumeurs et SAA2 dans le foie occupent une place clé dans cette cascade, les auteurs ont testé si ces protéines pouvaient aider à identifier les patients à haut risque de métastase hépatique. Dans plusieurs cohortes de patients, les personnes ayant des taux sanguins élevés des deux marqueurs étaient beaucoup plus susceptibles de développer des métastases hépatiques et de le faire plus rapidement. Un score combiné simple KIAA1199–SAA2 surpassait chacun des marqueurs pris isolément pour prédire le risque et a été intégré dans un « nomogramme » clinique estimant la probabilité individuelle d’extension hépatique sur les deux années suivantes. Ensemble, ces résultats dessinent un tableau clair : les cancers du côlon riches en KIAA1199 envoient des signaux véhiculés par des vésicules qui reprogramment les hépatocytes, lesquels convertissent à leur tour les neutrophiles voisins en complices durables promoteurs de néovaisseaux. En ciblant cet axe KIAA1199–PPARγ/SAA2–Egr1 — par des médicaments métaboliques, des agents modulant l’immunité, ou les deux — il pourrait être possible non seulement de traiter les métastases hépatiques existantes, mais aussi de les empêcher de s’implanter.
Citation: Li, L., Zhao, L., Cao, K. et al. Hepatocytes functionally reprogrammed by KIAA1199-high colorectal cancer cells favour the accumulation of pro-metastatic Egr1+ neutrophils. Nat Commun 17, 2462 (2026). https://doi.org/10.1038/s41467-026-69250-1
Mots-clés: métastase hépatique du cancer colorectal, niché pré‑métastatique, neutrophiles, reprogrammation des hépatocytes, microenvironnement tumoral